
肺肿瘤免疫预防新范式:LPS+褪黑素"去耐受化"联合,重启巨噬细胞抗癌力
LPS与褪黑素联用通过诱导M2型巨噬细胞凋亡预防肺癌
引言
据世界卫生组织统计,癌症已成为全球第二大死因,每年夺走约六分之一的生命。尽管手术、放化疗等传统手段仍是主流,但免疫疗法的迅猛进展为晚期及难治性肿瘤带来了曙光。巨噬细胞作为维持机体内环境稳态、抵御外来病原体的重要先天免疫细胞,具有高度可塑性。大量研究表明,肿瘤浸润巨噬细胞(TIM)是肿瘤微环境(TME)中一种重要的炎症细胞,依据功能表型不同,大致分为M1型和M2型。M1巨噬细胞主要表现出促炎和抗肿瘤作用,而M2巨噬细胞则表现出抗炎和促肿瘤活性。如果可以有目的地调节巨噬细胞,抑制巨噬细胞表达M2型的免疫抑制作用,上调M1型的抗原呈递和免疫激活功能,就有可能使机体发挥免疫功能来识别并杀死肿瘤细胞,起到肿瘤防治的目的。
肿瘤微环境(TME)中的肿瘤浸润巨噬细胞(TIM)是决定疗效的关键“开关”:促炎、抗原呈递能力强的M1型可杀伤肿瘤;而免疫抑制、促血管生成的M2型则加速肿瘤进展。因此,将TIM从M2“逆转”为并锁定于M1型,被视为提升免疫治疗响应率的核心策略之一。
经典M1诱导剂——LPS虽可瞬时激活巨噬细胞,但长期或高剂量暴露会触发 LPS-耐受,反而导致M2极化,削弱抗肿瘤效应。褪黑素参与调节广泛的生理功能,对免疫系统具有多效性,可抑制 PI3K/Akt 与 Jak/STAT3 两条关键信号轴,已被证实能够解除 LPS-耐受并维持M1表型。
本研究首次提出“LPS+ 褪黑素 ”联合策略:利用褪黑素阻断耐受通路,确保LPS持续驱动M1极化,从而在小鼠肺癌模型中实现持久的肿瘤预防效应。该发现不仅为克服巨噬细胞功能耗竭提供新思路,也为临床开发安全、可口服的免疫-代谢联合干预方案奠定理论与实验基础。
LPS与褪黑素联用通过诱导M2型巨噬细胞凋亡预防肺癌
摘要
背景和目标:
持续LPS刺激会使巨噬细胞向M2表型转化,从而导致免疫抑制。褪黑素具有改善睡眠、调节时差、增强免疫和抗肿瘤作用。本研究旨在观察褪黑素能否通过诱导M2型巨噬细胞凋亡来逆转持续LPS刺激导致的免疫抑制,从而预防肺癌,并探讨其潜在作用机制。
方法:
单独使用LPS或与褪黑素联用对巨噬细胞表型的影响,通过表面标志物、形态学变化、细胞因子、自噬及自噬外排等指标进行评估。抗癌效果在肺致癌模型和肺癌同种异体移植模型中得到验证。通过网络药理学预测了褪黑素相关靶点及作用通路。
结果:
单次LPS刺激使巨噬细胞极化为M1表型,而持续7天的LPS刺激则使巨噬细胞极化为M2表型。然而,持续LPS联合10 µM褪黑素治疗可抑制巨噬细胞向M2样表型的极化,并发挥持续抗肿瘤作用。在乌拉坦诱导的肺癌模型中,长期LPS给药(>4次)促进巨噬细胞向M2表型极化并加速肺癌发生,这种现象可通过巨噬细胞清除得以消除;而单独使用褪黑素或联合持续LPS治疗均可减少M2样巨噬细胞并阻止癌变。在Lewis肺癌同种异体移植物模型中,褪黑素能降低M2巨噬细胞数量,并增强短期LPS给药(<4次)的肿瘤抑制作用。网络药理学分析表明,褪黑素通过靶向多蛋白网络来调控巨噬细胞功能。
结论:
褪黑素作为巨噬细胞表型的关键调节因子,能够诱导LPS刺激的M2型巨噬细胞凋亡,从而逆转系统免疫抑制状态,实现肺癌预防作用。
引言
癌症是人类与疾病相关死亡的主要原因之一,关于癌症治疗的关注焦点多集中于靶向杀灭肿瘤本身,例如放射治疗、化学治疗和靶向治疗[1-5]。近年来,癌症免疫治疗已成为提升患者生存率最有希望的治疗支柱之一[6,7]。与其他癌症治疗手段不同,癌症免疫治疗通过激活宿主免疫系统或缓解肿瘤微环境中的"免疫耗竭"来清除癌细胞[8]。一线抗CTLA4疗法的数据分析显示,20%的晚期转移性黑色素瘤患者获得了前所未有的长期生存率,这一鼓舞人心的数值远超其他治疗方案,标志着癌症免疫治疗领域取得重大突破,为"超级幸存者"概念在不可治愈癌症患者中提供了现实希望[9,10]。然而即便最具前景的PD-1抑制剂——作为免疫检查点阻断(ICB)疗法的代表能介导耗竭T细胞再生——其总体生存获益在许多实体瘤中仅维持在20%左右;此外,CAR-T细胞疗法据报道可能导致脑水肿和细胞因子释放风暴[11] 。最新临床报告显示,9%的癌症患者使用PD-1抑制剂后出现肿瘤加速生长及超进展现象,这表明现有癌症免疫治疗方案亟待优化。当前免疫治疗主要激活肿瘤浸润性T淋巴细胞和自然杀伤细胞,却忽视了微环境变化导致的T细胞功能异常状态,包括衰老、耐受、耗竭和失能等[12]。事实上,抗肿瘤T细胞免疫疗法最初显示出应答反应,但随后在长期抗原暴露过程中因肿瘤相关炎症细胞形成的免疫抑制微环境所诱发的"免疫耗竭"而产生耐药性[13]。显然,有效的肿瘤免疫排斥不仅依赖于抗原暴露诱导的适应性免疫应答,还取决于先天免疫监视调控的微环境[14]。
肿瘤浸润巨噬细胞(TIMs),M2样巨噬细胞,是浸润肿瘤微环境的主要炎症细胞,负责形成免疫抑制微环境并促进肿瘤进展[15]。如果巨噬细胞介导的吞噬作用受到抑制,就会导致肿瘤免疫逃逸现象发生[16]。临床研究表明,TIMs与多种癌症的高肿瘤分级及不良预后呈正相关。在小鼠癌症模型中,清除或重编程TIMs可逆转其促肿瘤功能[17,18]。此外,先天性巨噬细胞在CD8+细胞毒性T细胞的瘤内浸润和长效记忆淋巴细胞的形成过程中也起着关键作用。因此,靶向TIMs以唤醒先天性免疫已成为癌症免疫治疗的新策略[19]。然而,迄今为止,抗TIM疗法不仅存在全身毒性风险,还可能被巨噬细胞池快速适应并逃逸[19]。众所周知,活化巨噬细胞可极化为抗肿瘤M1表型和促肿瘤M2表型[20]。LPS可诱导巨噬细胞向M1表型极化,但持续刺激会导致免疫耐受[21]。褪黑激素作为松果体分泌的神经激素,具有改善睡眠、调节时差、增强免疫和抗肿瘤作用[22]。本研究旨在探讨LPS与褪黑素联合应用能否通过诱导M2型巨噬细胞凋亡,从而产生持久的肺癌预防效应。
结果
一、与M1巨噬细胞相比,M2巨噬细胞对LLC细胞具有相反的作用
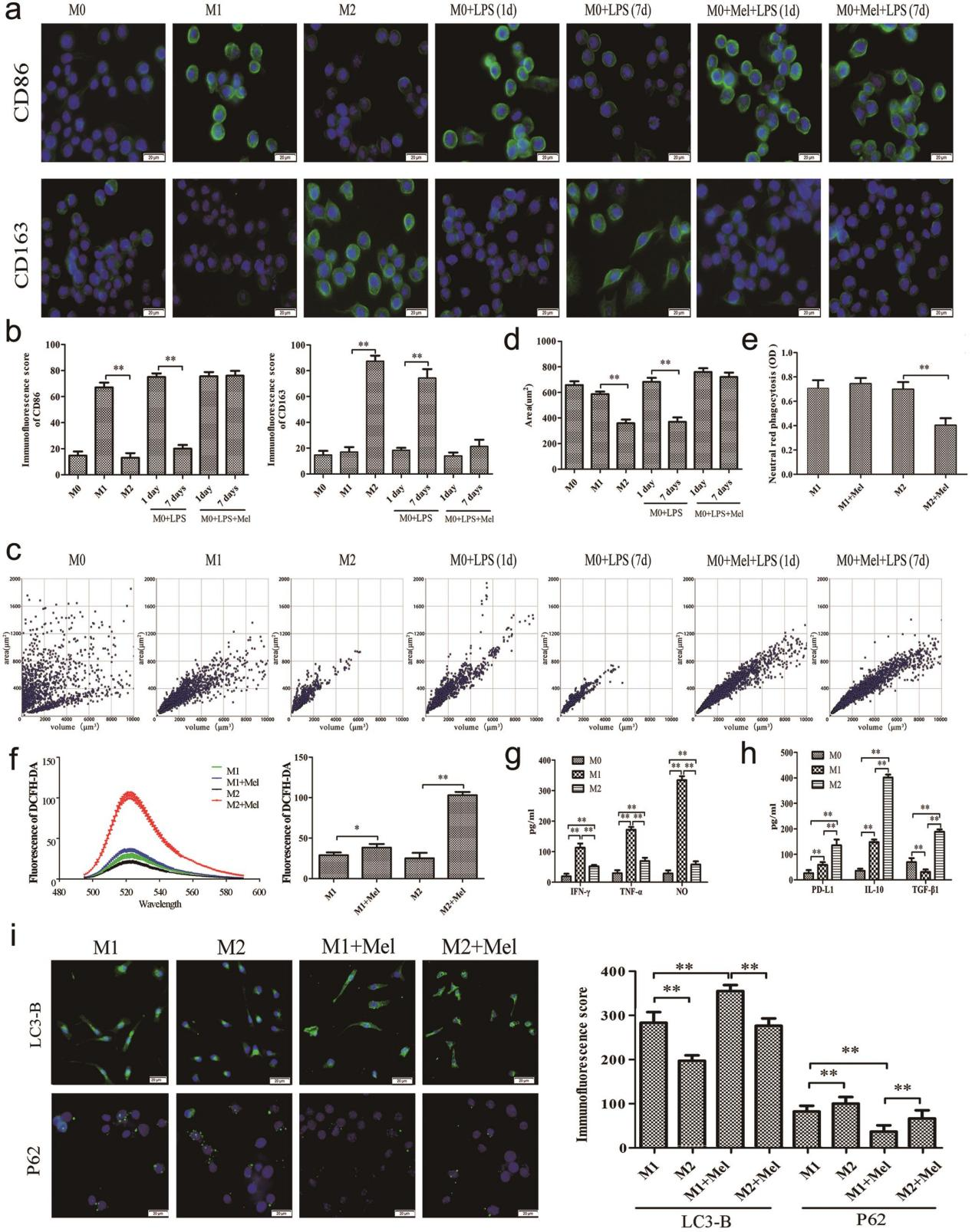
图1. M1型与M2型巨噬细胞存在差异。
据报道,具有M2样特征的癌症相关巨噬细胞会发挥促肿瘤作用,这与展现抗肿瘤功能的M1样巨噬细胞形成鲜明对比。为探究这些特性,我们通过短期单一LPS刺激诱导Raw264.7巨噬细胞极化为M1样细胞,通过长期单一LPS刺激诱导为M2样细胞。正如预期,M1样细胞表面CD86表达量高,M2样细胞表面CD163表达量高(图1a、b),细胞分布也显示出它们的形态变化(图1c、d)。在中性红吞噬实验中,M1细胞与M2细胞无显著差异(图1e);但M2样细胞的活性氧(图1f)、IFN-γ、TNF-α、NO水平下降(图1g),而程序性死亡PD-L1、IL-10、TGF-β1水平升高(图1h)。与此同时,M2样细胞表现出自噬和自噬流出的减弱,表现为LC3-B减少和p62增多(图1i)。在功能上,M1样细胞对LLC细胞的细胞溶解活性强于M2样细胞(图2a),M1细胞条件培养基(M1-CM)对LLC细胞增殖的抑制作用也更强(图2b),并导致比M2细胞条件培养基(M2-CM)更高的凋亡率(图2c)。由于MTT实验显示对照组培养基与M0条件培养基无显著差异,且考虑到本实验旨在研究LPS与褪黑素联合作用对巨噬细胞预防肺癌的影响,后续实验不再使用M0条件培养基作为阴性对照。此外,M1样细胞与NK细胞共培养可降低NK细胞的PD-1表达,而M2样细胞则促进该表达——这种效应可通过在M2样细胞(而非M1样细胞)中预施MβCD、抗TGF-β1抗体和抗IL-10抗体来阻断,表明M2巨噬细胞对NK细胞功能的影响具有脂质筏/细胞因子依赖性作用(图2d)。与此结果一致的是,M1条件培养基促进了NK细胞对LLC细胞的免疫清除(图2e),而M2条件培养基则抑制了这一作用。
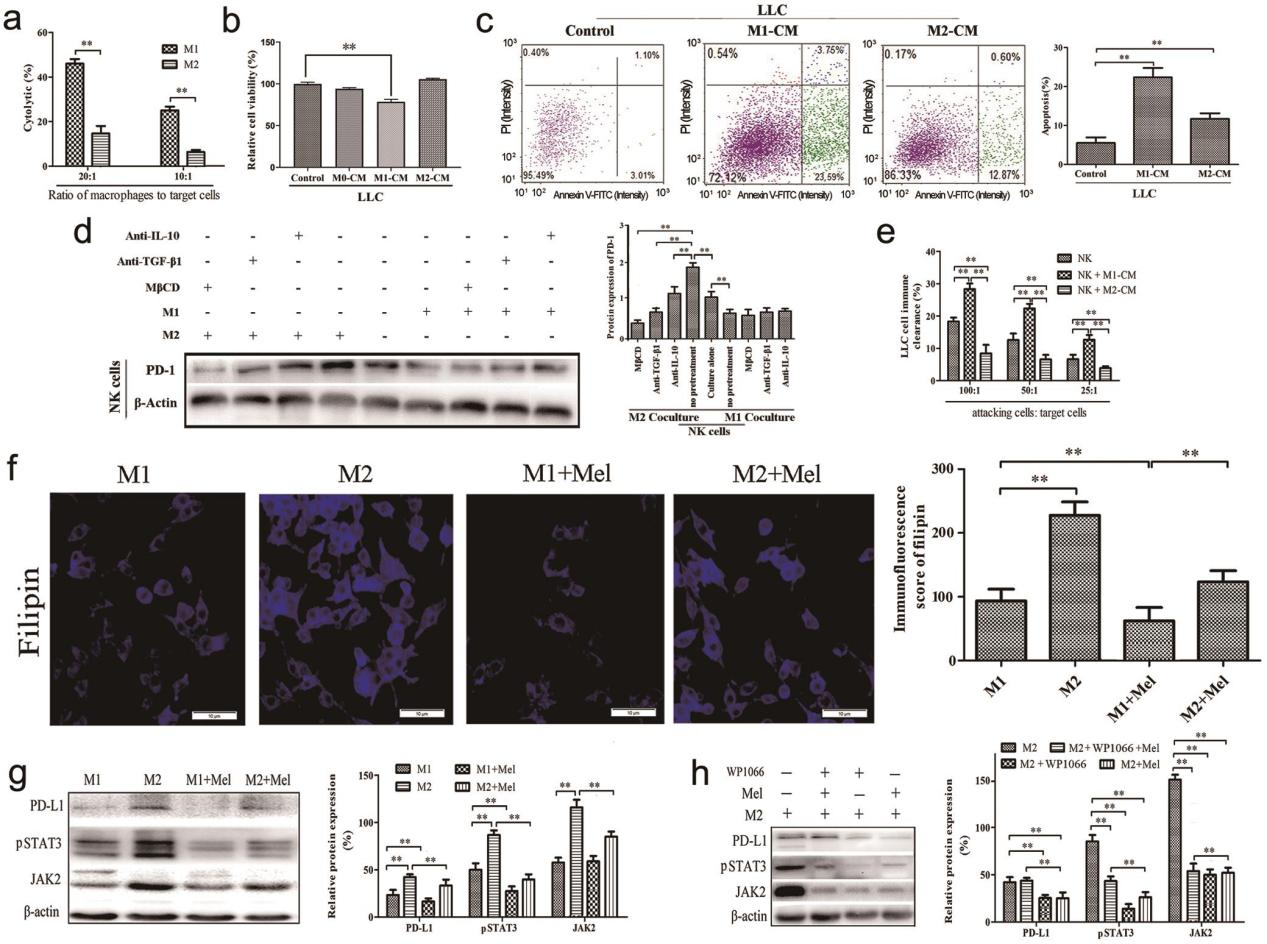
图2. M1型和M2型巨噬细胞对LLC细胞和NK细胞具有不同作用。
二、褪黑素通过减少M2型巨噬细胞来逆转巨噬细胞对LPS的耐受性
巨噬细胞可能对LPS产生耐受性,这种效应会持续一段时间[30]。为探究巨噬细胞如何形成LPS耐受性,我们观察了褪黑素与LPS对巨噬细胞极化的影响。正如预期,持续LPS处理导致巨噬细胞免疫分型从M1型向M2型转变——表现为表面标志物CD86表达下降而CD163表达上升(图1a、b),这一结果通过形态学变化得到进一步验证(图1c、d)。在10µM浓度下,褪黑素虽未影响细胞活力,但能在重复LPS处理条件下减少M2型巨噬细胞(图1a-d)。同时,褪黑素可促进巨噬细胞从M2向M1的功能性转变,例如增加ROS生成(图1f)、增强自噬及自噬外排(图1i)、减少脂筏形成并抑制JAK2/STAT3通路激活(图2f、g)。褪黑素对JAK2/STAT3激活及PD-L1生成的抑制作用可被WP1066减弱或阻断(图2h)。
三、褪黑素通过抑制巨噬细胞M2表型逆转氨基甲酸乙酯诱导的肺癌模型中LPS介导的致癌作用
为阐明巨噬细胞在癌变过程中的影响,我们研究了乌拉坦诱导的小鼠肺癌模型中巨噬细胞的免疫表型。该模型通常用于探究肺癌的基础生物学特性,并寻找肺癌的新型干预策略。在本研究中,实验小鼠连续十二周接受褪黑素或LPS注射,至第十三周时,肉眼可见肺癌结节形成(图3a)。对照组肺癌结节数量为26.2±4.1个,肿瘤组织学异质性可忽略不计(图3b)。正如预期,对照组肺泡腔内巨噬细胞浸润程度与肺癌发展呈正相关(图3c,f),这些巨噬细胞通过表面CD86低表达和CD163高表达呈现出M2型极化表型(图3c-f)。与该结果一致,与正常小鼠相比,对照组小鼠肺泡腔和血清中IFN-γ、IL-2和TNF-α水平下降,而白IL-10、TGF-β1和ROS水平升高(图3g、h),表明存在免疫耐受和慢性损伤。单独使用LPS并不能阻止肺癌发生,反而促进了这些现象(图3a、b),与对照组小鼠相比,巨噬细胞表面CD163以及ROS、TGF-β1和IL-10水平均有所上升(图3c-f),提示M2型巨噬细胞极化。褪黑素和LEC介导的巨噬细胞清除均能抑制肺癌发生(图3a、b),与对照组相比,巨噬细胞表面CD86与CD163的比例以及Th1型细胞因子(IFN-γ和IL-2)与Th2型细胞因子(IL-10和TGF-β1)的比例均有所增加(图3c-f),表明免疫监视功能得到恢复。值得注意的是,褪黑素与LPS的联合治疗逆转了LPS促进肺癌发生的作用(图3a、b),同时伴随着巨噬细胞表面标志物CD86和CD163所指示的M2型巨噬细胞减少,以及IFN-γ、IL-2、TNF-α、IL-10、TGF-β1和ROS水平的下降(图3c-f)。
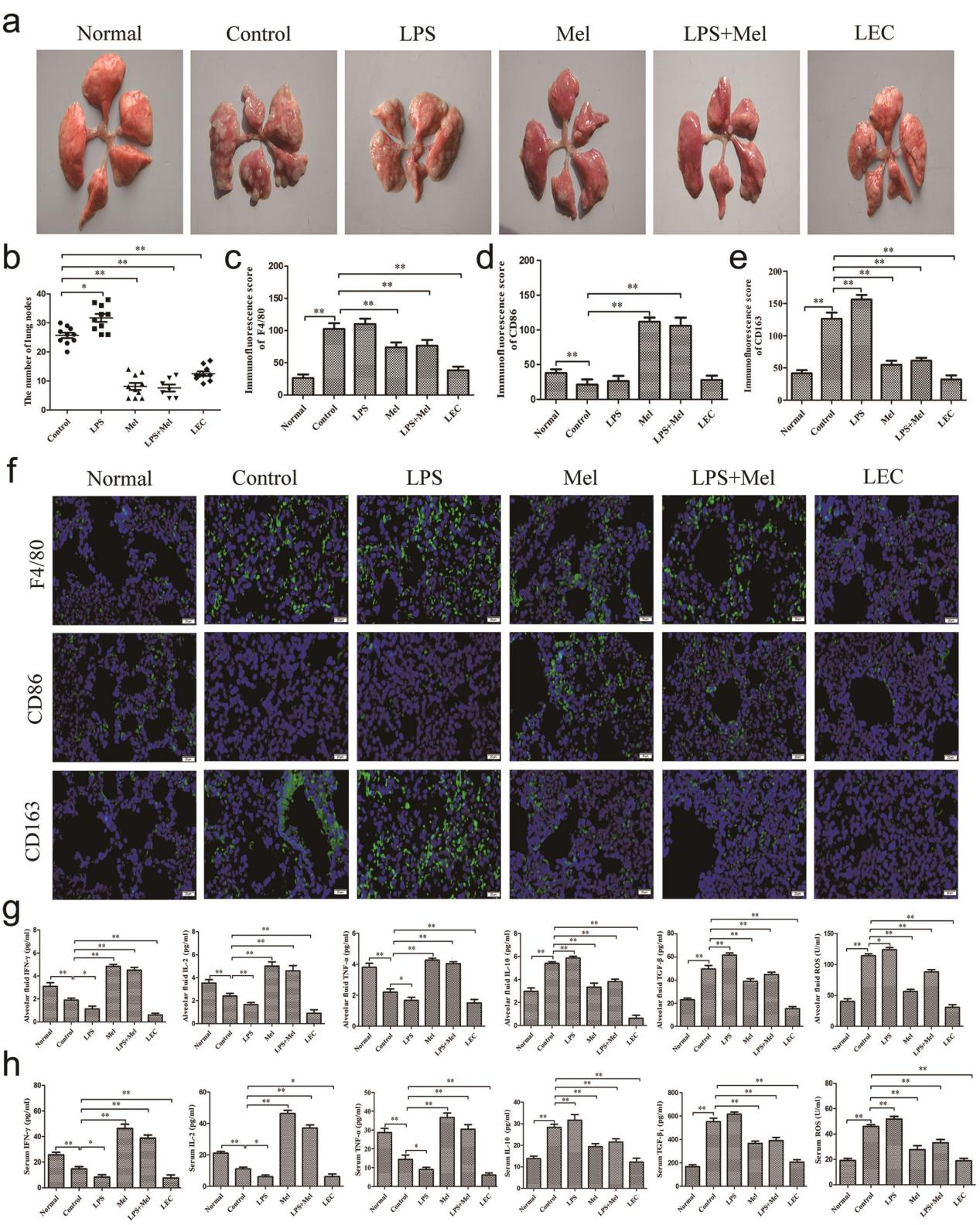
图3. 巨噬细胞影响氨基甲酸乙酯诱导的肺癌发生。
自然杀伤(NK)细胞在抗肿瘤免疫中发挥重要作用。为探究巨噬细胞是否参与NK细胞相关抗肿瘤功能,我们检测了脾脏PD-1+ NK细胞与记忆性NK细胞(NKG2C+ NKG2A−)的比例。结果显示:与正常小鼠相比,对照组小鼠脾脏PD-1+ NK细胞比例显著升高,而脾脏记忆性NK细胞比例明显下降(图4a、b);LPS处理会加剧这种趋势,但单独使用褪黑素、或褪黑素联合LPS及LEC诱导的巨噬细胞清除处理可缓解该现象(图4a、b)。这些变化趋势与巨噬细胞表型改变相一致,提示M2型巨噬细胞对NK细胞具有抑制作用。与此结果一致的是,肺组织出现了更明显的炎症细胞浸润现象,对照组小鼠肺组织中伊文思蓝染色(图4c)与CD31免疫荧光(图4d)较正常组显著增加,提示存在慢性炎症与血管新生现象。免疫组化结果显示,与正常组相比,对照组肺组织PD-1表达升高而iNOS表达降低(图4e),表明存在免疫抑制微环境。LPS可加剧这种慢性炎症、血管新生及免疫抑制微环境,而单独使用褪黑素或联用LPS与LEC诱导的巨噬细胞清除均可有效缓解上述病理改变(图4c-e)。
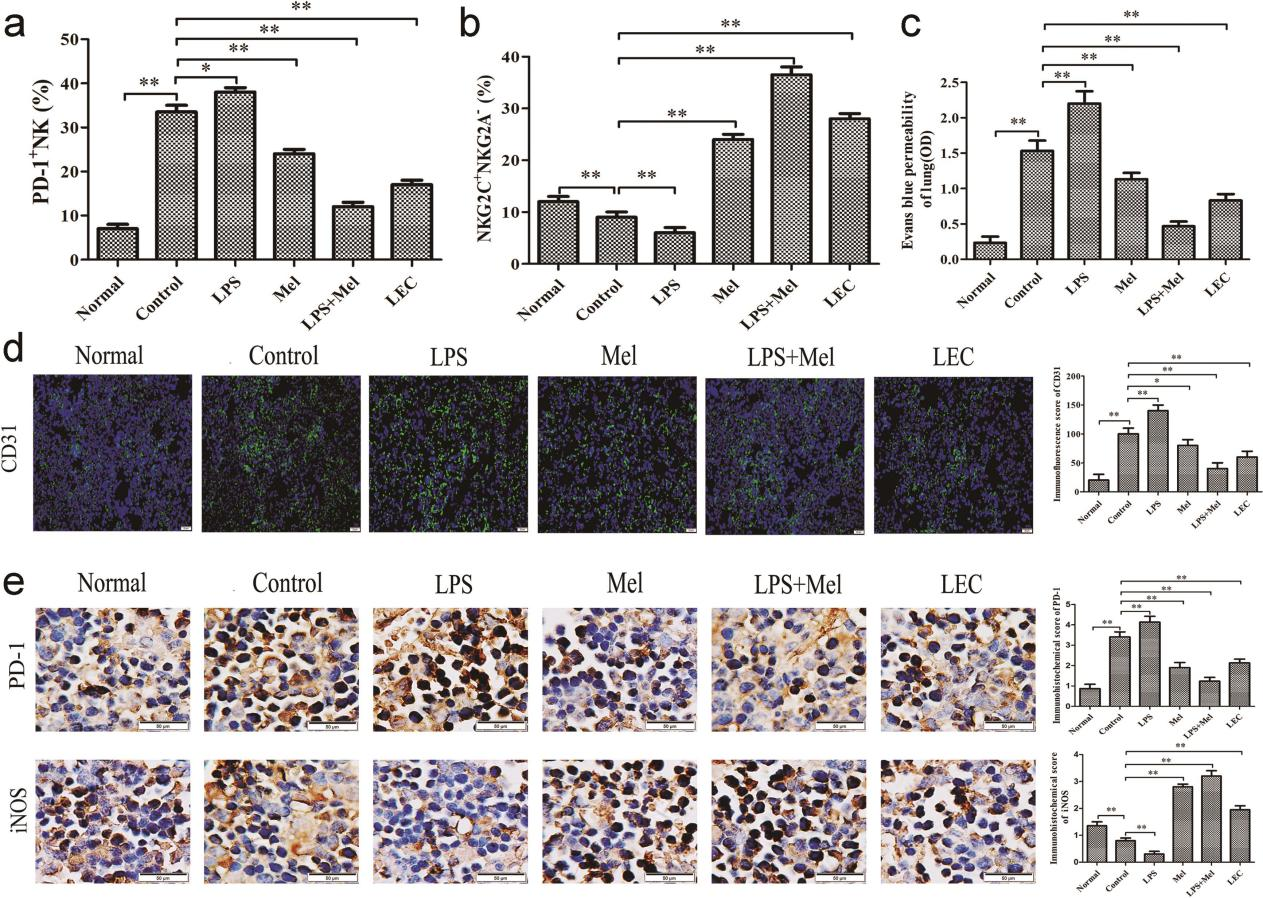
图4. 褪黑素在乌拉坦诱导的肺癌发生过程中维持免疫功能
四、褪黑素通过减少M2型巨噬细胞来促进LPS诱导的肿瘤抑制作用,并在LLC同种异体移植模型中增强短期LPS刺激引发的肿瘤免疫排斥反应。
为进一步研究不同表型巨噬细胞在肿瘤进展中的影响,我们采用LLC肿瘤的同种异体移植模型,同步向荷瘤小鼠分别静脉注射M1表型或M2表型的巨噬细胞。M2细胞注射表现出促癌效应,而M1细胞注射则显示出抑制肿瘤生长的作用(图5a、b),这分别表明了巨噬细胞的促肿瘤和抗肿瘤功能。与乌拉坦诱导的肺癌模型不同,在同种异体移植物模型中,褪黑素(20mg/kg)或巨噬细胞耗竭对新生物生长的抑制作用不显著,但LPS对肿瘤进展表现出显著的抑制效果(图5a、b)。LPS的肿瘤抑制作用通过褪黑素、巨噬细胞耗竭以及注射M1表型巨噬细胞得到增强(图5a、b)。在该模型中,LPS单独或联合M1细胞注射可增加伊文思蓝染料在肿瘤内的浸润,而LEC诱导的巨噬细胞耗竭、褪黑素及M2细胞注射则降低了这种浸润(图5c)。肿瘤内巨噬细胞表型检测显示,对照组中浸润的巨噬细胞表面CD163表达量高于CD86,表明其呈现M2表型(图5d)。这一现象在LPS处理组、M1细胞注射组、单独或联合使用褪黑素组中均发生逆转,而在M2细胞注射组则得到增强,表明LPS的抗肿瘤作用依赖于M1表型。脾脏自然杀伤细胞(NK细胞)分析表明,与正常小鼠相比,对照组小鼠PD-1阳性NK细胞增多而记忆性NK细胞减少(图5e、f)。然而与乌拉坦诱导的肺癌模型相反,本模型结果显示,LPS可减弱M2表型对自然杀伤细胞效应的抑制作用,而M1细胞注射、褪黑素及LEC诱导的巨噬细胞耗竭则能抑制该作用,M2细胞注射则促进该效应(图5e、f)。这一结果通过检测抗肿瘤相关血清ROS、IFN-γ、IL-2及TNF-α水平,以及促肿瘤相关血清IL-10和TGF-β1水平得到验证(图5g)。LPS抗肿瘤作用对M1表型的依赖性在LLC细胞再攻击免疫实验中得到进一步验证:再攻击对照组小鼠的肿瘤体积小于荷瘤正常小鼠,表明肿瘤再攻击组出现了肿瘤排斥现象(图6a)。这种肿瘤排斥效应可被LPS和褪黑素单独或联合使用所增强,而LPS与褪黑素的协同作用可被LEC诱导的巨噬细胞耗竭所消除(图6a)。腹膜巨噬细胞表型检测显示,肿瘤排斥反应与表面标志CD86和CD163指示的M1型细胞存在相关性(图6b)。脾脏NK细胞检测表明,与荷瘤正常小鼠相比,再攻击对照组小鼠的PD-1+ NK细胞减少而记忆性NK细胞增加(图6c、d),提示NK细胞免疫监视功能依赖于M1型细胞。这一结果还通过以下指标得到进一步验证:抗肿瘤相关血清ROS、IFN-γ、IL-2及TNF-α水平,以及促肿瘤相关血清IL-10和TGF-β1水平(图6e)。这些参数可能因单独或联合使用LPS和褪黑素而向免疫监视方向转变,而LPS与褪黑素的协同效应可被LEC诱导的巨噬细胞耗竭所消除(图6b-e),这表明巨噬细胞在二次免疫和免疫记忆过程中发挥着不可或缺的关键作用。
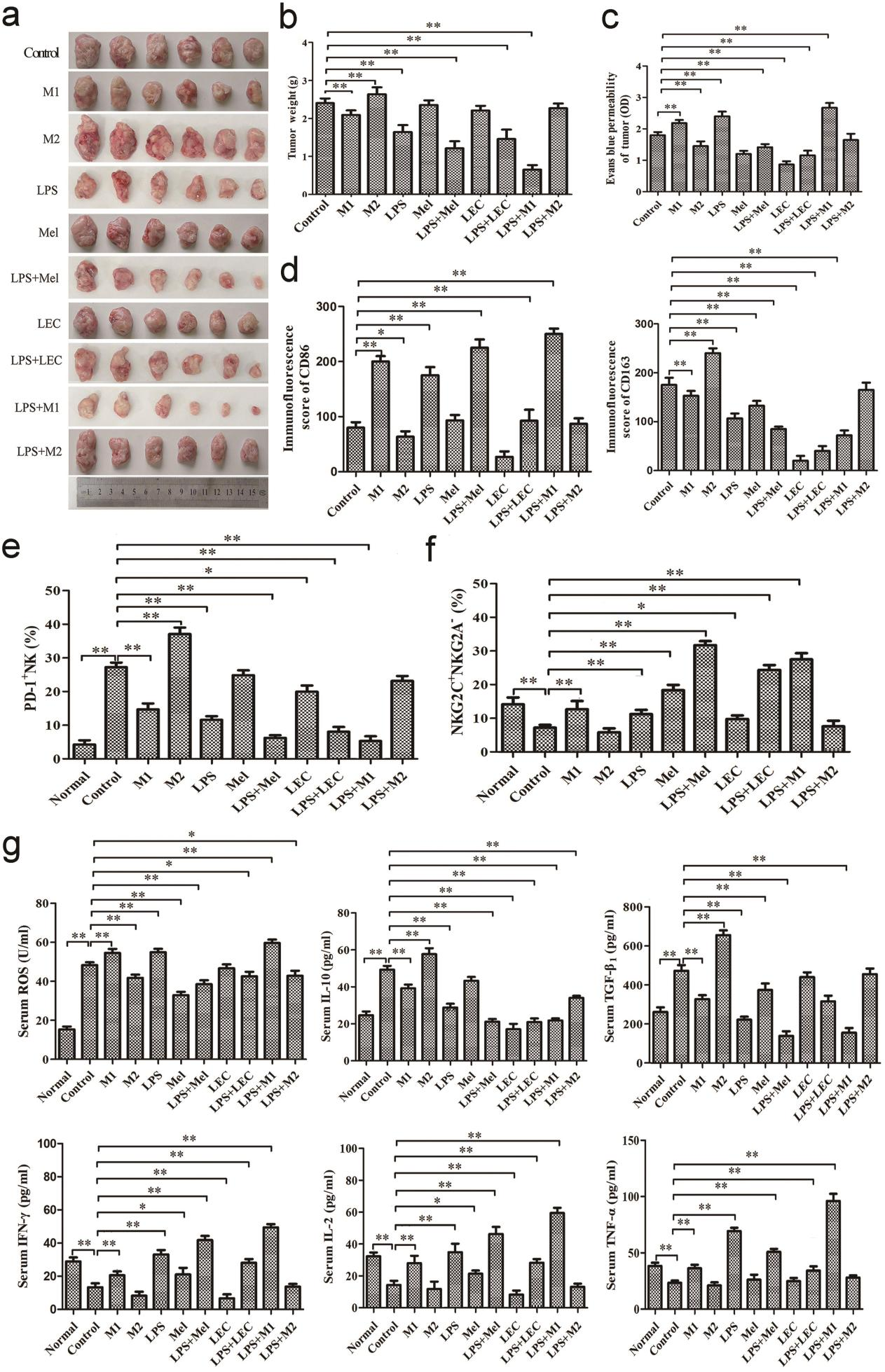
图5. 褪黑素通过减少M2型巨噬细胞来增强短期LPS刺激的抑瘤效应。
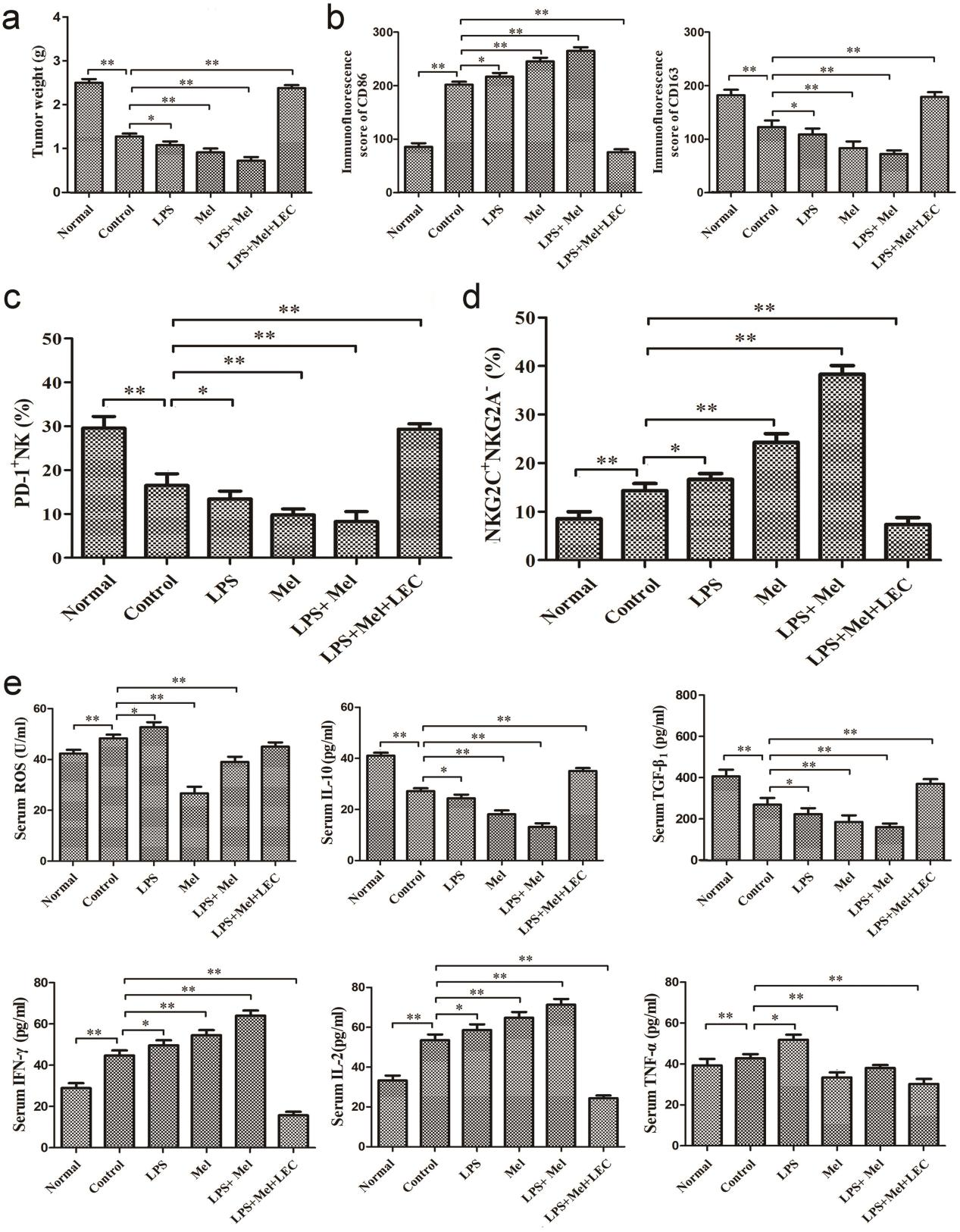
图6. 褪黑素通过减少M2型巨噬细胞维持肿瘤免疫排斥
讨论
癌症可能源于不同生理过程的改变,由于病因不明和遗传异质性而难以治愈。基于自愈能力,免疫治疗已被寄予厚望来对抗多种癌症类型[31-36]。当前针对不同细胞检查点控制器的免疫疗法,由于免疫抑制性肿瘤环境而出现先天或获得性耐药,这指引着癌症免疫治疗的发展方向[37]。癌症免疫治疗的目标是激发持久的免疫监视作用,维持抗肿瘤免疫力[38]。巨噬细胞作为先天免疫系统中的一线免疫应答者,负责肿瘤中无法消退的炎症反应。了解巨噬细胞在肿瘤免疫反应中的作用,有助于开发新的免疫治疗策略并提高免疫治疗的应答率[39]。巨噬细胞可表现出促肿瘤或抗肿瘤效应,这取决于其免疫分型。最新研究表明,靶向肿瘤浸润髓系细胞(TIMs)能够逆转免疫抑制性肿瘤微环境,并激发强烈的肿瘤特异性免疫应答——这一现象与以下事实相符:免疫抑制性TIMs在肿瘤微环境中大量存在,且与不良预后呈正相关。因此,维持巨噬细胞的抗肿瘤表型而非完全清除肿瘤浸润性巨噬细胞(TIMs),代表了一种新的癌症免疫治疗策略[40,41]。LPS是巨噬细胞介导炎症的有效触发剂,在动物肿瘤模型中被证实为有效的抗肿瘤剂[41]。然而由于LPS诱导的耐受性——即巨噬细胞反应性改变的状态,其在人类癌症治疗中的应用并不成功,这种状态会导致肿瘤反应不佳,并且是继发感染的主要原因。诺瓦科维奇(Novakovic)团队此前研究发现,β-葡聚糖能够逆转LPS诱导的免疫耐受表观遗传状态,从而降低脓毒症整体死亡率[42]。本研究首次证明,LPS与褪黑素联用能够抑制巨噬细胞向M2样细胞的极化过程,从而产生持久的抗肿瘤效应,这为逆转LPS耐受性提供了一种新型有效策略。
巨噬细胞可被不同刺激物激活分化为M1和M2型巨噬细胞,从而发挥不同功能。众所周知,LPS能够促使巨噬细胞向M1表型极化,这种表型具有促炎和抗肿瘤效应[43]。与这些功能一致的是,在动物模型中,LPS对移植瘤展现了治疗效果[44]。在小型临床试验中,LPS还具有缓解癌症患者症状、稳定病情的功效[45]。尽管多年来对耐受性巨噬细胞中各种表观遗传和遗传变化进行了深入研究,但导致LPS耐受的统一机制仍不明确[49-51]。据报道,耐受性巨噬细胞中大多数LPS靶基因呈现低反应性[52]。本研究中,短期LPS刺激可诱导Raw264.7巨噬细胞极化为M1样细胞,而长期LPS刺激则促使其向M2样细胞转化,这表明巨噬细胞对LPS耐受的关键过程。
褪黑素是一种具有多重功能的分子,具有多种生理和药理作用[53] 。该分子通常在免疫和炎症反应中扮演平衡者角色,起到制衡调节作用[54]。一般而言,M1型肿瘤浸润巨噬细胞被认为是肿瘤早期阶段的主导表型,而M2型则在癌症发展进程中更具支配性[44] 。褪黑素作为一种免疫刺激剂,在正常或免疫抑制状态下能促使免疫细胞进入活化状态,从而更有效地清除病原体;同时它也可作为免疫调节剂发挥作用。免疫抑制因子能促使免疫细胞进入失活状态,在过度炎症条件下抑制炎症反应[55,56]。多项研究发现褪黑素具有突破免疫抑制性肿瘤微环境的惊人潜力[57]。基于这些研究结果,我们认为LPS与褪黑激素的联合使用能够在维持巨噬细胞对LPS敏感性的同时,有效限制过度的病原性刺激,从而避免出现"巨噬细胞衰竭"的表型。这一发现与我们的实验数据高度吻合。本研究中,LPS与褪黑素的联合使用在乌拉坦诱导的肺癌模型和LLC同种异体移植模型中实现了最佳癌症预防效果,且未出现显著副作用。此外,我们发现反复接受LPS刺激的巨噬细胞会呈现高水平的表面脂筏结构和JAK2/STAT3通路激活,这种现象会同时阻碍M1型极化和免疫应答;而褪黑素则能降低表面脂筏水平并抑制JAK2/STAT3的激活。生物信息学分析表明,褪黑素与巨噬细胞调节相关的潜在靶点主要涉及"炎症反应"、"信号转导"、"细胞增殖"、"先天免疫反应"及"凋亡过程的负调节",这提示褪黑素通过作用于"Jak-STAT信号通路"、"Toll样受体信号通路"和"趋化因子信号通路"等多靶点网络,诱导M2型巨噬细胞凋亡从而逆转LPS刺激引发的免疫耐受。本研究揭示,褪黑素能诱导M2巨噬细胞凋亡并增强短期LPS刺激的抗肿瘤效应,为LPS的临床应用提供了安全有效的策略,该治疗方案值得深入探究。
未来研究方向
LPS作为革兰氏阴性菌细胞壁成分,曾被用于肿瘤消融治疗多年。LPS既可能作为强效抗肿瘤剂,也可能成为促癌剂,具体取决于免疫状态。我们的研究表明,LPS与褪黑素联用可促进肿瘤免疫排斥,这表明M2型巨噬细胞极化与LPS刺激引发的"巨噬细胞耗竭"极化现象为预防肺癌提供了一种新型治疗策略。该策略旨在重塑肿瘤微环境中的巨噬细胞功能而非直接杀伤巨噬细胞,这种疗法在系统与免疫之间建立和谐关系,具有临床转化价值,值得深入探索。
结论
综上所述,巨噬细胞跟肿瘤发生、发展密切相关,M2巨噬细胞对于肿瘤的进程起到促进作用。巨噬细胞经过LPS连续诱导使极化的M1产生LPS耐受转化为M2巨噬细胞,褪黑素与LPS联用解除由M1型巨噬细胞发生LPS耐受,使巨噬细胞维持M1型,其机制跟抑制PI3 K/AKT和Jak/Stat3两条信号通路密切相关。我们的研究发现褪黑素是维持巨噬细胞表型以保持系统免疫监视功能的关键调节因子,它能够诱导LPS刺激的M2型巨噬细胞凋亡,逆转持续LPS刺激的促肿瘤效应,为免疫增强型肺癌预防提供了新策略。
免责声明:
以上部分内容来源于外网我们重在信息分享,版权归属原作者或原刊发平台所有,如有侵权、信息有误或其他异议,请联系处理,我们将在24小时内删除或整改。
复合免疫 健康活力





























