
LPS激活肺泡巨噬细胞:肺肿瘤细胞毒性效应的新机制
LPS激活的肺泡巨噬细胞通过细胞间结合机制对肺肿瘤细胞具有细胞毒性
近年来,肺肿瘤的发病率和死亡率持续上升,成为全球范围内的重大健康挑战。肺肿瘤细胞毒性是肿瘤治疗中一个重要的研究方向,旨在通过诱导肿瘤细胞死亡来抑制肿瘤生长。肺泡巨噬细胞作为免疫系统中的关键细胞,其活化状态和功能对肿瘤微环境有着重要影响。脂多糖(LPS)作为一种免疫调节剂,已被证实能够激活巨噬细胞,增强其抗肿瘤能力。然而,LPS激活肺泡巨噬细胞对肺肿瘤细胞的细胞毒性作用及其潜在机制尚未完全阐明。
本研究旨在探讨LPS激活的肺泡巨噬细胞如何通过细胞间结合机制对肺肿瘤细胞产生细胞毒性效应。通过深入分析巨噬细胞的活化状态、细胞毒性因子的释放以及肿瘤细胞凋亡途径,我们将揭示LPS诱导的免疫反应在肺肿瘤治疗中的潜在作用。这一发现不仅增进了我们对肿瘤免疫逃逸机制的理解,而且为开发新的肿瘤治疗策略提供了科学依据。随着研究的深入,LPS及其激活的巨噬细胞有望成为肺肿瘤治疗中的重要工具,为患者带来新的希望。
LPS激活的肺泡巨噬细胞通过细胞间结合机制对肺肿瘤细胞具有细胞毒性
摘要
背景:在肺肿瘤生物治疗中,通常与肿瘤细胞接触的局部巨噬细胞,如肺泡巨噬细胞和肿瘤相关巨噬细胞(TAMs),被认为是潜在的治疗目标。为了利用药物递送系统开发新的肺癌治疗方法,了解邻近巨噬细胞杀死肺肿瘤细胞的潜力及其机制至关重要。
材料和方法:A549,一种人肺腺癌细胞系,以及Lewis肺癌LLC1,一种小鼠肺癌细胞系,分别以1:10和1:5的比例与NR8383,一种大鼠肺泡巨噬细胞系,和AMJ2-C11,一种小鼠肺泡巨噬细胞系共培养。巨噬细胞通过LPS激活,并通过染料摄取法和3H-胸苷释放试验评估其对肿瘤细胞的细胞毒性。一氧化氮(NO)的产生通过Griess测定法估计,肿瘤坏死因子(TNF)-α和白细胞介素(IL)-1β则通过ELISA测量。
结果:使用NR8383时,观察到显著的巨噬细胞聚集和对A549细胞及LLC1细胞的细胞毒性。
引言
肺癌是导致男性和女性癌症死亡的主要原因(1)。尽管手术技术不断进步,放疗和化疗也有所发展,但该疾病患者的五年生存率仍不足15%(2)。由于肺癌的进展迅速,许多情况下无法进行手术,而非小细胞肺癌占日本肺癌病例的80%,对化疗具有耐药性(3)。因此,仍需开发新的创新疗法。
巨噬细胞存在于所有动物体内,以其在组织重塑、炎症和免疫中发挥的多种功能而著称,包括吞噬作用、细胞毒性以及分泌多种体液因子(4)。近年来,巨噬细胞被广泛分为两种类型:经典激活型巨噬细胞(M1)和替代激活型巨噬细胞(M2)(5)。M1型激活的巨噬细胞是高效的效应细胞,能够杀死微生物和肿瘤细胞,产生炎症细胞因子,并表达高水平的主要组织相容性复合体(MHC)分子。相比之下,M2型激活的巨噬细胞则诱导炎症反应和适应性Th1免疫,清除组织碎片,促进血管生成、组织重塑和修复(6)。此外,肿瘤细胞能够诱导巨噬细胞向M2型转变,从而促进肿瘤生长(6,7)。研究表明,将肿瘤相关巨噬细胞(TAMs)重编程为活化的M1型后,可在肿瘤组织中观察到抗肿瘤效应(8-10)。基于这些发现,若能通LPS等物质(11)将组织巨噬细胞激活为M1型,则有望有效清除肿瘤。
肺部存在大量具有清除异物功能的肺泡巨噬细胞(12)。由于其数量庞大且与肿瘤消退密切相关,若能通过特定给药方式将M1型巨噬细胞激活剂递送至肺部,肺泡巨噬细胞将成为肺癌免疫治疗的理想靶点。近期,干粉吸入器作为肺部给药装置已成功研发(13),更有针对结核感染动物肺泡巨噬细胞的抗结核干粉吸入制剂已问世(14,15)。因此,未来通过激活肺泡巨噬细胞可能成为克服此类疾病的有效手段。
然而,关于肺泡巨噬细胞如何杀死肺癌细胞的具体机制尚未完全明了。为了探索通过递送巨噬细胞激活药物来治疗肺肿瘤的可能性,需要进一步研究肺泡巨噬细胞的抗肿瘤功能。在本研究中,我们通过激活具有肺组织特异性特征的肺泡巨噬细胞,检测其是否能诱导对肺癌细胞的细胞毒活性,旨在为经肺部给药巨噬细胞激活剂的肺癌治疗奠定基础。
结果
激活的巨噬细胞对肺癌细胞的抗肿瘤效应(共培养实验)
为探究验证肺泡巨噬细胞能否对肺癌细胞产生抗肿瘤作用,本研究将A549细胞(人肺腺癌细胞)和LLC1细胞(小鼠肺癌细胞)分别与肺泡巨噬细胞(NR8383细胞和AMJ2-C11细胞)在有无LPS的情况下进行了共培养。通过观察生长速率评估细胞抑制效果,通过检测存活率评估细胞杀伤效果。
图1.肺泡巨噬细胞活化后对肺癌细胞的细胞毒性作用。
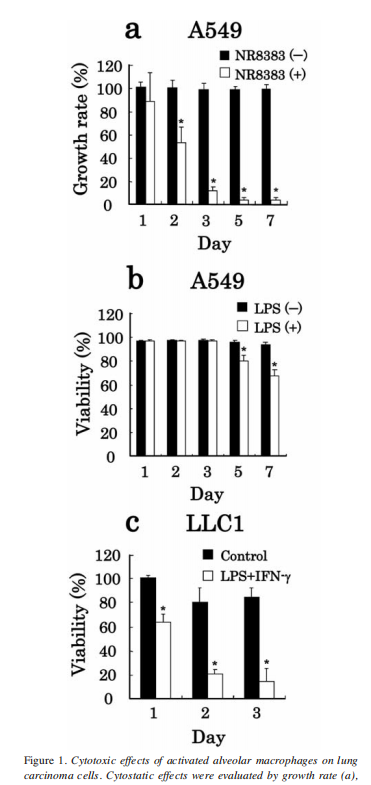
如图1所示,当NR8383细胞与A549细胞以10:1比例(NR8383:A549)在LPS存在下共培养时,NR8383细胞表现出对A549细胞的生长抑制和杀伤作用。培养第2天起即可观察到生长抑制作用,至第7天A549细胞生长速率降至约4%(图1a);培养第5天起检测到杀伤效应,第7天A549细胞存活率降至67%(图1b)。上述效应在与NR8383细胞共培养时才会出现。AMJ2-C11细胞与LLC1细胞以5:1比例(AMJ2-C11:LLC1)共培养时,仅在LPS和IFN-γ共同存在条件下才表现出对LLC1细胞的杀伤作用,第3天LLC1细胞存活率即降至约14%。
这些结果表明,活化的肺泡巨噬细胞对肺癌细胞具有细胞毒性作用。
LPS激活巨噬细胞,增加了巨噬细胞与肺肿瘤细胞的接触
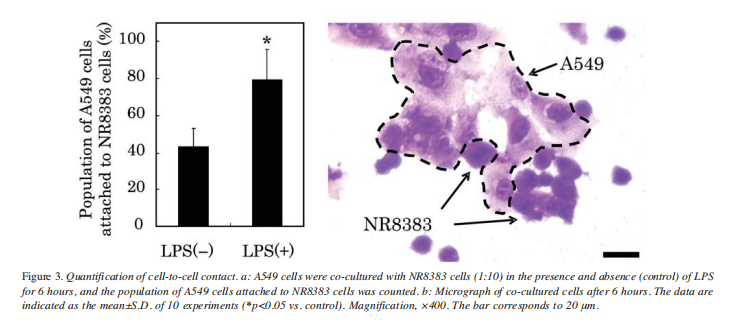
如图1所示,肺癌细胞与肺泡巨噬细胞在LPS存在条件下共培养可导致肿瘤细胞死亡,而LPS本身并不能直接诱导肺癌细胞死亡(图1a)。为观察LPS激活的NR8383细胞对A549细胞的影响,我们分别进行了单独培养(A549细胞:图2a;NR8383细胞:图2b)以及LPS存在/不存在条件下的共培养(无LPS:图2c;含LPS:图2d)。结果显示,当LPS存在时,NR8383细胞与A549细胞共培养时能够迁移并粘附到A549细胞上,而在无LPS条件下则不能。这种粘附现象被量化分析。在A549细胞与NR8383细胞的粘附数量对比中,结果显示LPS能在6小时内使NR8383细胞对A549细胞的粘附率提高近两倍(图3)。
图2.
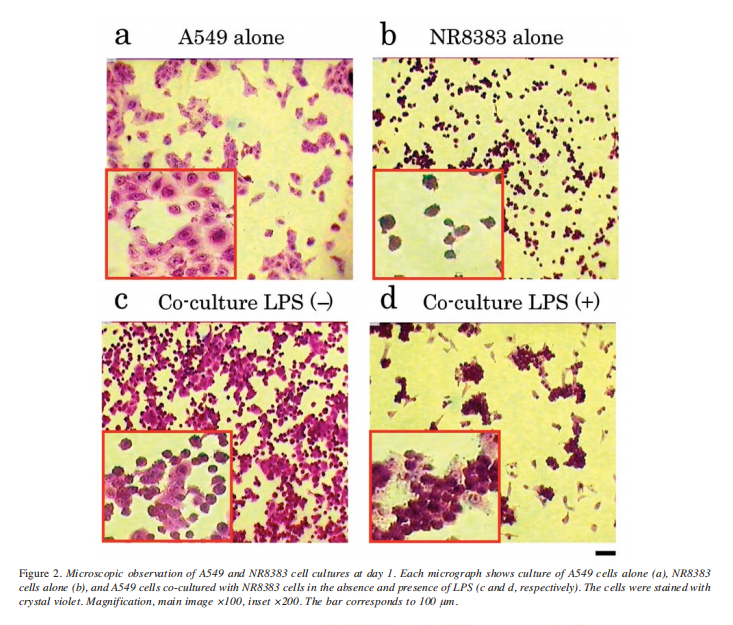
图3.
细胞间接触对细胞毒性效应的影响
为评估NR8383细胞与A549细胞直接接触对生长抑制的影响,本研究采用细胞培养插片系统,在LPS存在(实验组)与不存在(对照组)条件下将两种细胞分隔培养,并测定A549细胞生长速率。
图4.细胞接触对细胞毒性效应的影响
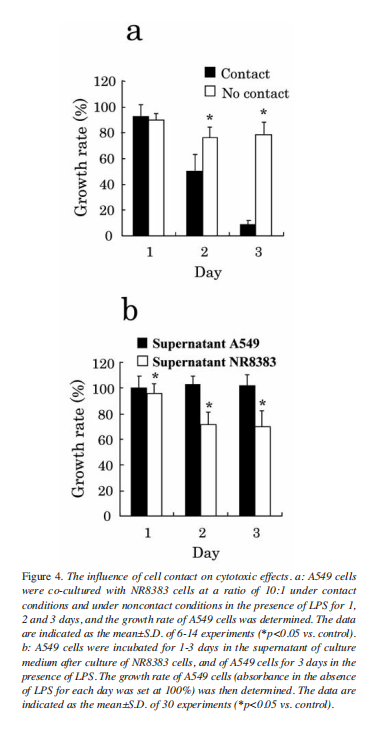
通过与LPS激活的NR8383细胞直接共培养组对比发现:在非接触培养条件下,A549细胞生长速率仅降至78%;而直接共培养组在第3天即显著下降至约8%(图4a)。随后在无插片系统的共培养条件下检测培养上清液的细胞毒性效应(图4b)。LPS激活的NR8383细胞培养3天后的条件培养基上清液,仅能使A549细胞生长速率在培养2-3天后降至70%,该效果与非接触培养组相当(参见图4a)。与之形成鲜明对比的是,A549细胞在自身LPS处理3天后的培养上清液中生长速率未发生改变。
这些结果表明,肺泡巨噬细胞与肿瘤细胞的接触对抑制肺肿瘤细胞生长至关重要。
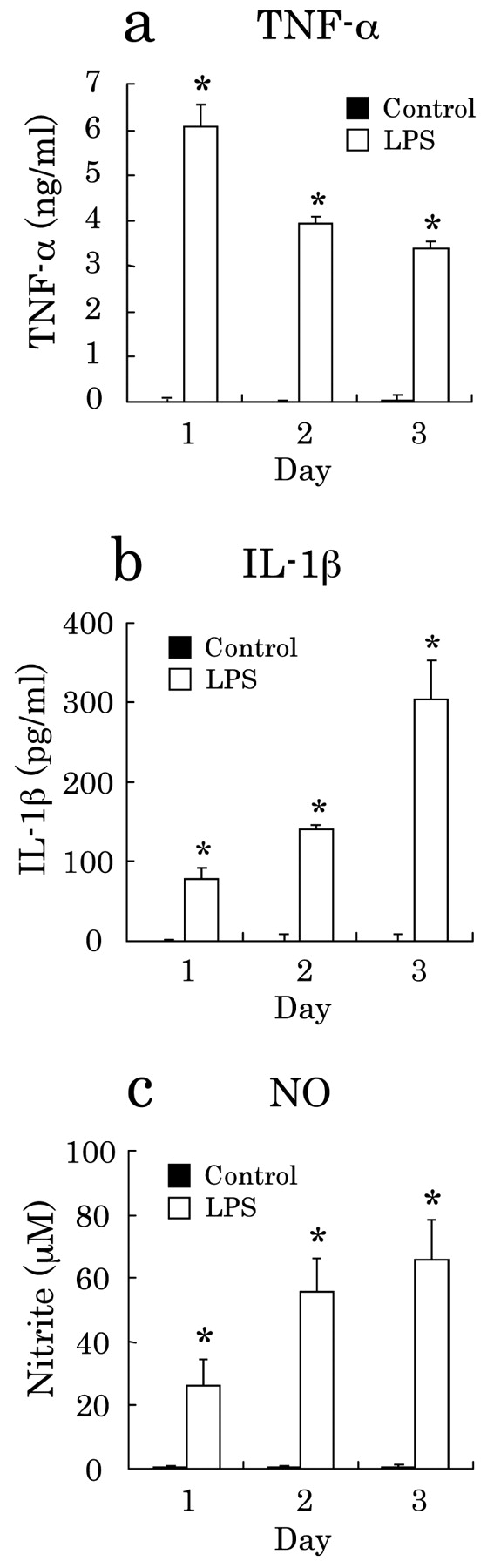
接下来,我们检测了LPS激活的NR8383细胞产生的体液因子TNF-α、IL-1β和NO的量(图5)。结果显示,这些因子在LPS刺激后均显著增加。因此,LPS激活的肺泡巨噬细胞对肿瘤细胞的细胞毒性作用,可能是由于这些体液因子中的任意单一因子或其组合所介导的。
论述
尽管激活的M1表型肺泡巨噬细胞能够杀死肺癌细胞,但其抗肿瘤功能尚未完全明确。为了探究肺泡巨噬细胞对肺癌细胞的杀伤和细胞抑制机制,本研究证实了,LPS激活的肺泡巨噬细胞在与肿瘤细胞的接触条件下,能够有效杀死肺癌细胞。这表明,巨噬细胞与肿瘤细胞的结合是导致肿瘤细胞被杀死的关键因素。
在本项研究中,采用LPS诱导M1类型的活化肺泡巨噬细胞。研究结果表明,在LPS存在的情况下,A549细胞与NR8383细胞共培养时表现出高水平的细胞毒性。而在没有LPS的情况下,这种细胞毒性并未出现。在LPS和IFN-γ存在的情况下,LLC1细胞与AMJ2-C11细胞共培养也观察到了类似的细胞毒性效应(图1)。因此,LPS激活的肺泡巨噬细胞显著增强了对肺癌细胞的细胞毒性活性,无论是在异种(LLC1和AMJ2-C11)还是同种(A549和NR8383)组合中。
由于巨噬细胞具有多种功能,它们可以通过促进或抑制肿瘤生长来调节肿瘤的进展。巨噬细胞通过直接接触肿瘤细胞或释放效应分子间接杀伤肿瘤细胞,从而减少肿瘤的生长。显微镜观察显示,LPS激活的NR8383细胞聚集并接触A549细胞(图2和图3)。已有研究表明,巨噬细胞的膜受体能识别肿瘤抗原分子,使巨噬细胞能够与肿瘤细胞紧密结合(18,19)。阻止NR8383细胞与A549细胞之间的直接接触,几乎可以将A549细胞的生长速度恢复到正常水平(图4)。另一方面,LPS激活的巨噬细胞培养基的上清液对肿瘤细胞的生长有一定的抑制作用,但这种效果有限。因此,肺泡巨噬细胞的抗肿瘤作用可能主要归因于细胞间的直接接触。
此外,我们发现LPS刺激的NR8383细胞上清液中存在大量效应分子,如TNF-α、IL-1β和NO。研究表明,TNF-α能够抑制肿瘤细胞的生长,这表明其在癌症治疗中可能具有潜在价值(20)。IL-1在多种免疫和炎症反应中发挥重要作用,也是一种由巨噬细胞产生的抗肿瘤因子(21)。NO是一种低分子量的介质,具有多种功能,与组织损伤、炎症和休克密切相关。大量NO的产生可以诱导肿瘤细胞凋亡(22,23)。此外,NO通过与超氧自由基反应生成过氧亚硝酸盐(24),而过氧亚硝酸盐具有强烈的细胞毒性(25)。进一步研究这些效应分子的作用机制,对于全面理解LPS刺激的肺泡巨噬细胞在细胞间接触条件下对肿瘤细胞的细胞毒性作用至关重要。
结语
综上所述,本研究揭示了LPS激活的肺泡巨噬细胞对肺肿瘤细胞的细胞毒性作用主要通过细胞间结合机制实现。我们观察到LPS激活的肺泡巨噬细胞能够与肺肿瘤细胞紧密结合,并显著抑制其生长,而这种抑制作用在细胞间接触被阻断后几乎消失。此外,尽管LPS激活的巨噬细胞培养上清液中存在如TNF-α、IL-1β和NO等效应分子,这些分子对肿瘤细胞的生长也表现出一定的抑制作用,但其效果远不及细胞间接触机制显著。因此,细胞间结合是肺泡巨噬细胞发挥抗肿瘤作用的主要途径。这一发现不仅为理解肺泡巨噬细胞在肿瘤免疫中的作用机制提供了新的视角,也为开发基于巨噬细胞的肿瘤免疫疗法提供了重要的理论依据。未来的研究将进一步探索细胞间结合的分子机制以及如何通过调节巨噬细胞的激活状态来增强其抗肿瘤能力,以期为肺癌的治疗提供更有效的策略。
免责声明:
以上部分内容来源于外网我们重在信息分享,版权归属原作者或原刊发平台所有,如有侵权、信息有误或其他异议,请联系处理,我们将在24小时内删除或整改。
复合免疫 健康活力





























