
突破传统镇痛局限:LPS在术后镇痛中的创新应用“机制探索与临床前景”!
活化巨噬细胞调节的稳态:LPS的镇痛作用
LPS作为革兰氏阴性菌外膜的关键成分,长期以来因其强效的促炎特性而被视为疼痛恶化的潜在因素。然而,近年研究发现,LPS在特定条件下可能表现出令人意外的镇痛效应,这一现象正逐渐成为疼痛研究领域的新热点。其镇痛作用可能通过以下机制实现:
一、TLR4/MyD88/NF-κB信号通路:LPS通过激活Toll样受体4(TLR4),进而激活MyD88依赖的信号通路,最终导致NF-κB的激活。NF-κB是一种重要的转录因子,能够调节多种炎症因子的表达。通过调节炎症反应,LPS可以减轻术后疼痛。
*PHARMACEUTICAL BIOLOGY, 2018
VOL. 56, NO. 1, 275–286
https://doi.org/10.1080/13880209.2018.1457061
二、调节炎症因子平衡:LPS能够调节促炎因子(如IL-18)和抗炎因子(如IL-18BP)之间的平衡,这种平衡的恢复有助于减轻炎症引起的疼痛。
*生命的化学, 2024, 44(11): 2054-2066
doi: 10.13488/j.smhx.20240210
三、肠-脑轴作用:肠道菌群失调时,LPS通过“微生物-肠-脑轴”影响中枢神经系统,可能与慢性疼痛和术后疼痛持续状态相关。
*ZHEJIANG HEALTH SCIENCE AND
TECHNOLOGY RESEARCH & TRANSLATION PLATFORM
https://www.msttp.com/information/detail?id=1934814014898962432
四、影响神经胶质细胞和巨噬细胞:LPS可能通过影响背根神经节(DRG)中的巨噬细胞活性来发挥镇痛作用。这些细胞在神经炎症和疼痛传导中起重要作用,LPS通过调节这些细胞的活性,有助于减轻术后疼痛。
*ZHEJIANG HEALTH SCIENCE AND
TECHNOLOGY RESEARCH & TRANSLATION PLATFORM
https://www.msttp.com/information/detail?id=1934814014898962432
五、内源性阿片系统激活:LPS 刺激免疫细胞释放 β-内啡肽,作用于外周/中枢 μ-阿片受体,抑制疼痛传导。
*Chem.Pharm.Bull.40(4)1001-1003(1992)
六、抗氧化酶诱导(HO-1):
LPS上调血红素氧合酶-1(HO-1),清除氧自由基,减轻氧化应激性神经损伤。
*Eur J Pharmacol. 2020
*European Journal of Pharmacology(《欧洲药理学杂志》)
*Journal of Neuroinflammation(《神经炎症杂志》)
*Molecular Neurobiology(《分子神经生物学》)
*Published in final edited form as:
*Curr Opin Nephrol Hypertens. 2014 January ; 23(1): 17–24.
doi:10.1097/01.mnh.0000437613.88158.d3
术后疼痛是手术后常见的问题,严重影响患者的康复进程和生活质量。传统的镇痛方法虽然在一定程度上能够缓解疼痛,但往往伴随着诸多副作用,如成瘾性、胃肠道不适等。近年来,研究发现LPS在术后镇痛方面具有潜在的应用价值。LPS作为革兰氏阴性菌细胞壁的主要成分,能够激活机体的免疫反应,进而调节炎症反应和神经信号传导,从而发挥镇痛作用。其镇痛机制涉及多个信号通路和分子靶点,包括TLR4/MyD88/NF-κB信号通路、TLR4/Nrf2/HO-1轴以及炎症因子平衡的调节等。这些机制不仅能够减轻术后炎症引起的疼痛,还可能通过抗氧化作用保护神经细胞免受氧化应激损伤。然而,LPS的镇痛效果及其机制尚未完全明确,仍需进一步深入研究。本综述旨在探讨LPS在术后镇痛中的作用机制,分析其潜在的临床应用前景,并指出当前研究中存在的问题和未来的研究方向,以期为术后疼痛管理提供新的思路和策略。
活化巨噬细胞调节的稳态:LPS的镇痛作用
LPS(一种从小麦粉水提取物中获得的脂多糖)对疼痛反应的影响通过小鼠醋酸诱导扭体实验进行了研究。LPS在10 ng至10 μg/只小鼠静脉注射的剂量范围内呈剂量依赖性抑制扭体反应。此效应在LPS注射后1.5至3小时达到最大,甚至在8小时后仍可检测到。LPS的镇痛作用可被静脉注射纳洛酮所抑制,并且在注射LPS后的血清和脑组织中检测到了β-内啡肽。初步临床试验,其中LPS通过经皮给药来缓解疱疹患者的疼痛。结果显示此给药方式缓解了疼痛。LPS可能是目前已知的最佳镇痛药物,因为它诱导了内源性的镇痛介质——β-内啡肽。
引言
疼痛被认为是人体保护自身免受进一步伤害的重要警告信号。然而,慢性疼痛似乎是最严重的临床问题之一。长期以来,麻醉性镇痛药一直用于治疗剧烈疼痛,但这些治疗方法通常伴随着一些严重的副作用,如麻醉剂成瘾或呼吸抑制。因此,迫切需要开发一种没有此类副作用的新型镇痛药物。
诸如阿片肽和Kyotorphin等内源性镇痛物质已被鉴定出来。 最近,有报道称炎症介质如肿瘤坏死因子(TNF)、白细胞介素1(IL-1)和干扰素(IFN)具有镇痛效果。活化巨噬细胞的诱导剂,如大肠杆菌(E. coli)LPS和胞壁酰二肽(MDP),也被报道具有镇痛作用。 然而,这些物质由于其严重的副作用或不适当的给药途径而不能临床使用。为了寻找一种可临床适用的新药,我们最近发现了LPS,这是一种从小麦粉水提取物中纯化得到的脂多糖。
LPS是一种鲎阳性物质,能够将巨噬细胞激活至内源性肿瘤坏死因子(TNF)产生的启动阶段。它与大肠杆菌脂多糖(LPS)及其他来源的LPS存在多项差异,尤其在分子量和磷含量方面。LPS的分子量(5千道尔顿)低于大肠杆菌LPS(30千道尔顿),且可通过口服或经皮途径给药应用。
本研究探讨了LPS在小鼠体内的镇痛效应,发现该效应可通过静脉注射纳洛酮被抑制。当静脉注射LPS时,检测到β-内啡肽释放。我们同时报告了将LPS经皮给药作为镇痛疗法应用于疱疹患者的初步研究结果。
结果
LPS对醋酸诱导扭体的抑制作用
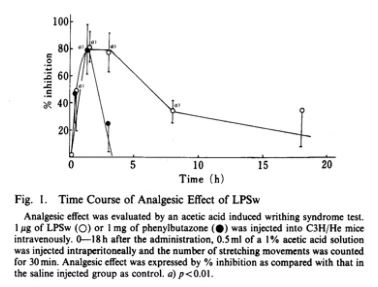
首先检测了LPS对醋酸诱导扭体综合征的影响。图1显示了该镇痛作用在小鼠体内的时间进程。将1µg的LPS静脉注射给C3H/He小鼠,在给药后0、0.5、1.5、3、8 和 18 小时,向小鼠腹腔内注射0.5 ml 1% 醋酸溶液,并在30分钟内计数伸展运动的次数。注射生理盐水的小鼠作为对照组。镇痛作用以相对于盐水组的抑制百分比表示。LPS对伸展运动表现出显著的抑制作用。该效应在 LPS注射后1.5至3小时达到峰值,随后逐渐减弱,但即使在8小时后,仍可检测到明显效果。研究发现LPS的镇痛作用持续时间长于阳性对照药物 (phenylbutazone)。
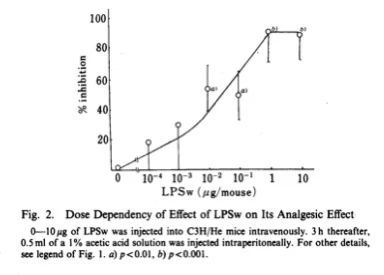
LPS镇痛作用的剂量依赖性如图2所示。10ng剂量的 LPS即对伸展运动产生显著抑制效果,且该抑制作用在每只小鼠1μg剂量时达到最大效果。
内源性阿片肽对LPS镇痛作用的影响
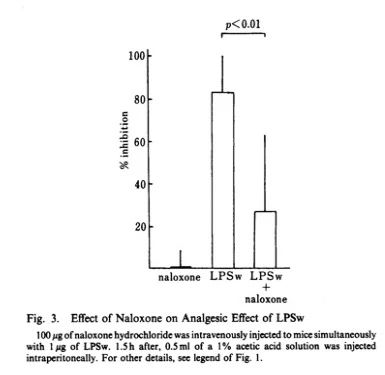
通过注射阿片受体拮抗剂纳洛酮进行作用验证。向小鼠同时静脉注射100微克盐酸纳洛酮与1微克LPS。如图3所示,盐酸纳洛酮抑制了约67%的LPS镇痛效果。
注射LPS后β-内啡肽的检测
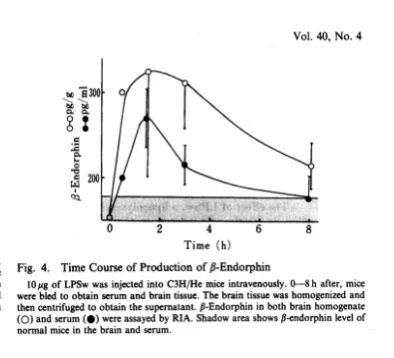
我们随后检测了LPS诱导产生的内源性阿片肽——β-内啡肽,静脉注射LPS后其产生的时间进程如图4所示。血清和脑组织中的β-内啡肽水平在注射后0.5至3小时达到峰值,随后逐渐下降,这与LPS镇痛作用的时间进程相一致。
LPS在疱疹患者中的临床试验
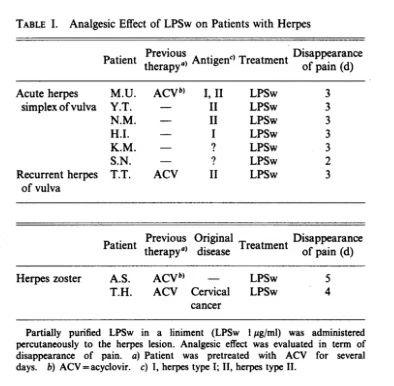
表I显示了LPS的镇痛效果。如先前报道所述,该物质可通过透皮给药方式施用。初步试验中,将含LPS(1μg/ml)的搽剂施用于疱疹患者病灶处后,在急性疱疹、复发性疱疹和带状疱疹(表 I)患者中,在给药后2至5天疼痛消失。
讨论
LPS的镇痛作用被明确观察到,并且其最低有效剂量很小(10 ng/小鼠)(见图 1, 2)。此效应通过静脉注射途径获得,但我们先前报道过 LPS经皮给药同样有效,并且如下文所述,即使在疱疹患者的疼痛治疗中,该方法也已被证实有效。
LPS的镇痛效果比阳性对照药物苯丁唑酮更持久(图1)。我们曾报道发现,LPS能够根据剂量的不同,诱导出启动状态和触发状态,通过激活巨噬细胞促进内源性TNF的产生。启动状态是指TNF前体开始生成,而触发状态则是指成熟的TNF开始生成。LPS对镇痛效果的时间进程和剂量依赖性的这些特征与LPS诱导的启动状态相似,这表明,LPS诱导的启动状态,即轻度活化产生TNF前体的巨噬细胞,可能是LPS发挥镇痛作用的关键。这可以很好地解释为什么具有启动作用但不具备触发作用的胞壁二肽(MDP)能抑制醋酸引起的扭体反应这一事实。
我们的研究结果表明,LPS的镇痛作用可被纳洛酮抑制,并且注射LPS可诱导 β-内啡肽水平上升,这提示镇痛作用可能是由阿片类物质介导的,特别是 β-内啡肽。此外,根据 β-内啡肽产生的时间进程与LPS镇痛作用时间进程相关联这一事实,我们能够提出,这种镇痛作用的机制可能归因于LPS激活巨噬细胞后,同时产生β-内啡肽和TNF前体所致。
据报道,TNF、IL-1、IFN 和其他细胞因子也具有镇痛作用,我们之前的研究表明,这些因子能够激活巨噬细胞,使其产生内源性TNF前体。因此,它们最终可能通过同时产生 β-内啡肽等内源性阿片肽来发挥镇痛作用。基于这一概念,我们可以推测,作为一种天然药物,LPS可能比外源性阿片类药物或传统镇痛药更有效,因为它能够持续诱导内源性的镇痛介质——β-内啡肽。
初步临床试验显示,通过经皮给药LPS至疱疹病灶,可以有效缓解疱疹住院患者的疼痛。如表I所示,即使对于因长期后遗症而感到疼痛的患者中,其镇痛效果也非常显著。研究发现,LPS能够通过黏膜吸收,并诱导激活巨噬细胞。因此,因此,这表明经皮给药的LPS可能通过疱疹病灶被吸收,从而发挥镇痛作用。
据报道,IFN-a和MDP,这两种物质都是引发TNF产生的启动剂,已被证实对吗啡成瘾有影响。这表明LPS也可能影响吗啡成瘾,因为它同样能诱导TNF产生的启动状态。LPS无论来源如何,通常具有类似的活性。LPS因其分子量小而允许经皮给药,因此更为实用。
参考文献:
1.J. Hughes, T. W. Smith, H. W. Kosterlitz, L. A. Fothergill, B. A. Morgan and H. R. Morris, Nature (London), 258, 577 (1975).
2.H. Takagi, H. Shiomi, H. Ueda and H. Amano, Eur. J. Pharmacol., 55, 109 (1979).
3.B. P. Candace and H. S. Solomon, Science, 179, 1011 (1973).
4.L. A. Matsuda, S. J. Lolait, M. J. Brownstein, A. C. Young, and T. I. Bonner, Nature (London), 346, 561 (1990).
5.H. Nakamura, K. Nakanishi, A. Kita and T. Kadokowa, Eur. J. Pharmacol., 149, 49 (1988).
6.T. Ogawa and S. Kotani, Immunopharmacology and Therapy, 6, 39 (1988).
7.T. Ogawa and S. Kotani, Infect. Immun., 55, 494 (1987).
8.T. Nishizawa, H. Inagawa, H. Oshima, T. Okutomi, D. Tsukumo, M. Iguchi, G-I. Soma and D. Mizuno, Chem. Pharm. Bull., 40, 479 (1992).
9.N. K. Tanabe, Y. Tanabe, A. Morikawa, D. Mizuno and G-I. Soma, Chem. Pharm. Bull., 39, 417 (1991).
10.M. Krieger, C. Perez, K. Defay, I. Albert and S. D. Lu, Cell, 53, 45 (1988).
11.T. Okutomi, H. Inagawa, T. Nishizawa, H. Oshima, G-I. Soma and D. Mizuno, J. Biol. Res. Modif., 9, 564 (1990).
12.H. Inagawa, H. Oshima, G-I. Soma and D. Mizuno, J. Biol. Res. Modif., 7, 596 (1988).
13.M. Satoh, H. Inagawa, Y. Shimada, G-I. Soma, H. Oshima and D. Mizuno, J. Biol. Res. Modif., 6, 512 (1987).
14.M. Satoh, Y. Shimada, H. Inagawa, H. Minagawa, T. Kajikawa, H. Oshima, S. Abe, M. Yamazaki and D. Mizuno, Jpn. J. Cancer Res. (Gann), 77, 342 (1986).
15.P. M. Dougherty and N. Dafny, J. Neurosci. Res., 19, 140 (1988).
16. P. M. Dougherty, K. J. Krajewsky, N. R. Pellis and N. Dafny, Neuropharmacology, 26, 1595 (1987).
免责声明:
以上部分内容来源于外网我们重在信息分享,版权归属原作者或原刊发平台所有,如有侵权、信息有误或其他异议,请联系处理,我们将在24小时内删除或整改。
复合免疫 健康活力





























