
口服来自成团泛菌1型的免疫增强剂(IP-PA1)提高B16黑色素瘤接种模型小鼠的存活率 ·
LPS可以降低癌症化疗剂的副作用,提高抗癌剂的效果。
注:
本文为中、日、英三种语言,下方附有中文翻译,供您查阅!
LPSは抗がん剤の効果をあげるLPSは、癌の化学療法剤の副作用を低減し、抗がん剤の効果をあげることが報告されています。
癌になるような異常な細胞は、1日に5000個レベルで出来ていると言われます。けれども異常な細胞は、ほとんどの場合、免疫細胞が監視し処理してくれているのです。癌の発症が加齢やストレスで増加するのは、免疫機能の衰えにも関係します。一方癌になったとき、癌を治療するための化学療法剤は、癌細胞と同時に正常な細胞にもダメージを与え、このため免疫細胞も衰えます。化学療法剤を使うケースでは、特に免疫を落とさないことが重要です。動物実験では、癌を移植したマウスに化学療法剤を与えただけよりも、LPSとともに化学療法剤を与えたほうが延命効果が高いことが示されています(*1)。
(*1)Oral administration of immunopotentiator from Pantoea agglomerans (IP-PA1) improves the survival of B16 melanoma-inoculated model mice, Experimental Animal 60 (2): 101-109 (2011)
中文翻译:
据报告显示,LPS可以降低癌症化疗剂的副作用,提高抗癌剂的效果。
LPS提高抗癌剂的有效性
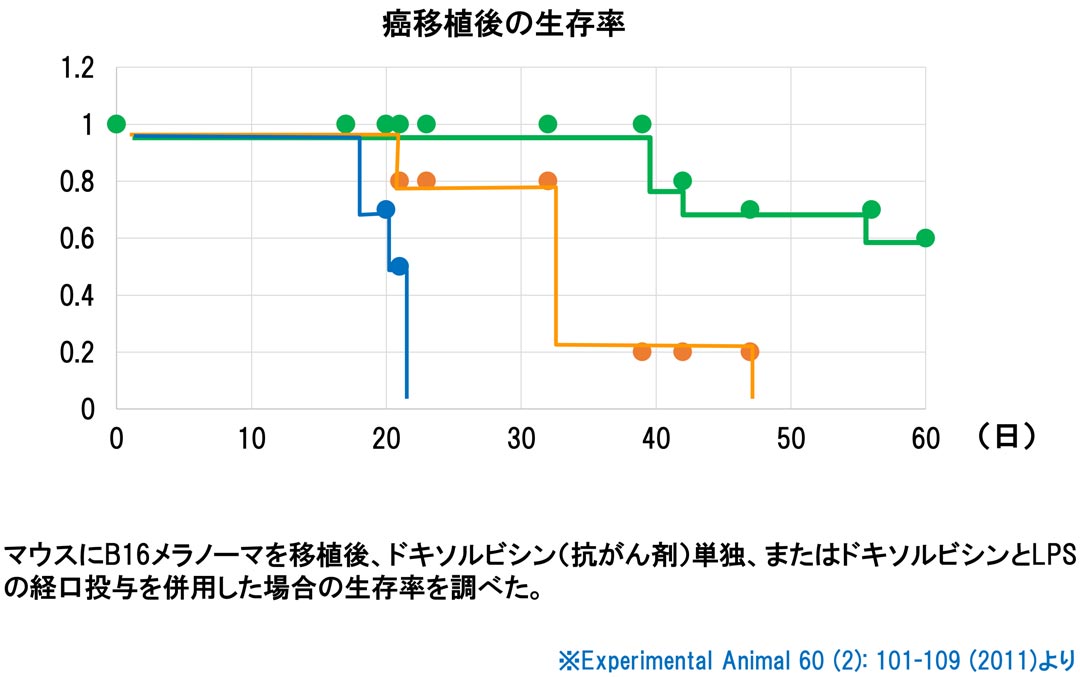
据说每天大约会形成5000个可能癌变的异常细胞。然而,在大多数情况下,异常细胞是由免疫细胞监测和处理的。癌症发病率随着年龄和压力的增加而增加,这也与免疫功能减弱有关。另一方面,当癌症发生时,用于治疗癌症的化疗药物会损害正常细胞和癌细胞,结果免疫细胞也会减弱。使用化疗药物时,不要削弱免疫系统尤为重要。动物实验表明,对于癌症移植小鼠来说,与单独给予化疗药物相比,同时给予化疗药物和 LPS 更能有效延长生存期(*1)。
参考文献:
(*1)Oral administration of immunopotentiator from Pantoea agglomerans (IP-PA1) improves the survival of B16 melanoma-inoculated model mice, Experimental Animal 60 (2): 101-109 (2011)
以下内容为文献详情内容
中文翻译:
文件内容是一篇关于成团泛菌(Pantoea agglomerans)1型(IP-PA1)中提取的免疫增强剂在黑色素瘤治疗中作为辅助药物的研究论文。以下是翻译成中文的内容:
口服来自成团泛菌1型的免疫增强剂(IP-PA1)提高B16黑色素瘤接种模型小鼠的存活率
摘要
●为了研究成团泛菌属1型(IP-PA1)免疫增强剂在黑色素瘤治疗中的辅助作用,我们分析了IP-PA1对黑色素瘤接种模型小鼠的免疫作用。
通过ELISA评估,在未受感染的BALB/cCrSIc小鼠中,口服IP-PA1在给药后2小时增加了肿瘤坏死因子(TNF)-a的血清水平,在给药后12小时增加了干扰素(IFN)-Y和IL-12的血清水平。
IP-PA1不影响通过3-[4,5-二甲基噻唑-2-基]-2,5-二苯基四唑溴化物(MTT)试验直接测定的黑色素瘤细胞的增殖。
通过ELISA评估,与阿霉素单独治疗相比,IP-PA1与阿霉素联合治疗9天使荷黑色素瘤C57BL/6NCrSlc小鼠的血清IFN-y和IL-12水平分别增加了71.0%和15.3%。
通过流式细胞术分析,它还增加了脾脏中自然杀伤(NK)细胞的比例以及CD4+与CD8+ T细胞的比例,从6.1±0.3%增加到7.4±0.5%,从1.25±0.03增加到1.38±0.04。
黑色素瘤携带的多柔比星治疗小鼠的平均存活期从31.4±7.1天延长到35.3±8.4天、51.1±5.4天和45.0±8.4天,这是通过每天0.1、0.5和1 mg/kg剂量的IP-PA1联合治疗实现的。
总之,本研究的结果表明IP-PA1作为黑色素瘤治疗中的辅助药物的有效性。
● 关键词:化疗、免疫调节剂、免疫抑制、IP-PA1、黑色素瘤
介绍
恶性黑色素瘤(MM)是皮肤癌中最侵袭性的形式,其发病率的增长速度快于任何其他类型的癌症[6, 19, 22, 26]。原发性黑色素瘤的主要治疗方法是广泛局部切除;然而,即使是接受外科切除的患者也面临着高风险的淋巴结和远处转移[11, 37]。此外,MM通常对常规疗法如全身化疗和放疗具有抗性[5];因此,MM的预后较差[10]。
癌症患者的预后因素之一是抗肿瘤免疫功能,即对抗癌症发生和进展的防御机制[29, 43]。据报道,肿瘤浸润性淋巴细胞的溶瘤功能与黑色素瘤患者的临床反应有关[2]。大多数肿瘤细胞可以通过产生免疫抑制性IL-10等各种机制潜在地抑制宿主的免疫[9]。此外,常规化疗[44]、放疗[21]和手术[4, 24]经常抑制宿主的免疫;因此,癌症患者通常在免疫学上受到抑制。
成团泛菌属1型(IP-PA1)免疫增强剂是一种低分子量(5 kDa)的泛菌糖脂质(LPS),来源于常见于各种粮食作物(如谷物、水果和蔬菜)中的共生革兰氏阴性细菌的细胞壁[17, 18, 20, 27]。IP-PA1具有增强免疫功能,如在小鼠中保护免受细菌和寄生虫感染[8, 20, 32],以及在鸡中从应激诱导的免疫抑制中恢复[14]。因此,IP-PA1被认为是一种潜在的可食用免疫调节剂。
为了研究IP-PA1作为黑色素瘤治疗辅助药物的实用性,我们评估了IP-PA1口服给药在黑色素瘤接种小鼠模型中的效果。我们最初评估了IP-PA1对黑色素瘤细胞增殖的影响以及对多柔比星体外细胞毒性的影响。然后,我们评估了IP-PA1与多柔比星联合治疗在黑色素瘤接种模型小鼠中的免疫学效果。最后,我们检查了接受IP-PA1和多柔比星治疗的黑色素瘤携带小鼠60天的生存情况。
结果
1、IP-PA1口服给药后在原始BALB/c小鼠中诱导的细胞因子产生
从口服给予IP-PA1后的原始BALB/cCrSlc小鼠中收集血样。使用ELISA确定TNF-α、IFN-γ和IL-12的血清水平。TNF-α的血清水平在给予IP-PA1后2小时增加(图1A),在给予后12小时仍然如此(图1B)。IL-12和IFN-γ的血清水平仅在给予IP-PA1后12小时增加(图1C和1D)。
图1
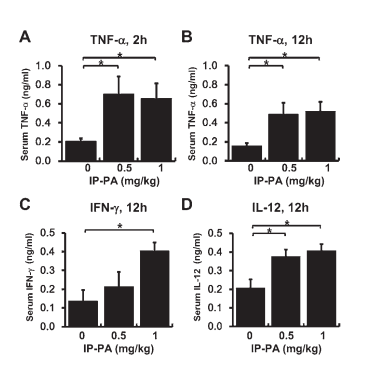
口服给予IP-PA1后原始BALB/cCrSlc小鼠中TNF-α、IFN-γ和IL-12的血清水平。
2、对B16黑色素瘤细胞增殖的影响
用0-100 μg/ml IP-PA1在PBS中预处理的B16细胞,1小时后用0-1 μM的多柔比星进行体外处理。使用MTT试验在用多柔比星处理72小时后确定细胞增殖。与未用多柔比星处理的细胞相比,IP-PA1并未影响B16细胞的增殖(表1)。多柔比星以剂量依赖性方式抑制B16细胞的增殖;然而,IP-PA1并未影响多柔比星对B16细胞的抑制效果(表1)。
细胞毒性的影响
IP-PA1预处理对体外多柔比星对B16黑色素瘤细胞毒性的影响
表1
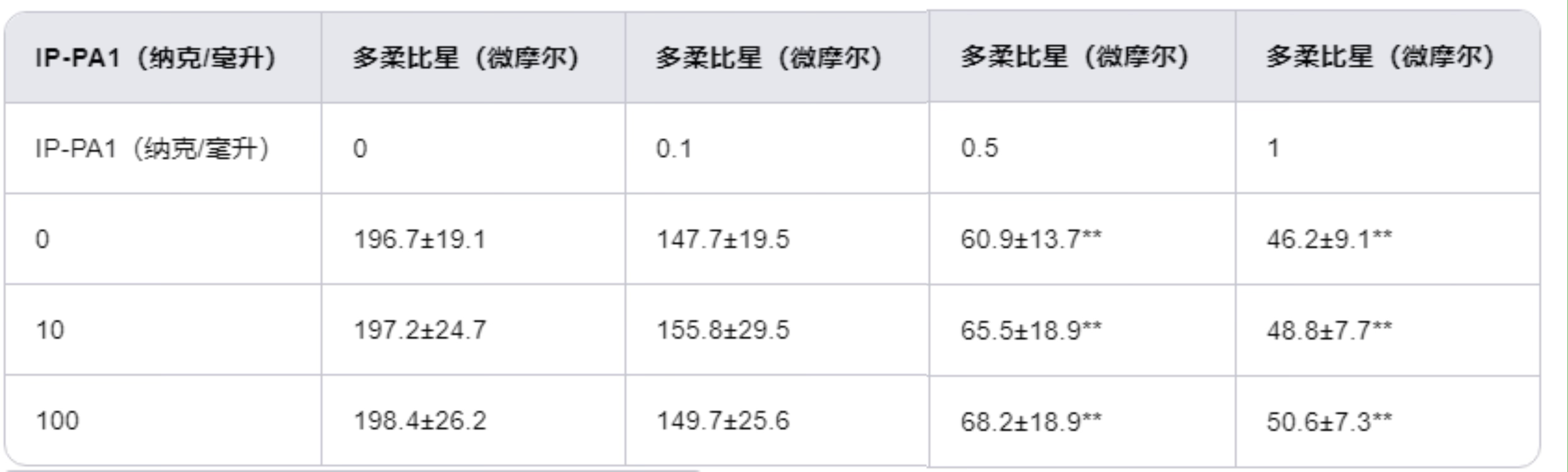
结果表示为3个独立实验的平均值±标准误差(SEM)。
**与未用多柔比星处理的对照细胞相比,P<0.01。
3、黑色素瘤携带小鼠的血清细胞因子水平
对C57BL/6NCrSlc黑色素瘤携带小鼠进行了8天的多柔比星和IP-PA1治疗。
在最后一次给药后24小时收集血样,并使用ELISA确定TNF-α、IFN-γ和IL-12的血清水平。
血清中的TNF-α和IL-12的水平没有变化,而在携带黑色素瘤的小鼠中,与原始小鼠相比,IFN-γ的水平略有下降,但这种下降并不显著(数据未显示)。
在携带黑色素瘤的小鼠中,IP-PA1和多柔比星的联合治疗相比于无药物处理或仅多柔比星治疗,增加了IFN-γ的血清水平(图2A)。
在携带黑色素瘤的小鼠中,IP-PA1和多柔比星的联合治疗相比于仅多柔比星治疗,也增加了IFN-γ的血清水平(图2B)。在各组之间,TNF-α的血清水平没有观察到差异(数据未显示)。
图2
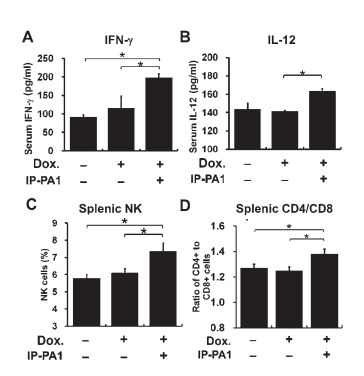
接受IP-PA1和多柔比星治疗的黑色素瘤携带C57BL/6NCrSlc小鼠的IFN-γ和IL-12血清水平,以及脾脏中NK细胞、CD4+ T细胞和CD8+ T细胞的比例。
接种了B16黑色素瘤细胞的C57BL/6NCrSlc小鼠接受了8天的IP-PA1和多柔比星治疗。在最后一次给药后24小时收集血样并分离脾脏。
通过ELISA测定IFN-γ(A)和IL-12(B)的血清水平。使用流式细胞术测定NK细胞(C)的比例和CD4+与CD8+ T细胞的比例(D)。
结果以3或4只小鼠的平均值±标准误差(SEM)表示。组间显著差异用*表示:P<0.05。
脾脏中免疫细胞的比例
C57BL/6NCrSlc黑色素瘤携带小鼠接受了8天的多柔比星和IP-PA1治疗。在最后一次治疗后24小时分离脾脏,并使用流式细胞术测定NK细胞、CD4+ T细胞和CD8+ T细胞的比例。
与原始小鼠相比,黑色素瘤携带小鼠的NK细胞数量和CD4+与CD8+ T细胞的比例略有下降,但这些差异在统计学上并不显著(数据未显示)。
在黑色素瘤携带小鼠中,与未接受药物或仅接受多柔比星治疗的小鼠相比,接受IP-PA1和多柔比星联合治疗的小鼠的NK细胞数量和CD4+与CD8+ T细胞的比例显著增加(图2C和2D)。
黑色素瘤携带小鼠生存率的提高
接种B16黑色素瘤细胞的C57BL/6NCrSlc小鼠在未接受药物治疗的情况下,肿瘤接种后19.3±1.2天死亡。
在接种后10天,超过一半的小鼠出现了抑郁行为、严重消瘦、脱水和腹部膨胀。每只解剖小鼠的腹腔内充满了黑色素肿瘤簇,肠道呈透明状。在肺、肝、脾和肾的表面经常观察到分散的肿瘤细胞。
由于体重迅速下降,8只未接受药物治疗的对照小鼠中有2只在自然死亡前被安乐死。腹腔内给予多柔比星将黑色素瘤携带小鼠的生存期延长至31.4±7.1天(图3)。
与仅接受多柔比星治疗的小鼠相比,0.5 mg/kg IP-PA1与多柔比星的联合治疗显著延长了生存期,这在对数秩检验下具有统计学意义(P=0.02;图3A)。
接受0.1、0.5或1 mg/kg/天IP-PA1与多柔比星治疗的小鼠的平均生存期分别为35.3±8.4、51.1±5.4和45.0±8.4天(图3B)。
所有未接受药物或仅接受多柔比星治疗的小鼠在第60天之前死亡;然而,分别有25.0%、51.4%和45.1%接受0.1、0.5或1 mg/kg/天IP-PA1与多柔比星治疗的小鼠在第60天仍然存活。
0.5 mg/kg/天剂量的IP-PA1与多柔比星的联合治疗比其他剂量更有效。在大多数存活小鼠的腹腔内未观察到黑色素肿瘤簇。
图3
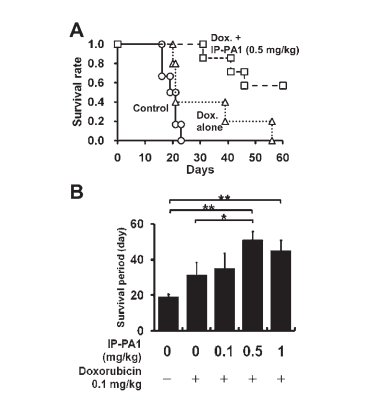
接种了B16黑色素瘤细胞的C57BL/6NCrSlc小鼠接受了60天的IP-PA1和多柔比星治疗,并对它们的生存情况进行了观察。
结果以Kaplan-Meier生存曲线(A)和生存期(B)的形式展示。
在(B)中,结果以5-8只小鼠的平均值±标准误差(SEM)表示,组间显著差异用*表示:P<0.05,**表示:P<0.01。
论述
传统细菌来源的LPS通过Toll样受体(TLR)-4激活巨噬细胞和树突状细胞(DCs),TLR-4是LPS的特异性受体[3]。IP-PA1也在体外通过激活TLR-4的主要靶点核因子(NF)-κB,部分刺激巨噬细胞[15]。对原始BALB/cCrSlc小鼠口服给予IP-PA1在2小时(TNF-α)或12小时(IFN-γ和IL-12)内增加了TNF-α(图1A和1B)、IFN-γ(图1C)和IL-12(图1D)的血清水平,这可能是由于IP-PA1激活了肠道黏膜组织中的巨噬细胞和DCs。
IP-PA1增加了黑色素瘤携带C57BL/6NCrSlc小鼠的IFN-γ(图2A)和IL-12(图2B)的血清水平,表明IP-PA1即使在携带肿瘤、接受化疗、免疫抑制的宿主中也能增强宿主的免疫力。
IP-PA1增加了脾脏NK细胞的比例(图2C)并改善了脾脏CD4+与CD8+ T细胞的比例,这是化疗诱导的淋巴细胞耗竭的典型标志(图2D)[25]。这些结果表明IP-PA1诱导了该模型免疫系统的恢复。
由于IP-PA1并未直接影响B16细胞的增殖(表1),我们推测IP-PA1治疗在黑色素瘤携带小鼠中显著提高生存率(图3)主要是由于增强了抗肿瘤免疫力(图4)。这表明IP-PA1的应用范围扩展到了其他与肿瘤相关的疾病以及黑色素瘤。
各种免疫细胞参与了抗肿瘤免疫。巨噬细胞直接识别并杀死肿瘤细胞[33,39];它们吞噬凋亡的肿瘤细胞[30],并处理和呈现肿瘤特异性抗原给CD8+细胞毒性T淋巴细胞(CTL)这些细胞直接裂解抗原特异性肿瘤细胞[36]。自然杀伤(NK)细胞在监视和排除发展中的癌细胞中发挥关键作用[12, 13]。活化的巨噬细胞产生的几种细胞因子通过影响其他免疫细胞来增强抗肿瘤免疫力。TNF-α通过增加IL-2受体的表达[31]部分增强T细胞反应,并介导单核细胞的分化[41]。IFN-γ增强细胞毒性T淋巴细胞(CTL)[28]和NK细胞[1]的抗肿瘤功能。IL-12通过增加巨噬细胞的数量[38]部分支持CTL的有效抗肿瘤功能。BALB/c被认为是偏向Th2的品系,这意味着它是低水平的Th1细胞因子如IFN-γ和IL-12的产生者[23]。在本研究中,IP-PA1在BALB/cCrSlc小鼠中诱导了IFN-γ和IL-12(图1),表明IP-PA1是Th1型反应的强效诱导剂。
宿主免疫力可能支持化疗的结果。例如,巨噬细胞对凋亡肿瘤细胞的清除不足会阻止有效的化疗,因为凋亡的肿瘤细胞是抗肿瘤免疫力的强烈抑制剂[40]。然而,包括多柔比星在内的化疗药物经常抑制宿主免疫细胞[8]。IP-PA1对多柔比星诱导的免疫抑制显示出强大的保护效果,例如抑制巨噬细胞生长[15],这可能是本研究中观察到的黑色素瘤接种模型小鼠生存期延长的原因之一。
尽管来自病原性革兰氏阴性菌如大肠杆菌的LPS在体外具有强大的免疫增强效果,但由于大量进入血液时会引起严重的败血性休克,它们的临床应用受到限制[7]。然而,与全身注射相比,当在安全性测试中口服给予时,没有报告LPS的毒性:在大鼠中口服给予1000 mg/kg IP-PA1 28天没有产生毒性效果[18, 35]。此外,从作物中发现的共生革兰氏阴性菌衍生的IP-PA1被认为是安全的,因为它已经被人类和动物长期摄入[20]。因此,IP-PA1被期望作为一种免疫调节剂,这是我们评估口服给予IP-PA1在黑色素瘤治疗中的免疫学效果和有用性的主要原因之一。
口服给予的IP-PA1已经显示出对胃溃疡和寄生虫感染的预防效果;然而,来自大肠杆菌或其他常规细菌的LPS显示出非常小或可以忽略的效果[27, 32]。由于IP-PA1具有短的O链,它在溶液中形成比大肠杆菌LPS更小的胶束,这有利于渗透粘膜组织和刺激粘膜巨噬细胞,这是口服给予IP-PA1显示出效果的合理原因。关于口服给予IP-PA1对癌症患者的安全性,还没有足够的证据;然而,在本研究中显示免疫学效果的IP-PA1剂量远低于毒性测试中的无观察效应水平。因此,IP-PA1可能作为黑色素瘤治疗中的一种可食用的辅助药物有用。
图4
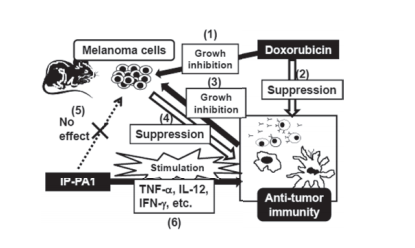
一个关于IP-PA1对携带黑色素瘤小鼠生存率正面影响的可想象机制模型。
多柔比星抑制了B16黑色素瘤细胞的肿瘤性增殖(1);然而,它可能抑制免疫细胞的功能(2)。免疫细胞抑制黑色素瘤细胞的发生和进展(3),而肿瘤细胞抑制免疫细胞的正常活动(4)。IP-PA1并不直接影响B16黑色素瘤细胞的增殖(5)。
因此,认为IP-PA1通过激活的巨噬细胞和树突状细胞(DCs)产生如IFN-γ这类炎症细胞因子,部分地调节了被抑制的抗肿瘤免疫,IFN-γ是激活的肿瘤溶解性NK细胞的最强激活因子之一(6),从而改善了携带黑色素瘤小鼠的生存情况。
免责声明:
以上内容来源于外网我们重在信息分享,版权归属原作者或原刊发平台所有,如有侵权、信息有误或其他异议,请联系我们,我们将在24小时内删除或整改。
复合免疫 健康活力





























