
微生态护肤维稳:口服LPS,翻开敏感肌的“免疫底牌”!
LPS对敏感肌的有效性——改善屏障功能
你是否也曾被“敏感肌”困扰——护肤品一上脸就感觉刺痛、泛红,天气一变皮肤就紧绷干燥,仿佛身体的每一寸屏障都在发出警报?我们总在寻找外用的修护神器,却可能忽略了,真正的答案或许源在我们身体内部,来自一个与微生物共生的奇妙世界。
近年来,科学家的目光正从皮肤表面转向更深的层面:我们与环境中数以万亿计的微生物,其实构成了一个相互依存的“生态系统”。其中,一种名为脂多糖(LPS) 的成分,正颠覆着我们以往的认知。它并非我们传统印象中的“有害物质”,相反,它就像是唤醒皮肤免疫力的“钥匙”。
最新研究发现,当LPS作用于人体表皮细胞时,它并不会引发炎症,而是以一种智慧的方式显著增强我们皮肤的“屏障功能”——它能促进“水泥”丝聚蛋白的合成,加固角质形成细胞之间的“桥梁”紧密连接蛋白,从而有效锁住水分,抵御外界刺激。这意味着,通过适当途径补充LPS,就如同为肌肤的防御工事输送了关键建材。当皮肤的屏障变得坚固,那些“刺痛”、“发痒”的敏感信号自然随之减弱。
今天,我们就来拆解这份来自皮肤微生态的“安全补丁”,一同看看这种存在于我们日常环境中的天然免疫调节剂,是如何从外到内帮助我们,重塑健康强韧的肌肤微生态,告别敏感困扰。
LPS对敏感肌的有效性——改善屏障功能
皮肤与环境中的微生物群落及其成分,有助于维持皮肤的稳态。本研究通过人体实验证实,持续涂抹革兰氏阴性菌成分脂多糖(LPS)对肌肤敏感性和保湿力的影响。为解析其作用机制,我们采用人角质形成细胞株HaCaT为模型,分析了LPS刺激引发的基因变化。一项针对11名敏感肌受试者的乳酸刺激试验表明,含泛菌属来源LPS(LPSpv)的乳液能有效缓解肌肤刺激感。进一步研究显示,受试者角质层水分含量增加,经皮水分蒸发量减少。在利用HaCaT细胞进行的体外实验中,1 µg/mL的LPSpv刺激显示可促进细胞增殖的效果。此外,通过RT-qPCR检测发现,在HaCaT细胞中,100 ng/mL的LPSpv刺激可显著增加与屏障功能相关的丝聚蛋白(Filaggrin)和纤连蛋白(Fibronectin)的基因表达,并显著提升与紧密连接相关的闭合蛋白1(Claudin 1)的基因表达。这些结果表明,LPSpv能够增强表皮屏障功能,可能有助于改善敏感肌肤问题。
引言
皮肤微生物群通过其代谢活动调节维持皮肤的健康状态¹。同时,细菌之间相互牵制,能有效抑制对皮肤有害的病原菌增殖²。此外,除了活体微生物的活动,微生物膜成分对宿主天然免疫的调节作用,也被认为有助于维持皮肤稳态。在微生物膜成分中,革兰阴性菌来源的脂多糖(LPS)是对天然免疫激活最强的物质。由于感染时细菌释放的LPS会引发强烈炎症,因此又被称为“内毒素”³。然而,LPS本身并非毒物:它不仅存在于空气中,日常我们也会随食物被摄入,同时也从常驻细菌中释放不断接触LPS,却并不会因此引发炎症⁴。由此可见,体内细胞与消化道、皮肤细胞对LPS的反应性存在显著差异。例如,血液中的单核细胞受LPS刺激后会表达肿瘤坏死因子(TNF)、白细胞介素-6(IL-6)等炎症细胞因子;而角质形成细胞虽表达LPS受体TLR4,却不会因LPS刺激而诱导促炎细胞因子产生⁵。相反,屏障蛋白丝聚蛋白(Filaggrin)⁶、抗菌物质β-防御素(β-Defensin)的表达上升⁷,创伤愈合所需的一氧化氮合酶(iNOS)也被诱导⁸。研究显示,朗格汉斯细胞受LPS刺激后,其促炎细胞因子表达远低于血液中的树突状细胞,而过敏性趋化因子TARC的表达反而下降⁹ ¹⁰。这些结果表明,在皮肤组织中,LPS主要发挥抗炎和促进自然修复的作用,而非诱导引发炎症。
实际上,已有研究报告指出:将革兰氏阴性菌移植至皮肤¹¹,或经皮给予革兰氏阴性菌溶解物¹²,能够改善特应性皮炎。Nakai 等人通过双盲临床试验证实,含有 Pantoea agglomerans 来源 LPS(脂多糖)的保湿霜可有效促进轻度特应性皮炎的改善¹³。这些结果表明,LPS在护肤领域可能具有应用价值。
当前护肤领域的一个难题是,敏感肌肤人群正在持续增长——即使用化妆品时会出现"刺痛"、"发痒"等不适感的人群。横田指出,虽然"敏感肌"存在多种类型,但皮肤屏障功能下降导致化学物质渗透性增强,正是诱发敏感这一现象的重要成因¹⁴。
关于"敏感肌"的客观评估方法已有若干报告。据研究表明,乳酸刺激试验(LAST)与经皮水分流失率呈正相关,并能有效识别以刺痛和瘙痒为主要特征的敏感肌受试者¹⁵。基于此,本次研究参考屋敷等人的LAST方法¹⁶,招募自述敏感肌的志愿者为研究对象,探讨评估了持续涂抹LPS对皮肤状态的影响。为进一步解析其作用机制,我们采用人角质形成细胞株HaCaT,检测分析了LPS刺激引起的相关基因表达变化。
结果
3.1 刺痛试验
试验期间无受试者脱落。LPSpv 乳液使用前及使用1周、2周、4周后的刺痛评分变化如图-2所示。乳酸水溶液刺激后30秒、2分钟、5分钟各时间点的刺痛评分,与使用前相比,在使用LPSpv 乳液1周、2周及4周后均显著下降。
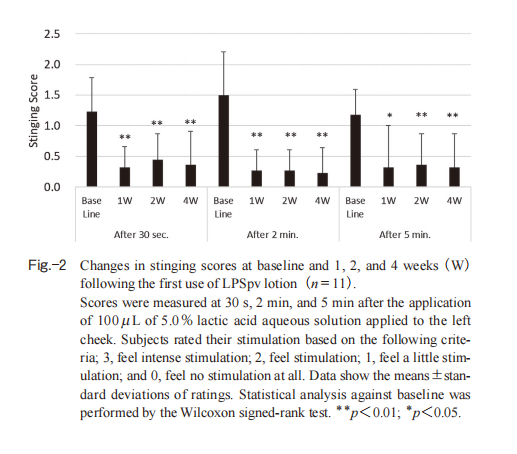
图2.首次使用LPSpv乳液后基线期及第1、2、4周(W)的刺痛评分变化(n=11)。
3.2 保湿力
LPSpv 乳液使用前、使用2周及4周后的皮肤角质层含水量(SCH)和经皮水分流失量(TEWL)变化如图-3所示。在使用2周与4周后,SCH 均显著提升;而TEWL则在持续使用4周后呈显著下降趋势。
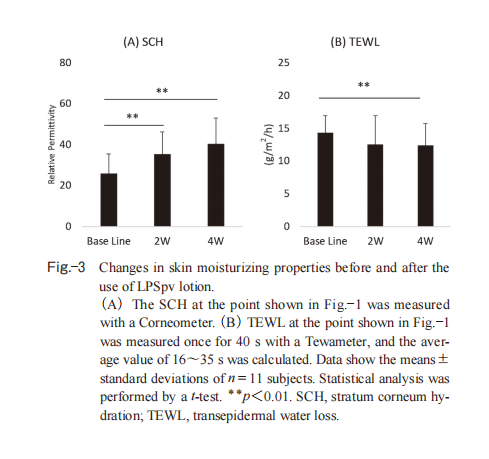
图3.使用LPSpv乳液前后皮肤保湿特性的变化
3.3 增殖促进效果
角质形成细胞的增殖通过促进正常的新陈代谢,可有效防止表皮老化。为此,我们在人角质形成细胞株HaCaT中验证了LPSpv的增殖促进作用。结果显示:虽然100 ng/mL浓度的LPSpv未观察到显著差异,但在1000 ng/mL浓度下,培养第4日的细胞数量较对照组出现显著增加(图-4)。
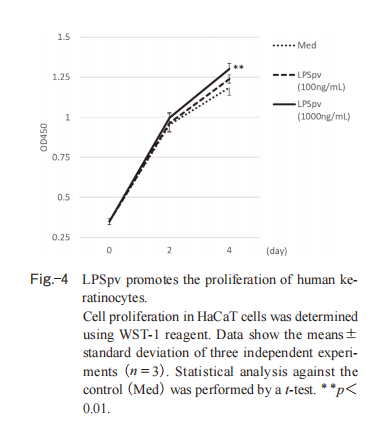
图4.LPSpv促进人角质形成细胞增殖。
3.4 屏障功能相关基因表达
由于在人体试验中LPSpv 乳液显示出可改善敏感及保湿效果的验证,我们采用人角质形成细胞株HaCaT,分析了对影响皮肤屏障功能相关因子的基因表达。将HaCaT细胞分别用100 ng/mL和1000 ng/mL浓度的LPSpv刺激后,通过RT-qPCR分别检测4小时和24小时的基因表达水平(图5)。在100 ng/mL与1000 ng/mL浓度LPSpv刺激24小时后,与角质层屏障功能相关的Filaggrin(丝聚蛋白)和Fibronectin(纤连蛋白)基因表达均呈现显著上调。随后对颗粒层紧密连接相关蛋白Claudin 1、Occludin及Zonula occludens-1(ZO-1)的基因表达进行分析,结果显示:经1000 ng/mL浓度LPSpv刺激4小时后,Claudin 1基因表达出现显著升高;而Occludin与ZO-1在所有浓度和时间点均未观察到显著变化。
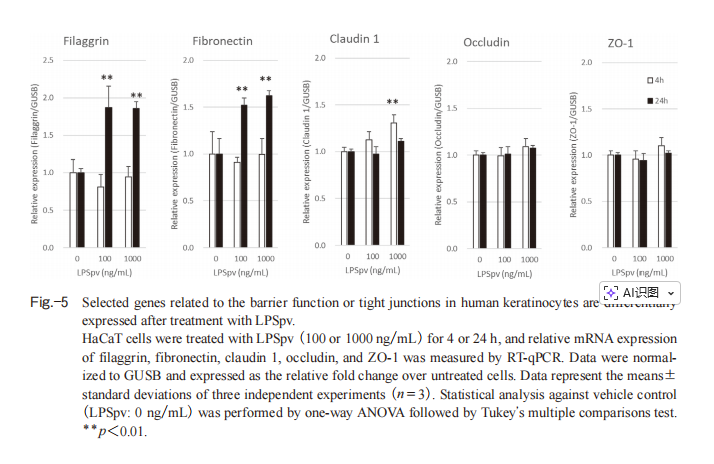
图5.经LPSpv处理后,人类角质形成细胞中与屏障功能或紧密连接相关的特定基因呈现差异表达。
讨论
本试验结果显示,使用LPSpv乳液可有效缓解皮肤刺痛感。此外,在受试者中观察到皮肤角质层含水量(SCH)增加与经皮水分流失量(TEWL)降低的现象。由于本研究为无安慰剂对照的开放试验,上述改善效果尚不能完全归因于LPSpv的单独作用。但需要特别指出的是,所有受试者平日已在使用含保湿成分的基础护肤品,却仍长期自认敏感肌,且试验期间并未更换原有护肤程序。因此,仅凭LPSpv乳液中的β-葡聚糖(BG)和甘油成分难以解释当前改善效果,这充分表明所添加的LPSpv确实具有一定的功效。
皮肤刺激感的产生,是由于外界刺激物渗入皮肤所致;因此,当表皮屏障功能下降时,这种刺激感就会明显加剧。
皮肤屏障功能与表皮结构密切相关。在表皮中,基底层角质形成细胞不断增殖,并在向上迁移的过程中逐渐分化,最终在最外层的角质层,老化细胞会以皮屑形式脱落,这一周期性过程即为皮肤新陈代谢。当细胞分裂增殖速率减缓时,新陈代谢周期随之延长,导致老旧细胞比例上升,表皮结构易老化并削弱屏障功能。因此,促进角质形成细胞增殖被认为能有效提升表皮屏障功能。通过HaCaT细胞实验证实,LPSpv可显著促进角质形成细胞的增殖活性。由此推测,LPSpv 可通过加速角质形成细胞增殖,有效调控皮肤新陈代谢周期,进而改善表皮结构完整性,从而增强皮肤屏障功能。
除促进角质形成细胞增殖外,LPSpv还显著提升了角质形成细胞中丝聚蛋白(Filaggrin)、纤连蛋白(Fibronectin)以及紧密连接关键蛋白Claudin1的基因表达水平。
丝聚蛋白(Filaggrin)最初以400 kDa的前体蛋白(Pro-Filaggrin)形式合成,经蛋白酶分解后转化为37 kDa的单体丝聚蛋白(Mono-Filaggrin)。该单体蛋白具有促进角蛋白纤维聚集的功能,对维持角质层的强度与柔韧性(弹性)具有重要作用。研究已证实,因丝聚蛋白基因变异导致其含量降低的表皮中,角质细胞更容易脱落,这可能诱发特应性皮炎的重要因素之一¹⁸。此外,在角质层最外层,丝聚蛋白会进一步分解为氨基酸和尿刊酸等天然保湿因子。而纤连蛋白(Fibronectin)已被学界确认在皮肤创伤修复愈合过程中发挥关键作用¹⁹。脂多糖(LPS)通过提升丝聚蛋白与纤连蛋白的表达水平,被认为有助于增强角质层的屏障功能。
除了由丝聚蛋白(Filaggrin)和纤连蛋白(Fibronectin)构成的角质层屏障外,颗粒层的第二层还形成了被称为紧密连接的屏障结构²⁰,这些结构在决定皮肤穿透选择性方面起着至关重要的作用²¹。研究表明,紧密连接的形成依赖 Occludin、Claudin、ZO-1 等多种蛋白因子²¹。Claudin家族共有20多种亚型,其中Claudin1在皮肤和肝脏中表达尤为显著。当该基因被敲除时,小鼠无法形成正常的表皮屏障,因皮肤过度脱水导致出生即死亡²²。在皮肤组织中,Occludin和Z0-1仅限于颗粒层表达,而Claudin1则广泛分布于全层表皮。Leonardo等团队研究发现,使用100 ng/mL大肠杆菌来源LPS刺激HaCaT细胞24小时后,Occludin基因表达量显著上升,而Claudin1基因表达量未见明显变化²³。虽然我们尚未明确与该结果存在差异的原因,但考虑到泛菌属(Pantoea)LPS的结构与大肠杆菌LPS存在显著差异²⁴,且在生物活性方面也存在明显区别²⁵,推测不同来源LPS可能对基因诱导模式产生影响。在HaCaT培养条件方面,Leonardo团队采用无血清(FBS)培养基进行研究,而本研究使用了含10%胎牛血清的培养基。这种培养条件的差异可能影响细胞分化程度不同,进而导致反应性差异。关于脂多糖(LPS)对紧密连接的影响机制,仍需进一步深入研究验证。
皮肤作为直接接触外界刺激的组织,其免疫应答不仅涉及朗格汉斯细胞和调节性T细胞等典型免疫细胞,其他细胞也参与其中。事实上,角质形成细胞中同样存在多种Toll样受体(TLR)表达,且已有数篇论文报道,其能通过TLR4受体途径对革兰氏阴性菌成分脂多糖(LPS)产生应答⁵。值得注意的是,角质形成细胞对LPS的应答反应不会引发炎症。体内(皮肤和消化道除外)的细胞将LPS视为细菌感染的标志,当LPS与受体结合时,会分泌炎症性细胞因子以清除细菌。而在皮肤和消化道等环境细菌和常驻菌群本就存在的场所,机体不会引发组织损伤的炎症反应,而是通过增强屏障功能的响应机制符合生理逻辑。本实验的人体试验也证实LPS不会诱发炎症。然而,LPS对敏感肌及SCH・TEWL的改善作用,仍需通过双盲试验等进一步解析验证。此前已有先行研究报道,在一项采用含Pantoea agglomerans LPS的保湿霜与安慰剂对照的轻度特应性皮炎双盲试验中,受试者的瘙痒和皮肤状态均显著改善¹³,这一发现使得LPS对皮肤屏障功能的修复作用备受关注。本次实验观察到LPS能诱导角质层屏障相关因子(如Filaggrin、Fibronectin、Cloudin1等)及紧密连接屏障相关因子的基因表达。后续仍需进一步研究这些因子的基因及蛋白动态变化,以深入阐明LPS在皮肤中的作用。
结论
本研究结果表明,来源于Pantoea vagans的LPS通过作用于表皮细胞,有助于维持皮肤的稳态。作为微生物膜成分之一,LPS有望应用于针对敏感肌肤的护肤化妆品中。
◆ 从外用到内服:一条更为根本的强韧之路
既然外涂LPS被证实能有效改善敏感,那么,一个更根本的问题浮现了:我们能否通过口服,从身体内部系统性地为皮肤补充这种“建筑师”?
假设通过日常补充,让这份构筑健康屏障的指令随着血液循环直达全身皮肤细胞。这不再是表面的修修补补,而是由内而外的系统性滋养与强韧。基于同样的科学原理,口服LPS旨在从内部调节免疫平衡,为皮肤这座“外部器官”提供最源头的支持。当内在的微生态信号趋于强健,外在的敏感、脆弱问题自然也失去了根基。
敏感肌的困扰,或许是一场由内而外的“对话失衡”。而科学,正为我们指明一条新的路径:不再仅仅停留在表面安抚,而是通过口服LPS这样的创新方式,深入参与这场对话,从内部唤醒肌肤固有的防御力与自愈力,重塑健康强韧的肌肤微生态。
免责声明:
以上部分内容来源于外网我们重在信息分享,版权归属原作者或原刊发平台所有,如有侵权、信息有误或其他异议,请联系处理,我们将在24小时内删除或整改。
复合免疫 健康活力





























