
过敏季必看临床新证:天然“免疫教官”对抗鼻炎,口服LPS让过敏反应“守规矩”,带来“无倦”春天!
LPS缓解鼻腔不适——一项安慰剂对照、随机、双盲、平行组比较试验
又到过敏季,鼻塞、流涕、眼睛痒……这些困扰是否正让你离不开抗过敏药?而服药后的昏昏欲睡,是否又成了新的烦恼?最新科研带来令人振奋的消息:一项发表在专业期刊的临床研究揭示,天然成分LPS(泛菌糖脂质)可能成为鼻炎患者的福音!
这项采用最高等级科学验证方法(双盲、安慰剂对照、随机、平行组比较) 的临床试验发现:通过持续摄入含LPS的食品,受试者在使用更少抗过敏药物的情况下,仍能保持相同的症状控制效果。更令人惊喜的是,反映过敏程度的关键指标——总IgE水平和嗜酸性粒细胞计数,在LPS组也显著降低。
如果你正在寻找除了药物之外的过敏缓解方案,不妨花3分钟了解这项颠覆传统认知的研究成果—— 一种通过调节免疫平衡来改善过敏体质的新途径!
LPS缓解鼻腔不适——一项安慰剂对照、随机、双盲、平行组比较试验
摘要
本研究采用双盲、安慰剂对照、随机、平行组比较的研究设计,探讨含成团泛菌脂多糖(LPS泛菌糖脂质)食品对眼鼻过敏症状的影响。研究纳入63名20-65岁患有眼鼻过敏症状的日本受试者,随机分配至LPS组(480µg/天)和安慰剂组。通过为期8周的观察,评估受试者主观眼鼻过敏症状及抗过敏药物使用情况,并检测免疫球蛋白E(IgE)和嗜酸性粒细胞计数作为可能与过敏相关指标。结果显示,两组在眼鼻过敏症状基线变化方面未见显著差异。然而,LPS组使用抗过敏药物的持续时间显著缩短,抗过敏药物总评分显著低于安慰剂组。在第8周时,经抗过敏药物评分校正后的鼻腔过敏评分在LPS组明显更低。LPS组针对屋尘和杉木花粉的特异性IgE水平以及嗜酸性粒细胞计数呈下降趋势,且在第4周时LPS组的总IgE水平和嗜酸性粒细胞计数显著低于对照组。结论表明:含LPS食品能有效缓解眼鼻过敏症状,从而减少抗过敏药物的使用需求(UMIN000049974)。
引言
过敏症可分为Ⅰ型、Ⅱ型、Ⅲ型和Ⅳ型。其中涉及IgE型抗体的Ⅰ型过敏(如支气管哮喘、花粉症、特应性皮炎、荨麻疹、食物过敏等)近年来发病率持续攀升。以日本环境省发布的《2022年花粉症环境健康手册》数据显示,花粉症患病率从1998年的19.6%增至2008年的29.8%,到2019年更是达到42.5%,几乎每十年增长近10%。根据《日本过敏性鼻炎管理实用指南2020版[1]》预测,未来花粉症患病率可能进一步上升。此外,日本消费者厅发布的《2022年食品过敏标签相关研究项目报告》显示,2020年即时食物过敏病例达6080例,较2017年调查数据(4851例)呈明显增长。
关于过敏发生率的上升现象,Strachan于1989年提出:“在过去的一个世纪里,家庭规模的缩小、家庭设施的改善以及个人卫生标准提高,减少了年轻家庭成员之间交叉感染的机会。这可能导致特应性疾病在临床上表现得更为普遍,且在富裕人群中更早出现,类似于花粉症的情况”,这一理论观点被称为卫生假说[2]。
随后在2002年,Braun-Fahrländer等人开展的欧洲流行病学研究证实:相较于卫生条件良好的城市儿童,生活在农村地区、自然接触革兰氏阴性菌成分脂多糖(LPS)的儿童患花粉症和哮喘的概率更低,这一发现为“卫生假说”提供了有力证据[3]。该研究揭示,卫生环境与过敏症发展存在关联,而LPS这种细菌成分正是抑制过敏反应的关键所在。
在Inagawa等人的研究表明,通过皮内注射成团泛菌脂多糖(LPS)可有效抑制小鼠的IgE依赖性过敏反应[4]。Yoshioka 等人在人体双盲试验中也证实,含有醋酸菌提取物的食品能显著缓解杉木花粉引起的鼻部不适[5,6]。由于醋酸菌属于革兰氏阴性菌,其提取物中含有LPS。
这些研究结果表明,摄入LPS可能有助于缓解Ⅰ型过敏症状。
众所周知,脂多糖(LPS)在感染或人工注入体内时是一种会诱发强烈炎症的物质[7-20]。然而,该成分广泛存在于自然环境中,通过口服或皮肤接触并不表现毒性。自2007年以来,由Macrophi Inc. (Kagawa,日本)公司生产并销售以LPS为活性成分的食品原料Somacy-FP100,相关健康食品也陆续上市,至今未发现对健康造成损害的案例。
尽管Somacy-FP100的标准摄入量为1 mg/kg/天(按LPS计为10 µg/kg/天),但根据经济合作与发展组织的标准,开展的大鼠90天重复给药试验证实,4500 mg/kg/天(LPS为45,000µg/kg/天)的高安全水平,未观察到不良反应影响[21]。
此外,迄今已开展了4项使用含Somacy-FP100食品的双盲人体临床试验;所有受试者均未出现实验室检查指标异常或不良事件,从而证实了该产品的安全性[22-25]。
此外,在一项针对30名患者的双盲免疫学试点研究中,研究人员使用含活性成分LPS的Somacy-FP100食品进行测试。结果显示,LPS能有效抑制受试者的眼鼻过敏症状[22]。当仅分析出现症状的患者时,LPS组的过敏症状呈现统计学意义上的显著改善。这表明通过食用含LPS的食品,可能有助于预防和改善眼鼻过敏问题。然而,目前尚未开展足够规模的人体研究,以评估验证摄入LPS对眼鼻过敏的具体影响。
因此,本研究旨在验证含LPS食品是否能减轻健康人群(指无特定慢性疾病、未接受任何医院治疗且不影响日常生活)的眼鼻过敏症状。为评估对鼻部过敏反应的影响,主要生理指标结果通过日本鼻结膜炎生活质量问卷进行主观问卷调查,评估眼鼻过敏症状及其对日常生活的干扰程度。同时采用每日记录方式监测研究期间抗过敏药物的使用情况,并通过血液检测观察免疫球蛋白E(IgE)和嗜酸性粒细胞计数,这两种已知在过敏发作时会升高的生物学指标。
结果
①参与受试者的基底特征
试验于2023年1月16日至2023年4月22日进行。共有63名受试者(17名男性和46名女性,平均年龄:46.4 ± 9.8岁)参与了这项研究。
分析的参与者筛选流程如图1所示,参与者的基本特征见表2。研究最终纳入安慰剂组32人与LPS组31人。本研究严格遵循试验方案执行,通过每日记录确认LPS摄入情况:在63名参与者中,62人摄入率≥90%(含43人摄入率达100%),仅1人摄入率为73.2%。研究期间未报告不良事件或受试者退出,共有63例患者被纳入意向性治疗(ITT)分析。此外还进行了按方案集(PPS)分析,排除了6例可能影响结果的受试者(含研究期间感冒症状超10天者3例、试验食品摄入量不足80%者1例、前半期记录丢失者1例、调查延期≥7天者1例),最终在PPS分析中,安慰剂组29人与LPS组28人纳入分析。
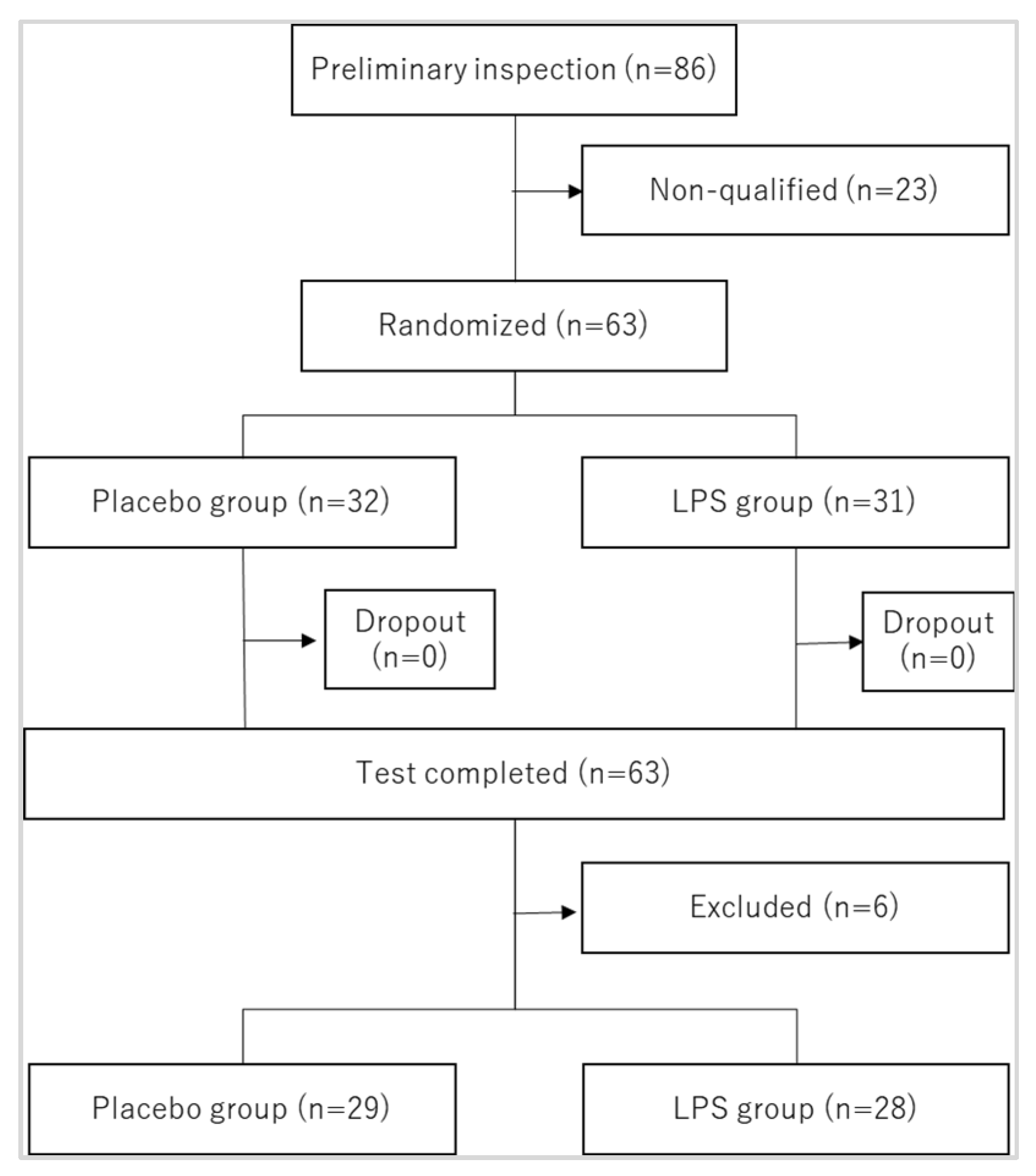
图1. 受试者筛选流程。排除对象包括:(1) 研究期间感冒症状持续超过10天者;(2) 试验食品摄入率低于80%者;(3) 丢失研究前半段日志者;(4) 调查日期偏离计划时间超过7天者。
表2.参与者的基本特征。
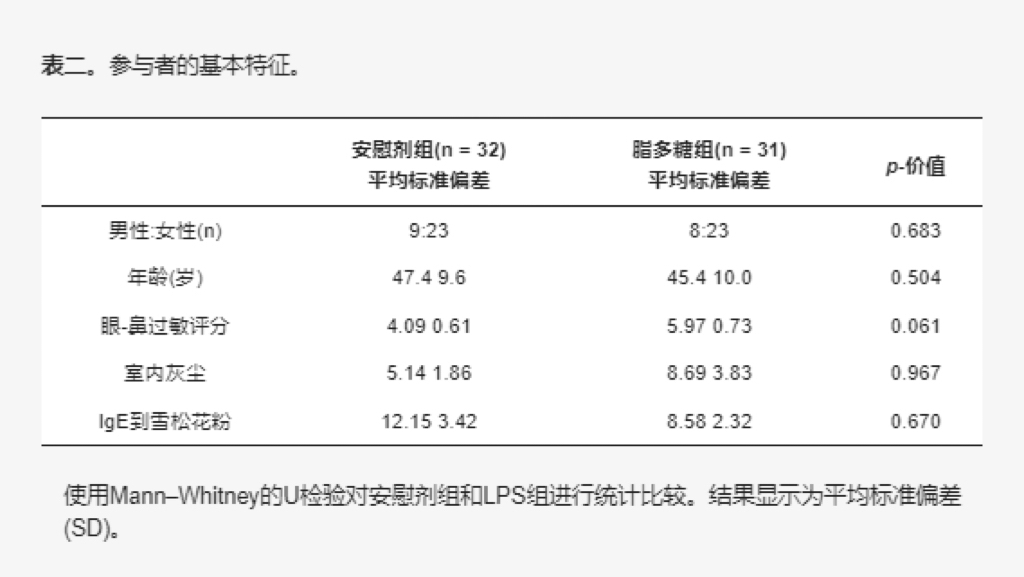
两组在性别、年龄方面无显著差异;在研究开始时的总体鼻部症状评分、对屋尘的IgE水平以及对杉木花粉的IgE水平方面亦无显著差异。
②眼鼻过敏症状
眼鼻过敏症状、生活质量(QOL)和综合状态评分相对于基线的变化,以及摄入后4周和8周的实验组数据如表3所示。图2显示了在研究期间试验地香川县的花粉散布情况。杉树花粉和柏树花粉分别在3月初和3月下旬是高峰期。数据显示,大多数参与者的眼鼻过敏评分相比基线有所上升(见表3)。在测试食品摄入开始后4周和8周时(调查过去1-2周的状况),对所有眼部-鼻腔过敏症状、整体生活质量和综合状态进行的ITT分析显示,安慰剂组与LPS组之间未显示出统计学显著差异。当分别分析眼部与鼻腔过敏症状时,结果也未呈现统计学显著差异。这一结果在方案集(PPS)分析中同样成立。
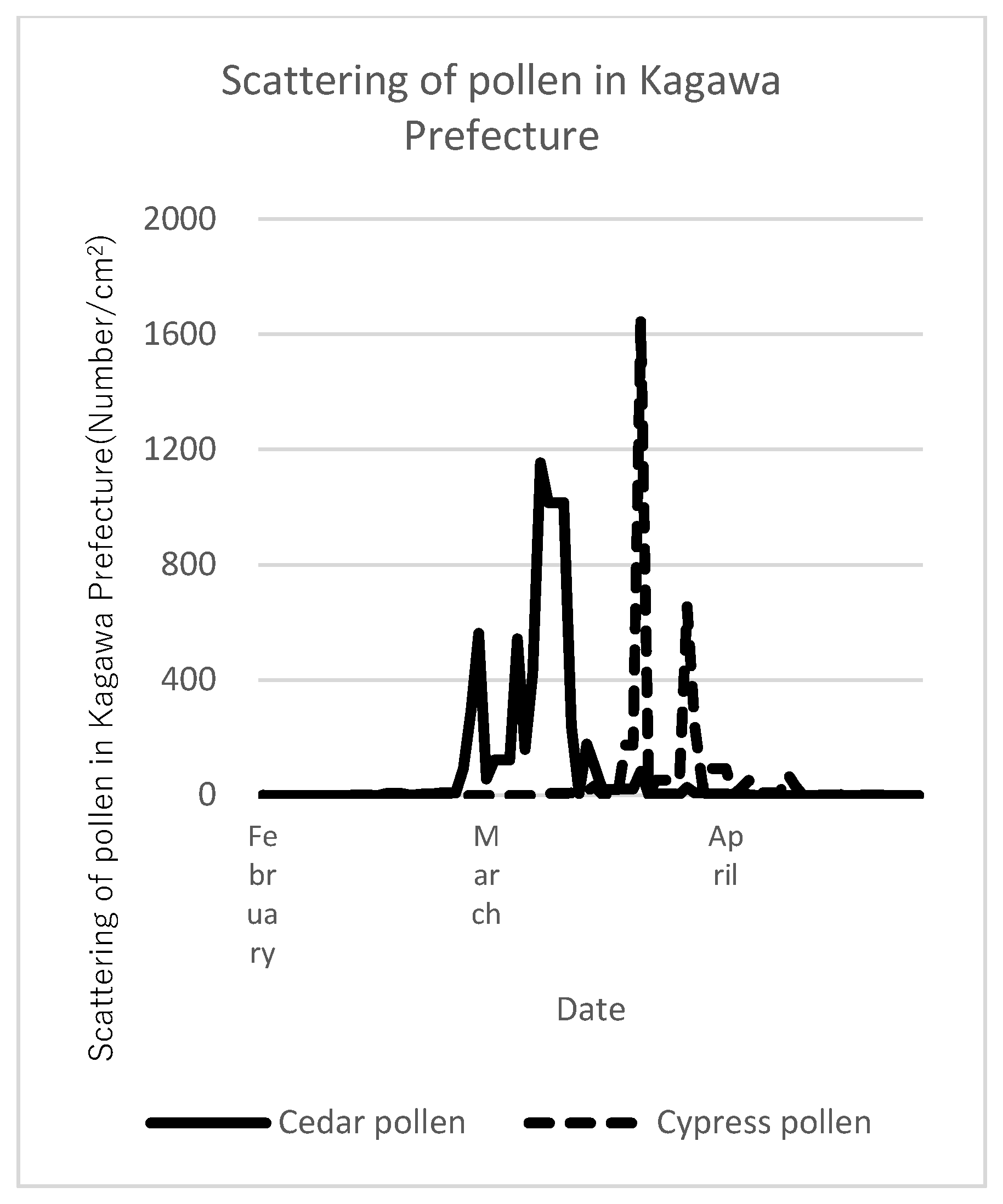
图2.研究期间花粉的扩散情况。测试地点香川县的花粉扩散状况由香川大学测量。
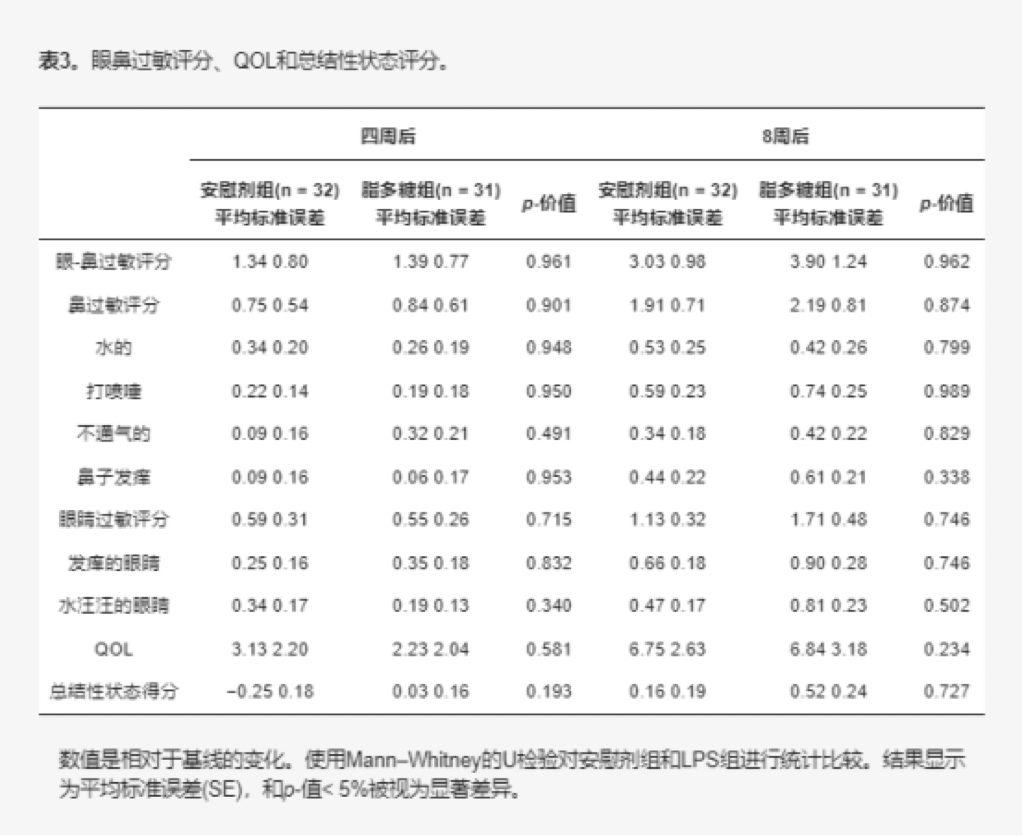
表3.眼鼻过敏评分、生活质量(QOL)和综合状态评分。
对鼻部过敏症状的分析按以下因素进行了分层:年龄≥40岁、性别、体重指数≥25 kg/m²、筛查时IgE评分≥10 UA/mL(受试者筛查时对杉木花粉的平均IgE为10.39)、筛查时鼻部过敏评分≥5(参与者筛查时的平均评分为5.02),以及研究开始日期。结果显示,安慰剂组与LPS组在总体眼鼻过敏评分方面未发现统计学显著差异。该结果在方案集(PPS)分析中也保持一致。
③结合抗过敏药物使用情况对眼鼻过敏症状的分析
在本研究中,参与条件规定研究开始前4周内未使用抗过敏药物,但研究期间抗过敏药物的使用不受限制。因此,尽管两组在花粉飘散开始后的眼鼻过敏症状方面无显著差异,但仍需考虑抗过敏药物的影响(见表3)。
在ITT分析中,被纳入分析的受试者里,安慰剂组有16人、LPS组有6人在研究期间使用了各类型的抗过敏药(见表4)。在研究期间,LPS组使用抗过敏药物的天数显著少于安慰剂组(图3A)。此结果与方案集(PPS)分析结果一致。
表4.服用抗过敏药物的人数。

图3.抗过敏药物。
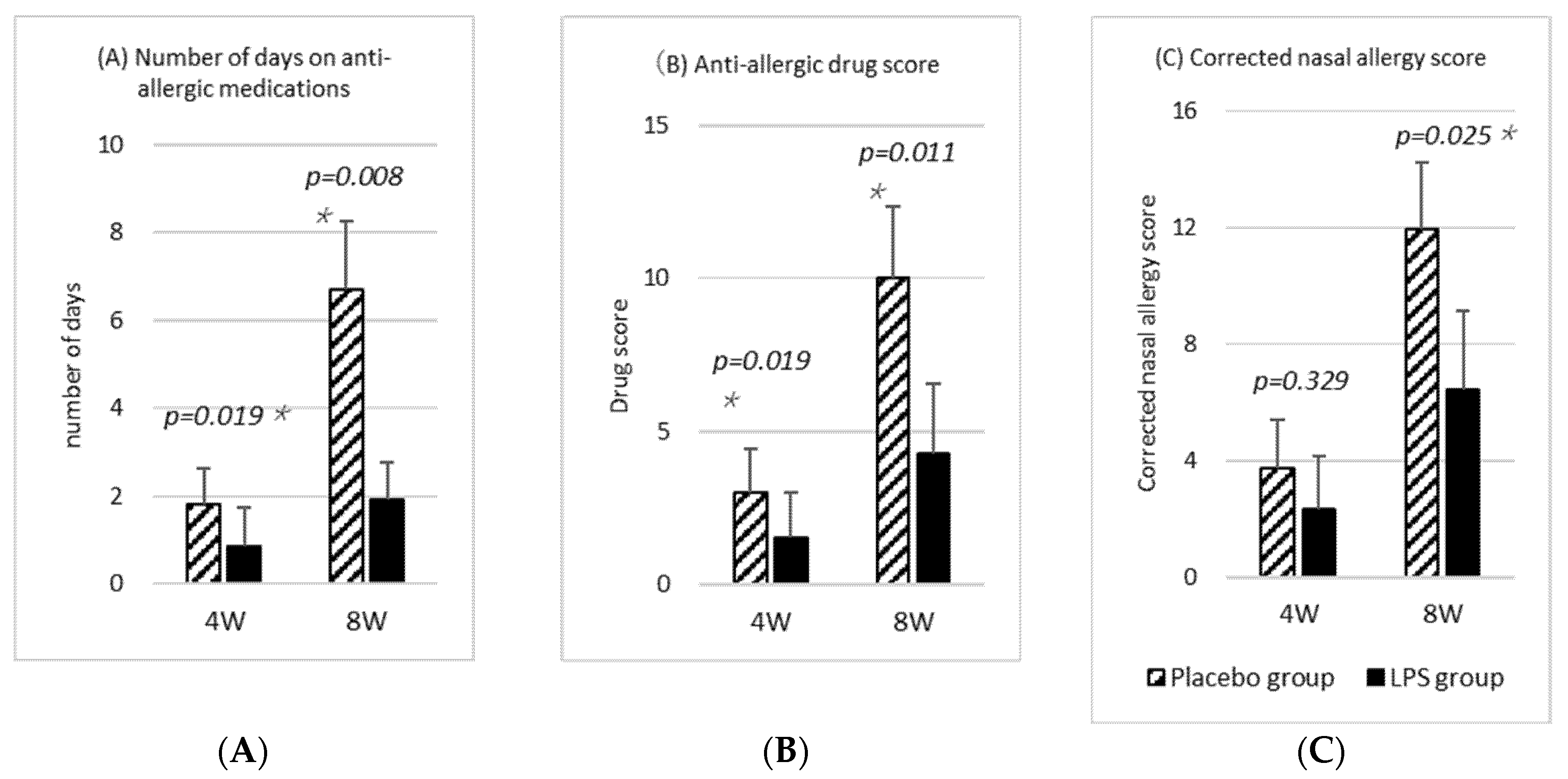
针对鼻部过敏症状,图3C展示了校正后的鼻过敏评分,即症状评分相对于基线的变化再加上药物评分。由于该评分用于鼻部过敏的诊疗,因此我们采用了六类过敏症状中的四种类型鼻部过敏症状进行评分(见表3)。第4周的校正鼻过敏评分是通过将摄入开始至第4周的药物评分与第4周鼻过敏评分变化值相加;第8周校正鼻过敏评分则为第5周至第8周的药物评分与第8周鼻过敏评分变化值之和。考虑到所有受试者在研究开始前4周内均未使用药物,因此将摄入前鼻过敏评分的药物评分设为零。经过抗过敏药物影响校正后的鼻过敏评分显示,LPS组在第8周的校正鼻部过敏评分显著低于安慰剂组[图3C],这一结果在方案集(PPS)分析中也得到验证。此外,若用眼鼻总过敏评分替代鼻部过敏评分并结合药物评分进行校正,意向性治疗(ITT)分析亦显示,LPS组在第8周的校正过敏评分显著更低(p = 0.045)。
④IgE和嗜酸性粒细胞计数变化
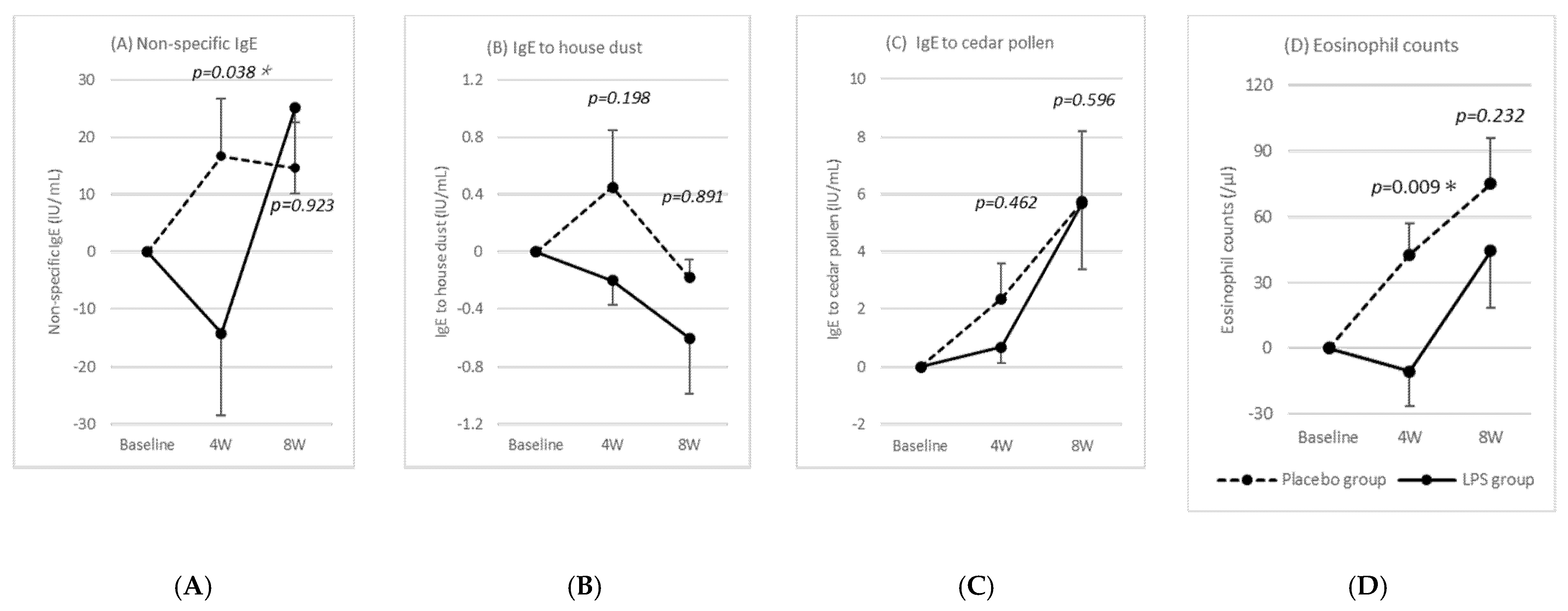
图4显示了摄入开始后4周和8周时,与基线水平相比的IgE和嗜酸性粒细胞计数变化,这些指标与过敏症状相关。在整个研究期间,LPS组的屋尘IgE、杉木花粉IgE及嗜酸性粒细胞计数均较安慰剂组呈降低趋势,其中总IgE与嗜酸性粒细胞计数在试验食品摄入开始后4周时,LPS组已显著低于安慰剂组。
图4.lgE和嗜酸性粒细胞计数的变化。
⑤安全性评估
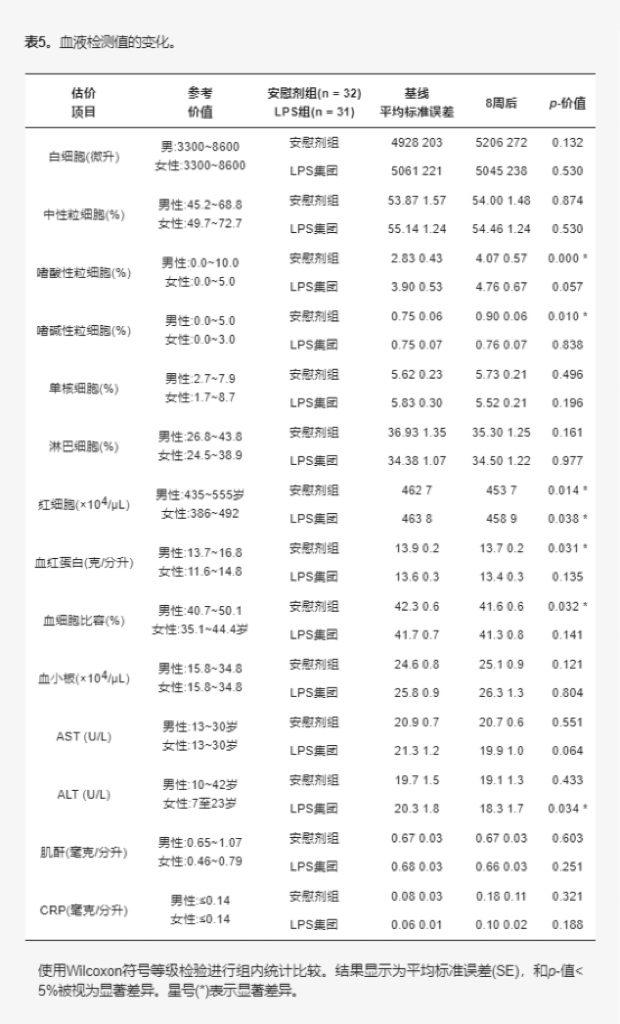
在研究期间未报告任何不良事件,所有参与者均未中途退出。基线值与8周摄入后血液检测指标的变化如表5所示。所有血液学及血液生化检测结果均显示,安慰剂组和LPS组的数值波动均在参考值范围内。这一结论在PpS分析中也得到验证。主要研究者评估认定,连续8周持续摄入含LPS的食品是安全的。
表5.血液检查值变化
讨论
本研究旨在探讨LPS作为膳食成分的应用价值,因此采用摄入方式进行实验展开研究。这项为期8周的平行分组、随机、双盲的研究,以健康受试者(无特定慢性疾病、未接受任何医院治疗、日常生活不受影响)为对象,通过观察其眼鼻过敏症状、抗过敏药物使用情况,以及IgE和嗜酸性粒细胞计数的变化,系统评估LPS摄入对眼鼻过敏症状的影响。研究期间未出现不良事件、受试者退出或血液生化指标异常等不良事件。
我们此前在一项包含30名患者的试点研究中,探讨了含LPS食品对免疫系统的影响。该研究主要考察眼鼻过敏症状。但由于未对受试者进行眼鼻过敏症状筛查,LPS组和安慰剂组眼鼻过敏症状的实际发生率为37%。当仅分析出现症状的患者数据时,LPS组的症状严重程度显著减轻[22]。因此,本研究将筛选标准设定为:通过JRQLQ量表评估眼鼻过敏症状评分为2-10分,或对室内尘螨和杉木花粉的特异性IgE水平≥0.35 UA/mL的受试者。JRQLQ是日本常用的眼鼻过敏问卷,已被鼻过敏实践指南推荐用于生活质量评估。最终纳入的受试者人数为:安慰剂组32人,LPS组31人。
我们的食品测试于1月中旬至4月下旬进行,是与试点研究相同的时间段。在此期间,杉木与柏树花粉的飘散在3月初至3月下旬变得更加明显,受试者的眼鼻过敏症状也相应加重。
对摄入4周和8周后的眼鼻过敏症状进行分析显示,LPS组与安慰剂组之间未见显著差异。如前所述,在早期的试点研究中,当分析仅限于出现症状的受试者时,LPS组的症状严重程度显著轻于安慰剂组。相反,本研究预先筛选了过敏者,尽管研究期间眼鼻过敏症状的发生率为100%,但两组症状却未见显著差异。
另一方面,在两组使用抗过敏药物的天数的比较中,LPS组的用药持续时间显著短于安慰剂组。这表明受试者根据自身症状使用抗过敏药物来控制眼鼻过敏症状,因此未观察到症状差异。事实上,通过将“鼻过敏评分”与“根据活性成分类型测量并记录的抗过敏药物评分”相加计算得出的校正鼻过敏评分。该方法用于鼻过敏的诊断治疗——在LPS组显著降低,这表明口服LPS至少能缓解减轻了鼻部过敏症状。
此外,我们还研究了与过敏症状相关的IgE和嗜酸性粒细胞计数。除尘螨过敏原IgE外,总IgE、杉木花粉特异性IgE及嗜酸性粒细胞计数均随花粉扩散量增加而上升。然而在整个研究期间,LPS组对尘螨过敏原IgE、杉木花粉特异性IgE及嗜酸性粒细胞计数均低于安慰剂组,且在第4周时,LPS组的总IgE和嗜酸性粒细胞计数显著更低。这表明LPS可能具有抑制IgE产生并发挥抗炎作用的潜力。然而,LPS摄入与IgE和嗜酸性粒细胞波动之间的相关性仍需进一步验证。
LPS,也称为内毒素,在经口或经皮给药时均未表现出毒性[27–29]。此外,近年来随着过敏性疾病发生率持续攀升[3,30-35],口服LPS已被视为是抑制过敏的潜在有效途径。
口服LPS抑制过敏反应的作用机制尚未完全明确,但可考虑以下可能性:LPS抑制IgE抗体依赖型Ⅰ型过敏的潜在机制可能是通过调节Th1/Th2细胞平衡[27]。辅助性T细胞(Th细胞)在不同细胞因子刺激下会分化为Th1或Th2细胞——Th1细胞负责诱导细胞免疫,而Th2细胞则主要诱导体液免疫,特别是促使B细胞产生IgE抗体[36-39]。Th1和Th2细胞本应相互抑制维持平衡,但在Ⅰ型过敏中,Th2细胞因某种原因占据主导地位,并对本不应攻击它们的抗原产生过度反应[40-47]。LPS与巨噬细胞、树突状细胞、肠上皮细胞等黏膜细胞表面表达的“Toll样受体4(TLR4)”结合,会促使这些细胞分泌IL-12等细胞因子,从而促进Th1细胞分化,使Th2细胞的主导地位回归正常状态,恢复Th1/Th2平衡,这可能是改善过敏症状的关键机制[48]。
另一种可能机制是LPS通过激活调节性T细胞(Treg细胞)发挥作用。Treg细胞能够直接抑制过敏原特异性Th2细胞的活化,减少促进Th2细胞活性的细胞因子IL-4、IL-5、IL-13和IL-9的产生,并通过直接影响肥大细胞、嗜碱性粒细胞和嗜酸性粒细胞来抑制过敏性炎症[49,50]。据报道,这些表达TLR4的Treg细胞在LPS的刺激下增殖,并进一步增强其抗炎功能[51-53]。因此,LPS也可能通过激活Treg细胞来缓解过敏症状。
虽然Braun-Fahrländer 团队的研究已证实,幼年期摄入LPS可降低特应性过敏性疾病的发生风险[3],但本研究结果表明,LPS摄入对成人过敏症状的缓解也同样有效。Braun-Fahrländer团队指出,幼年期接触LPS可能引发免疫耐受,进而抑制获得性免疫的发展。然而,由于口服摄入的LPS不被人体直接吸收,体外实验中先天免疫细胞对高浓度LPS刺激产生的免疫耐受现象,并不能直接应用于口服给药的LPS。尽管LPS摄入可能影响幼年期获得性免疫的发育,但本研究中观察到的成人过敏症状抑制现象,表明LPS在调节获得性免疫过程中发挥着重要作用。
既往关于含LPS食品的人体研究已确定每日摄入量为400-600µg。本研究中测得的摄入量同样为480µg。尽管现有结果所有实验案例均观察到LPS的积极效果,但该剂量是否足以充分展现LPS功效仍需进一步验证。此外,LPS摄入的起始时机与持续周期,也可能是影响疗效的重要因素。
关于过敏性疾病发病率,根据日本厚生劳动省2011年发布的《风湿病与过敏症对策研究报告》显示:“日本总人口中约每两人就有一人患有某种过敏性疾病,且病例数量正快速增长。”预计将有更多人会出现眼部和鼻部过敏症状,这些症状虽未达到疾病范畴,却可能因过敏性鼻炎(QOL)导致的季节性生活质量下降。虽然抗过敏药物能暂时抑制症状,却常伴嗜睡等副作用,因此开发有助于缓解过敏症状的安全食品具有重要意义。未来,开发含LPS且具备抗过敏功效的食品值得期待。
结论
口服LPS减少了眼鼻过敏症状所需的抗过敏药物剂量。尽管抗过敏药物的剂量减少,眼鼻过敏症状却未见加重,这一事实被认为是LPS缓解了眼鼻过敏症状的结果,表明口服LPS对眼鼻过敏症状具有改善作用。
免责声明
以上部分内容来源于外网我们重在信息分享,版权归属原作者或原刊发平台所有,如有侵权、信息有误或其他异议,请联系处理,我们将在24小时内删除或整改。
复合免疫 健康活力





























