
免疫力“躺平”时代,解密日本力捧的LPS“四两拨千斤”的防御逻辑有多绝?熬夜党/压力族/中老年必看!
口服LPS对于预防多种疾病的益处和有效性
在日本,一种从土壤中“破译”的天然物质——LPS,天然免疫调节,科学辅助健康新选择!
它不是抗生素,却能激活人体免疫“哨兵”巨噬细胞,不直接杀菌,却能通过“训练”免疫系统,从根源降低感染、癌症甚至老年痴呆的风险。
日本为何成为LPS研究与应用的全球先驱?
答案藏在近十年《Nature》《Cell》的论文里:
1、免疫练兵场:LPS通过TLR4受体“点火”巨噬细胞,让免疫系统长期保持“战备状态”,抵御病毒、细菌甚至癌细胞突袭。
2、精准调控力:与传统抗生素“无差别轰炸”不同,LPS能平衡促炎/抗炎信号,避免免疫过度反应(如过敏、肠炎)。
3、耐药性破局:面对超级细菌威胁,LPS从“增强宿主防御”切入,让病原体无处遁形却无法进化抵抗。
“以菌治百病”的真相:
日本医院将LPS纳入糖尿病、癌症术后、慢性疲劳等治疗方案,正是看中其“四两拨千斤”的特性——无需直接攻击病灶,而是通过“训练”免疫系统,重构人体自愈的底层逻辑。
这种“菌体智慧”的临床应用,正在颠覆现代医学的困局,例如:
1. 糖尿病:从“降糖战争”到“免疫维稳”
传统控糖药如同“消防队”,只在血糖飙升时紧急灭火,却无法修复胰岛β细胞的“慢性自杀”(自身免疫攻击)。
✅ LPS破局方案:
激活肠道派尔结巨噬细胞,抑制过度活跃的T细胞,减少胰岛炎症,促进GLP-1分泌,双路径改善胰岛素抵抗。
2. 癌症术后:化疗不再是“杀敌一千自损八百”
放化疗如同“核弹洗地”,在剿灭癌细胞的同时摧毁免疫防线,导致多数患者死于继发感染。
✅ LPS护航策略:
刺激骨髓释放“免疫预备军”单核细胞,加速中性粒细胞再生,降低化疗后感染。上调PD-L1表达,与免疫检查点抑制剂协同“围剿”残余癌细胞。
“LPS不是抗癌药,但它让患者有‘体力’扛到治愈临界点。”
3. 慢性疲劳:揪出“能量黑洞”的元凶
线粒体功能衰竭如同“电厂瘫痪”,传统疗法仅靠刺激神经递质,无异于给停电城市发手电筒。
✅ LPS能量续航:
激活巨噬细胞线粒体生物合成,抑制“疲劳毒素”IL-6过度分泌,阻断“脑-免疫-肌肉”恶性循环。更颠覆的是,研究发现阿尔茨海默病患者脑部TLR4活性普遍低下,而LPS或成“唤醒”神经免疫的关键钥匙。
当全球深陷“过度医疗”与“耐药危机”的泥潭,LPS代表的“免疫赋能疗法”或许正在改写规则——不是杀死疾病,而是让人体自身成为“最佳防线”。但需强调的是:LPS目前多为辅助治疗手段,而非替代主流疗法,患者使用需严格遵循医嘱。
- 以下为相关文献详情内容 -
口服LPS对于预防多种疾病的益处和有效性
摘要
众所周知,在哺乳动物中静脉注射LPS将产生重度毒性。据报道,人体静脉注射LPS的最大耐受剂量仅为 1~4 ng/kg 体重。然而,口服高剂量的LPS却不会在其他哺乳动物、鸟类、鱼类中引起毒性反应或全身炎症。在一个大鼠实验中,持续两周口服高剂量的LPS(2 mg/kg)未引发毒性损害。此外,还有多个实验表明,口服LPS对于多种疾病具有预防作用和治疗效果,包括过敏性疾病和生活方式相关疾病。这些结果表明LPS通过黏膜给药不同于注射用药,可以经另一种生物反应调节机制而发挥其作用。LPS黏膜给药被认为在疾病预防中具有广阔的前景,然而LPS这一物质的使用仍十分少见。为了扩大口服LPS 在预防生活方式和过敏性相关疾病中的应用,阐明口服LPS后引起免疫反应的机制十分必要。这篇简短的综述,旨在阐述近来学界对口服 LPS的用途及有效性的研究。
LPS的结构
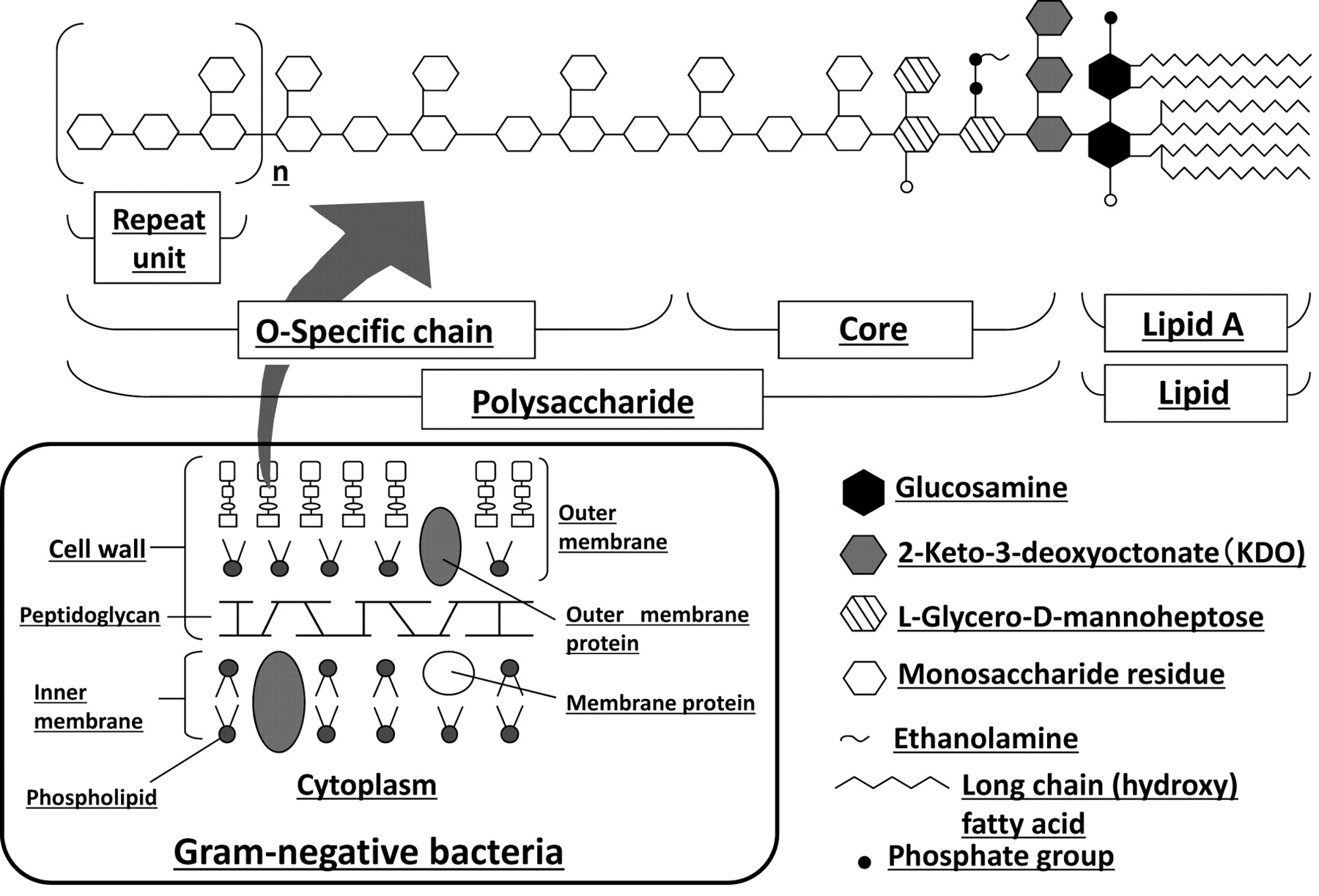
LPS是革兰氏阴性菌外膜的主要成分,由于其亲水性多糖和疏水性脂质部分,具有两亲性特性。LPS其基本结构包括三个部分:(i)脂质A、(ii)核心糖、(iii)和O抗原(O-多糖)。脂质A由4到7个脂肪酸链与两个葡萄糖胺结合,核心糖部分由8碳糖组成,酮-脱氧八烷酸酯(KDO),在各类菌种中高度保守。LPS的核心区域是含有特征性糖残基、KDO和庚糖类的低聚糖,其化学变化比O抗原更有限。脂质A作为一个LPS细胞的膜锚点(图1)。
LPS的免疫反应是由于它与免疫细胞和一些上皮细胞的受体相结合,从而导致细胞内信号激活细胞核转录因子,最终引起免疫反应的发生。学者普遍认为,CD14通过LPS结合蛋白(LBP)和CD14-LPS复合物催化转移LPS单体后,CD14作为LPS的高亲和力受体(1)。toll样受体(TLRs)的作用和结构在先天免疫过程中发挥着重要作用。免疫细胞能识别病原体上存在的特异结构,如肽聚糖、脂多糖、β-1,β-葡聚糖、双链RNA和非甲基化的CpG DNA(1,2)。
CD14、TLR-4和髓样分化因子-2(MD2)的复合物具有更高的灵敏度,它在LPS-LBP复合物浓度仅为0.1 ng/ml时就可以诱导产生细胞内信号(3)。因此,促炎细胞因子,如肿瘤坏死因子(TNF)-α,白细胞介素(IL)-1β,和IL-6被树突状细胞(DCs)、T细胞和B细胞、粒细胞、自然杀伤细胞和巨噬细胞诱导并激活为免疫应答。
人们认为,LPS中的脂质A成分负责这些生物活性。然而,我们最近使用针对LPS中O-多糖成分的特异性单克隆抗体,对LPS生物学功能的研究表明了O-多糖链对LPS功能的重要性。这一功能可以被认为是一种与LPS受体相关的凝集素样衔接分子。其结构可能类似于dectins (4),已知它是β-1,β-葡聚糖与TLR-2相关的结合分子。然而,到目前为止还没有研究确定LPS中O-多糖的特异性受体。
图1. LPS的基本结构
静脉注射LPS的生物活性
Otto等人曾报道报道了一项静脉注射LPS发挥抗肿瘤作用的临床试验,该试验在27例晚期结肠直肠癌患者中进行了研究(5)。在试验中观察到有一名患者完全康复,另有两名对药物产生部分响应;然而在患者中LPS的静脉注射还诱导了短暂的肾脏和肝脏毒性。一项I期临床研究确定了静脉给药人类对于流产沙门氏菌的 LPS 的最大耐受剂量为 1~4 ng/kg 体重(6,7)。严重的体质副作用是LPS的剂量限制性毒性因素,包括发热(世界卫生组织III级)、发冷以及低血压(6,8)。在小鼠中静脉注射LPS引起急性毒性的剂量为4~8 mg/kg,致命剂量为50(LD50)(9)。这些结果表明静脉注射LPS可引起全身炎症,从而导致严重的毒性,然而,LPS通过激活先天免疫,可以预见它还具有一些有益的抗肿瘤作用。
口服LPS后的生物学效果
与非肠道途径摄入LPS相比,口服LPS展现了完全不同的实验结果。Oketani等人认为口服LPS对动物无害(13)。Schryvers等人在实验中以20 μg/ml的LPS喂养小鼠40天后,未发现LPS毒性的证
据(14)。Illyés 等人报道了多次口服高剂量的大肠杆菌LPS对于大鼠小肠结构和细胞增殖无明显影响(15)。
我们发现单次口服高剂量的成团泛菌LPS(泛菌糖脂质)(600 mg/kg)对大鼠无副作用(16)。此外,给大鼠连续28天喂养300 mg/kg的这种LPS未产生任何肝毒性、肾毒性、炎症或体重减轻的迹象,而这一剂量几乎是动物(人类、鸡和鱼)中LPS的推荐用量(10μg/kg)的30000倍。以上研究表明:对于动物而言口服LPS是非常安全的。
已有报道阐述了口服LPS后产生的生物反应。Murakami等人报道了正常的C57BL/6小鼠,口服沙门氏菌LPS(100μg/只)7天后,来自其肠道和腹膜腔的B-1细胞被激活(17)。B-1细胞被认为也属于一种吞噬细胞,因为它们在体内和体外都能摄取凋亡的胸腺细胞和大肠杆菌(18),并且具有与吞噬细胞相似的分化潜能(19)。Chen等人报道了,在重度烧伤的小鼠中,口服大肠杆菌LPS(10μg/ml饮用水)对于使用抗菌药物引起的肠道细菌移位和腹膜巨噬细胞抑制有保护作用(20)。口服LPS的有益性质能保护肠道预防细菌感染。Masuda 等人报道了被激活的Paneth细胞可分泌cryptdin-4(21),在防御素中它具有最有效的抗微生物作用,并可能受LPS的诱导而产生(22)。
Rakoff-Nahoum 等人的实验表明,口服LPS能避免缺乏共生菌的小鼠受DSS的诱导而死亡(23)。Márquez-Velasco等人报道了,对于接受盲肠结扎穿孔术的小鼠,预防性的口服LPS,可以显著增加其生存率并减少其靶器官中的炎症反应(24)。
我们曾报道小麦粉的热水提取物(口服)中含有一种可以激活巨噬细胞的物质,它来源于与植物共生的革兰氏阴性菌如成团泛菌(LPS泛菌糖脂质)。这一类细菌的LPS是一种重要的巨噬细胞激活物质并被命名为IP-PA1(25,26)。研究表明,在人类和动物模型中,LPS在预防生活方式相关、过敏性和传染性疾病中有显著作用。口服LPS泛菌糖脂质有助于预防高脂血症(兔子)(27),糖尿病(小鼠和人类)(28),各类传染性疾病(小鼠和虾)(25,29,30)以及溃疡性结肠炎(小鼠)(31),并且它还能产生镇痛效果(小鼠、大鼠和人类)(32-34)。
口服LPS通过肠道的可能途径
Benoit 等人报道了,在体外实验中高纯度的LPS无法通过肠黏膜(35),然而,另有研究表明,在动物口服LPS后在体内可检测到LPS数量增加(36-38)。据估算,通过使用125个i标记的LPS,口服之后在血液中可检测到的LPS约为摄入含量的0.1%到0.25% 。根据这一比例计算,如果机体摄入吸收了1 mg的LPS,则在血液中必将相应存在1μg到2μg的LPS(36)。如果静脉注射这一含量的LPS 则足以在小鼠中引发严重的全身性炎症反应。然而,口服1 mg的LPS 并没有引起游离细胞因子含量的增长。根据这些结果,我们可以确定口服LPS在肠道内的吸收机制与静脉注射的吸收机制不同。最近研究报道的肠道黏膜吸收LPS的多种可能途径总结了见图2(20,36,39-44)。
图2.摄入的LPS通过肠道黏膜的可能途径。
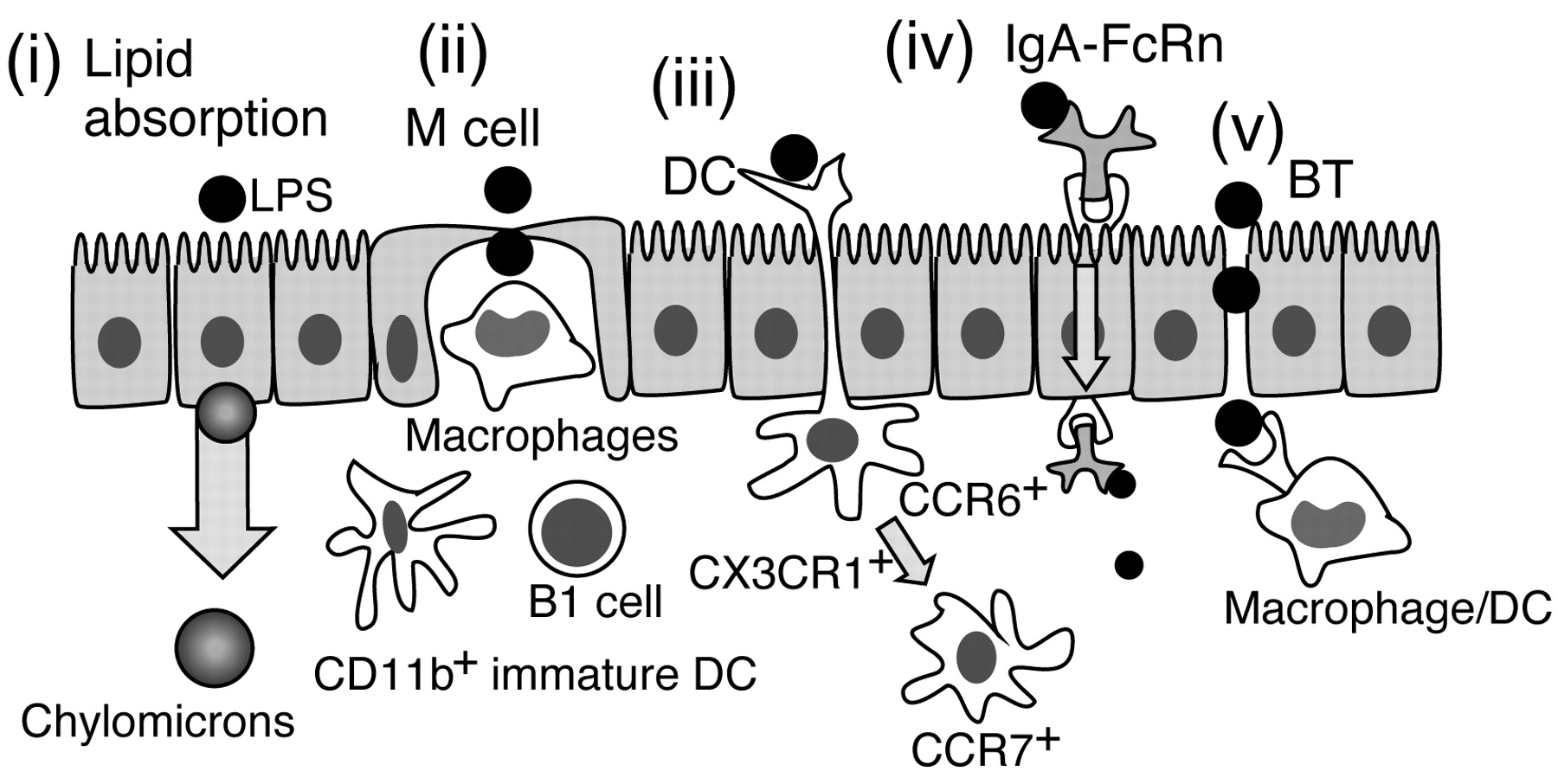
上述LPS转运途径可能允许其穿透进入淋巴组织,例如Peyer淋巴结和肠系膜淋巴结。然而,这些转运机制并不能帮助阐明口服LPS生物功能的机制。为充分研究口服LPS的生理机制和去路,检测其摄入后先天免疫细胞的状态将非常重要。
口服LPS的前景
LPS这一代谢底物随处可见,例如,几乎所有的食物每克都含有1 ng 到1μg的LPS。另一方面,通过口腔和肠道黏膜,人类每时每刻都与大量的细菌相接触。据估计,在人体每克组织中约含有10^3到 10^12个与人类共生的细菌(45)。因此,人类先天就暴露在含有LPS 的环境之中。有一些研究表明,通过这种方式接触LPS可能对维持宿主的免疫平衡(抗过敏体质)(46,47)以及保护肠道预防细菌感染(21)有重要意义。
LPS经口服产生的毒性很低,有许多论文提供了可信的证据支持,LPS 对过敏性和生活方式相关疾病的多种有益作用。因此,在不久的将来口服LPS预计将可应用于维持动物的健康。为促进口服LPS的使用,解释其预防和治疗各种疾病的机制十分必要,然而,LPS通过口服调节宿主健康状态的机制尚不明确。口服LPS所蕴含的功能机制很可能与静脉注射过程中的生化机制有极大区别,因此对前者的探索和研究更显得重要。
目前尚未出现有助于精确测定对口服LPS的反应的评估方法。我们认为,口服LPS产生作用的一种可能的机制可归因于诱导巨噬细胞进入启动阶段(48)。此外,在启动阶段先天免疫细胞对外来物质(如细菌、病毒和凋亡细胞)的灵敏识别被上调。在小鼠实验模型中,LPS的静脉注射(0.1~1 ng/只)可诱导进入启动阶段。这一含量几乎是 LPS的半数致死量(200μg/只)的二十万分之一(9),由于这一剂量的LPS不会诱导促炎细胞因子在小鼠血液中的释放,因而被认为是安全和无毒的。
分子分析表明,启动阶段的启始标志为巨噬细胞膜上TNF-α前体(pro-TNF-α)的出现(49)。有趣的是,pro-TNF-α可以作为邻近的其他巨噬细胞,即激活的巨噬细胞的配体和受体,从而构建形成一个反向信号系统使巨噬细胞可以进行双向应答(50,51)。结合上述研究和数据,我们认为通过口服LPS维持机体体内稳态的机制,包括以细胞间接触为基础的信号传输系统(又命名为巨噬细胞网络系统)(26,52)。
免责声明
以上部分内容来源于外网我们重在信息分享,版权归属原作者或原刊发平台所有,如有侵权、信息有误或其他异议,请联系我们,我们将在24小时内删除或整改。
复合免疫 健康活力





























