
LPS泛菌糖脂质是一种很有前途的通过TLR4途径诱导小鼠全身和粘膜免疫应答的舌下疫苗佐剂
注:
本文为中、日、英三种语言,下方附有中文翻译,供您查阅!
インフルエンザとLPS
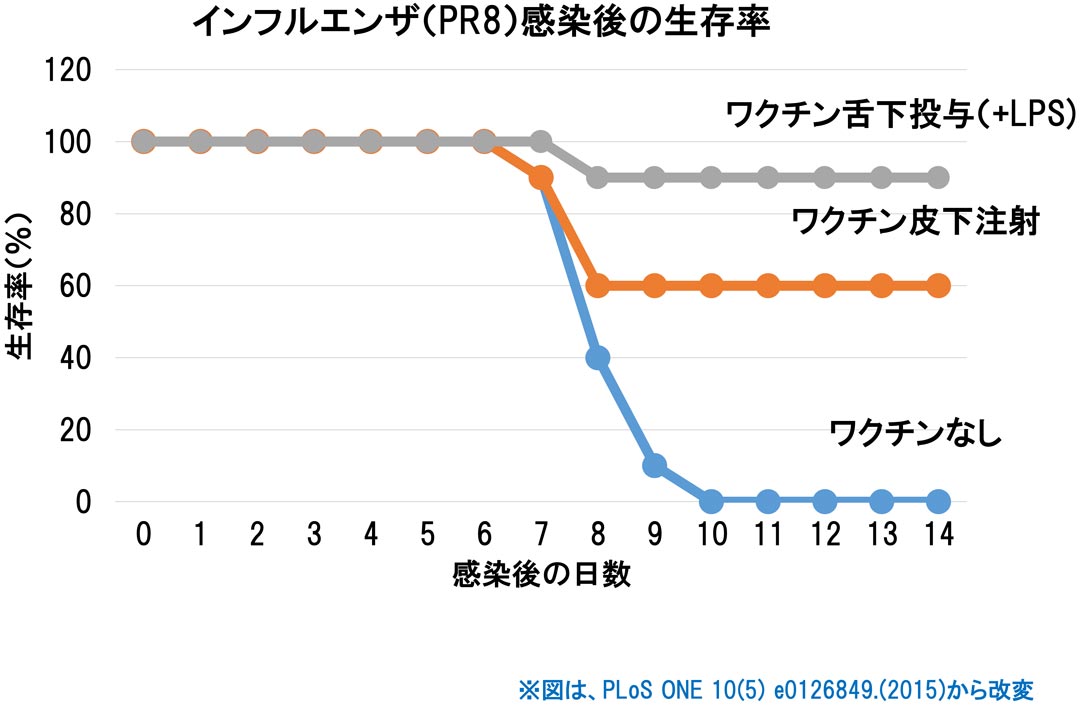
インフルエンザワクチンによる効果的な感染予防に、LPSの経口摂取が有効であることが報告されています(*1)。
ワクチンとは、一度病原菌に晒されるとその病原菌に対する抗体が体の中につくられて、2度目に感染した時には症状が出ないか軽くてすむ、という獲得免疫の原理を応用した予防法です。従って、インフルエンザワクチンとしては、インフルエンザウイルスの一部とか、殺したインフルエンザウイルスが投与されます。ところがこの時、インフルエンザウイルス成分の投与だけでは抗体は効果的に誘導されず、助け(アジュバンドと言います)が必要です。LPSは、この助けとして最高です。
動物実験では、LPSをアジュバンドとしてワクチン投与した場合、抗体産生が有意に高まるので、将来的には注射ではなく、舌下ワクチンの開発も夢ではないことが示されています(*1)。
LPS配合舌下ワクチンの効果
(*1)A Lipopolysaccharide from Pantoea Agglomerans Is a Promising Adjuvant for Sublingual Vaccines to Induce Systemic and Mucosal Immune Responses in Mice via TLR4 Pathway, PLoS ONE 10(5) e0126849.(2015)
中文翻译:
据报道,口服LPS可有效预防流感疫苗引起的感染(*1)。
疫苗是一种应用获得性免疫原理的预防方法,一旦接触病原体,针对该病原体的抗体,第二次感染时就不会出现症状或症状很轻。 因此,作为流感疫苗,可以使用流感病毒的一部分或杀死的流感病毒。 然而,此时仅仅通过施用流感病毒成分并不能有效诱导抗体,需要帮助(称为佐剂)。 LPS 在这方面提供了很大的帮助。
动物实验表明,将LPS作为佐剂进行疫苗给药时,抗体的产生会显着提高,因此未来开发舌下疫苗代替注射剂并不是梦想(*1)。
LPS配合舌下疫苗的效果
LPS泛菌糖脂质是一种很有前途的通过TLR4途径诱导小鼠全身和粘膜免疫应答的舌下疫苗佐剂
摘要
来自成团泛菌(Pantoea agglomerans)的脂多糖(LPSpa)已应用于多个领域,作为Toll样受体4(TLR4)配体,其安全性已得到证实。在此,我们首次展示了LPSpa作为一种有效的黏膜佐剂来激活疫苗诱导的抗原特异性免疫反应。小鼠通过舌下途径接种流感疫苗(HA分裂疫苗)和LPSpa,诱导了HA特异性IgG(系统性)和IgA(粘膜)抗体反应,与皮下接种相比,可显著提高对致死性流感病毒攻击的生存率。在LPSpa舌下给予卵清蛋白后,在靠近免疫部位的粘膜表面和远端粘膜表面诱导卵清蛋白特异性黏膜IgA反应。舌下给予LPSpa可引起颈部淋巴结树突状细胞的局部抗原摄取。LPSpa诱导了树突细胞的细胞因子产生和通过TLR4在树突细胞中的成熟和增殖。综上所述,这些结果表明LPSpa可以作为有效的粘膜佐剂来刺激和激活局部先天免疫细胞,以提高和增强粘膜疫苗的效果,对抗各种病原体。
引言
几乎所有的环境病原体都通过粘膜表面进入人体,包括呼吸道、胃肠道和生殖道,这些部位构成了第一道防线。因此,粘膜疫苗接种是预防感染性疾病最有效的预防措施之一,因为它能引发粘膜和全身免疫反应[1-3]。抗原的舌下(s.l.)给药已被充分证明用于过敏原脱敏治疗[4,5]。s.l.途径最近被证明是预防各种细菌和病毒疾病的疫苗接种的有吸引力的场所[6-10],因为抗原不会暴露于胃肠道引起的降解[11],并且被阻止被重定向到中枢神经系统[12-14]。
对于活化抗原,通过与佐剂(免疫刺激剂)的共同给药,特别是在粘膜表面,可以增强足够的免疫反应以保护免受感染病原体的侵害。灭活流感疫苗(A/PR/8)与突变霍乱毒素(CT)的亚单位和热稳定毒素(LT)的B亚单位的s.l.给药诱导了体液免疫反应并保护免受流感病毒感染[13],这些肠毒素、CT和LT能够作为佐剂[15-17]。通过s.l.接种流感H5N1病毒体与细菌第二信使体c-di-GMP[18]结合,引发了局部IgA反应和唾液血凝集抑制(HI)反应。此外,一些Toll样受体(TLR)配体是HIV gp140和破伤风类毒素的潜在粘膜佐剂[19]。这些发现表明,通过s.l.使用合适佐剂的途径是一种有吸引力的疫苗接种方法。然而,由于安全考虑,如明矾和单磷脂A(MPL)等佐剂在人类中很少使用。为了开发更安全的佐剂,特别是用于s.l.疫苗接种,我们重点关注已经批准用于人类使用的物质。
LPSpa是一种脂多糖(LPS)(TLR4配体),来源于泛菌,一种革兰氏阴性细菌,与小麦[20,21]共生。这种物质的口服或肠道内给药,是从小麦面粉中提取的水提取物或从Pantoea agglomerans(一种细菌)中纯化得到的,能激活先天免疫细胞如巨噬细胞,以预防和治疗各种健康疾病,包括病原体感染、I型过敏反应和癌症在内的各种健康问题[22-26]。此外,还对含有反突变或染色体畸变试验的发酵面粉提取物进行了安全性试验、单剂量毒性、重复剂量毒性和其他皮肤安全性研究进行了安全性试验[27]。这些研究证实了从发酵面粉提取物中提取的LPSpa的口服和经皮给药在引发免疫反应的剂量下没有显著毒性。基于这些特点,推出了若干产品;例如,健康食品的应用以预防和改善代谢综合征,护肤产品以维持皮肤的健康状态,以及用于家畜饲养和水产养殖以激活先天免疫。
在这项研究中,我们评估了s.l.给药的LPSpa在诱导抗原特异性体液免疫反应中的粘膜佐剂活性。s.l.给药的LPSpa抗原通过激活先天免疫细胞:树突状细胞(DCs)的成熟,有效地诱导系统IgG和黏膜IgA的产生和抗原迁移。我们的研究结果表明,LPSpa是增强s.l疫苗的潜在辅助剂。
结果
结果01
LPSpa是一种有效的佐剂,通过皮下免疫(s.l.)诱导HA特异性体液反应
为了阐明LPSpa是否作为s.l.的黏膜佐剂激活针对季节性流感病毒的皮下免疫反应,我们使用了含有3种毒株(H1N1、H3N2和B型)的HA分裂疫苗。这些疫苗毒株是为2012/13年日本季节(IASR来自国家传染病研究所)选择的。通过注射不含佐剂的分裂疫苗的效果尤其对儿童来说效果不佳[30,31]。通过ELISA(图1A-1D)或HI测定(图1E)检测了H1N1、H3N2和B型特异性血清IgG和黏膜IgA的水平。
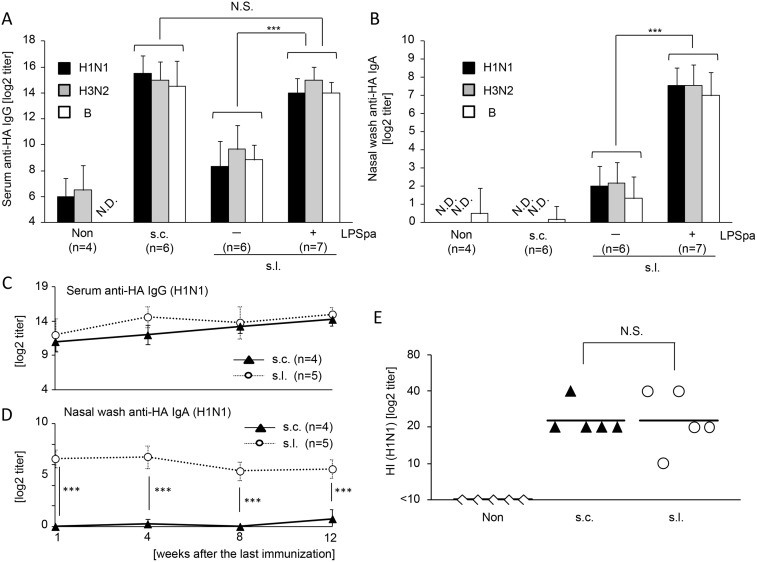
如图1A所示,针对每种毒株的血清HA特异性IgG反应在皮下(s.l.)免疫的小鼠中增加,特别是,用含有LPSpa的疫苗皮下(s.l.)免疫的小鼠诱导产生了HA特异性IgG,其水平与皮下(s.c.)免疫的疫苗相当。HI测定显示出与ELISA相同的趋势,即皮下(s.c.)和皮下(s.l.)免疫LPSpa都能在血清中诱导产生足够的HI抗体(H1N1)(图1E)。相比之下,与非治疗组相比,皮下(s.c.)免疫后在鼻洗液中未检测到HA特异性IgA,但黏膜疫苗接种诱导了IgA反应(图1B)。此外,与不含LPSpa的皮下(s.l.)免疫相比,LPSpa的皮下(s.l.)免疫显著增强了HA特异性IgA反应(图1B)。此外,在最终免疫后直到12周,一直观察到高水平的长期HA特异性抗体(H1N1)(图1C和1D)。这些结果表明,LPSpa的皮下(s.l.)免疫引发了与皮下(s.c.)免疫相当的系统性IgG以及黏膜IgA反应,而这些反应并未由皮下(s.c.)免疫诱导。
图01、季节性流感病毒通过皮下(s.l.)接种LPSpa诱导了血清和黏膜中的HA特异性免疫反应。
结果02
通过皮下(S.I.)接种PR8分裂疫苗与LPSpa保护小鼠免受流感病毒致命挑战
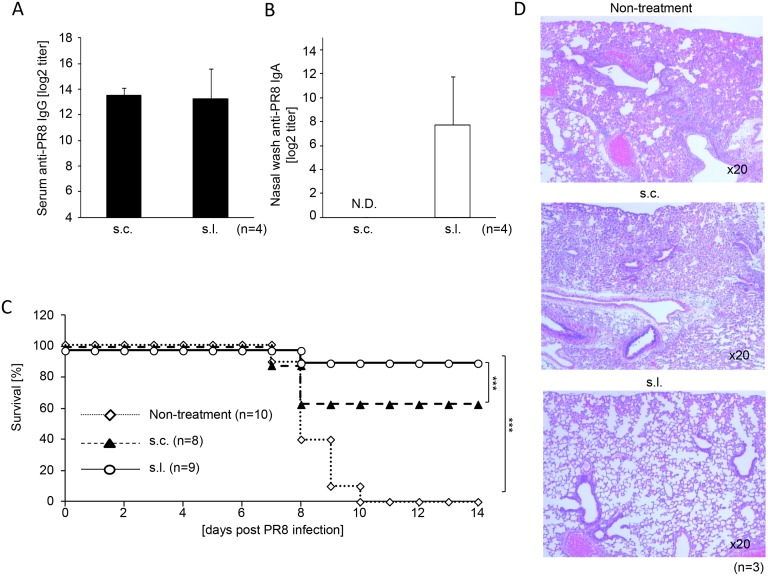
接下来,我们使用了来自PR8(H1N1)株的分裂疫苗和病毒,这是一种常用的实验室小鼠适应性流感病毒株,以确定皮下(s.l.)免疫是否提供了针对致命病毒挑战的保护性免疫。如图2A和2B所示,血清中pr8特异性IgG的充分产生是相当的。而pr8特异性IgA仅由s.l.有效诱导。最后一次免疫后七天,小鼠通过鼻内感染100倍LD50的PR8病毒,并进行日常监测。如图2C所示,所有未治疗的小鼠(10/10)在病毒感染后10天内死亡(其中8只死于病毒感染而未安乐死,2只在第8天体重减轻超过30%,被安乐死并记录为死亡)。然而,约60%(5/8)的皮下(s.c.)免疫小鼠存活下来,尽管观察到暂时的体重下降(数据未显示)。此外,约90%(8/9)的皮下(s.l.)免疫小鼠在没有任何体重下降的情况下存活下来(数据未显示)。在疫苗接种组中,8只中有3只和9只中有1只小鼠未实施安乐死即死于病毒感染。在病毒挑战后第5天,组织学分析显示,未处理小鼠和皮下免疫小鼠的肺切片表现出由大量淋巴细胞浸润和炎性充血引起的严重损伤。相比之下,皮下(s.l.)免疫小鼠的肺切片没有引起显著的肺部病理变化(图2D)。这些结果表明,LPSpa的皮下(s.l.)疫苗接种由于系统性和特别是黏膜PR8特异性抗体的产生,增强了对致命病毒挑战的显著保护反应。
图02、通过皮下(s.l.)接种PR8分裂疫苗与LPSpa可以保护小鼠免受病毒挑战的影响。
结果03
通过皮下(S.I.)接种OVA与LPSpa在远端黏膜表面诱导OVA特异性免疫反应
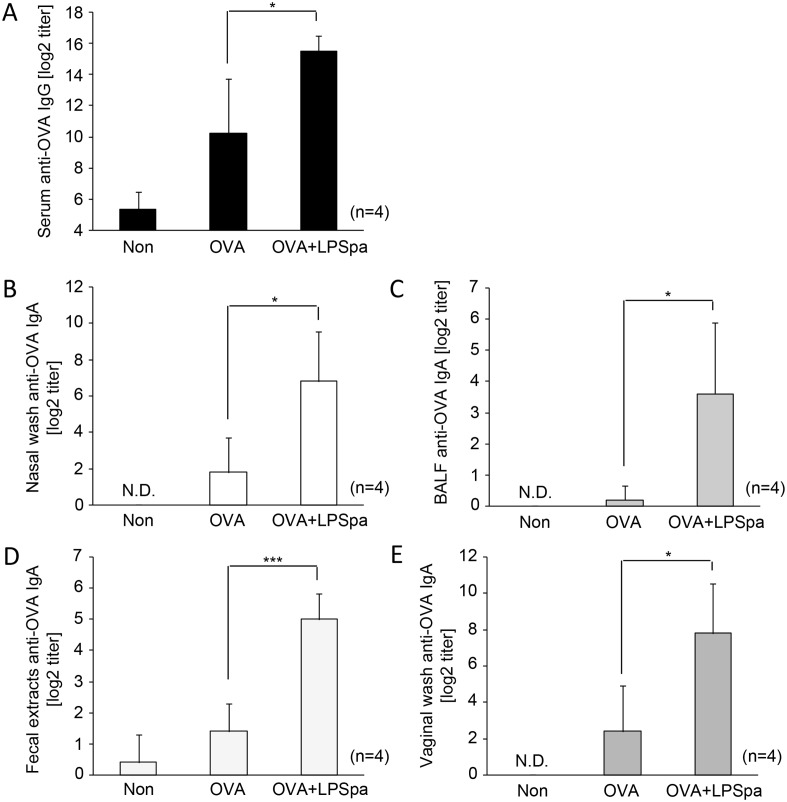
本研究证明了通过口腔黏膜使用LPSpa对流感疫苗进行有效免疫。由于黏膜疫苗接种在免疫部位和远端黏膜表面诱导抗原特异性IgA反应[32],我们使用了OVA,这是一种常用的接种模型抗原,并评估了在含有LPSpa的皮下(s.l.)免疫后在各种黏膜区域OVA特异性IgA的产生。如图3A所示,当免疫包含LPSpa时,血清中OVA特异性IgG的水平显著升高。此外,鼻洗液、BALF、粪便提取物和阴道洗液中的OVA特异性IgA在含有LPSpa的皮下(s.l.)疫苗接种后显著诱导(图3B-3E)。这些结果表明,LPSpa的皮下(s.l.)疫苗接种在气管、肠道和生殖道中引发了系统性IgG和黏膜IgA反应,表明其在防御各种病原体(如诺如病毒、人类免疫缺陷病毒和人类乳头瘤病毒)的疫苗中的潜在应用。
图03、通过LPSpa诱导的OVA特异性IgG和IgA在血清和不同黏膜区域的产生情况。
结果04
通过皮下(S.I.)给予LPSpa在早期阶段激活DC迁移
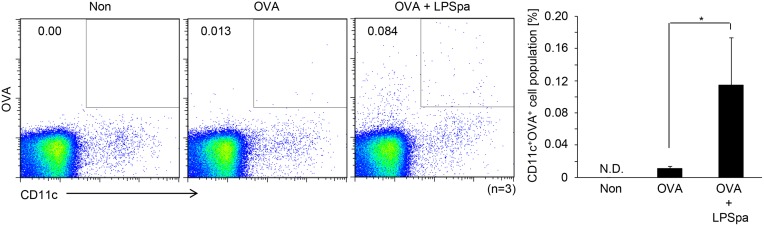
接种疫苗后,先天免疫系统被激活,作为抗原呈递细胞的DC捕获抗原并迁移到邻近的局部淋巴结,在那里它们向T细胞呈递抗原,随后激活适应性免疫系统[30]。为了检验LPSpa是否引发了抗原摄取和DC迁移,我们给予了Alexa 647偶联的OVA(50μg),有或没有LPSpa(5μg),并在18小时后确定了颈部淋巴结中包含OVA的CD11c+DC的比例。如图4所示,在LPSpa存在的情况下,包含OVA的DC数量增加。然而,在所有组的纵隔淋巴结中都很少有包含OVA的DC(数据未显示)。这些结果表明,LPSpa的皮下(s.l.)疫苗接种可以通过皮下(s.l.)途径增强抗原摄取和DC迁移至颈部淋巴结的效率,从而连接先天和适应性免疫。
图04、在LPSpa存在的情况下,颈部淋巴结中树突状细胞(DCs)对抗原(Ag)摄取的增强情况。
结果05
先天免疫细胞在LPSpa通过TLR4刺激后产生细胞因子、增殖和成熟。
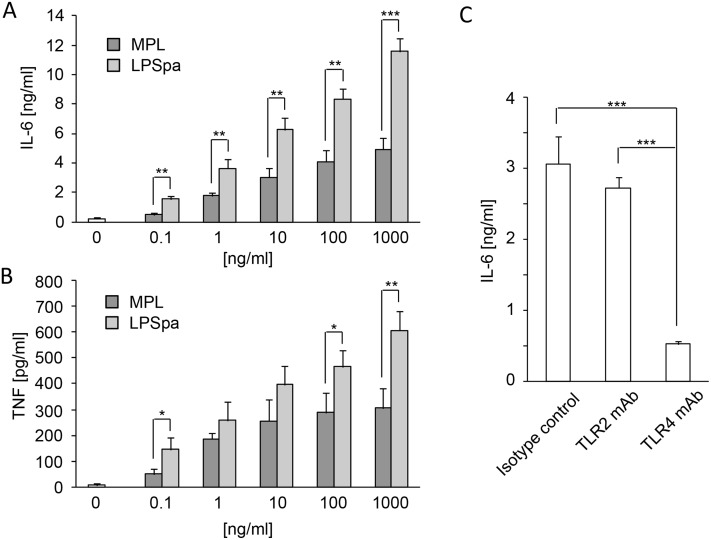
LPSpa是TLR4的配体,由TLRs触发的信号通路导致产生如IL-6、IL-12p40、TNF和I型干扰素(IFNs)等促炎细胞因子[33]。此外,信号通路增加了DCs(树突状细胞)表面共刺激分子的表达,如CD40、CD80和CD86,这些都是细胞激活的标志[34]。我们测量了腹腔巨噬细胞在LPSpa和MPL(另一种作为人类疫苗佐剂批准的TLR4配体)刺激后的反应。如图5A和5B所示,对LPSpa或MPL 24小时的反应中,IL-6和TNF的产生水平随剂量增加而增加,并且在相同浓度下,对LPSpa的反应产生的细胞因子显著高于MPL。为了研究TLR4在LPSpa诱导的细胞因子产生中的作用,腹腔巨噬细胞先用同型对照抗体、TLR2单克隆抗体或TLR4单克隆抗体处理,然后刺激LPSpa。TLR4单克隆抗体预处理严重损害了对LPSpa(1 ng/ml)刺激的IL-6产生(图5C),表明TLR4信号对于LPSpa诱导的细胞因子产生至关重要。
图05、小鼠巨噬细胞在通过TLR4受到LPSpa刺激后细胞因子的产生情况。
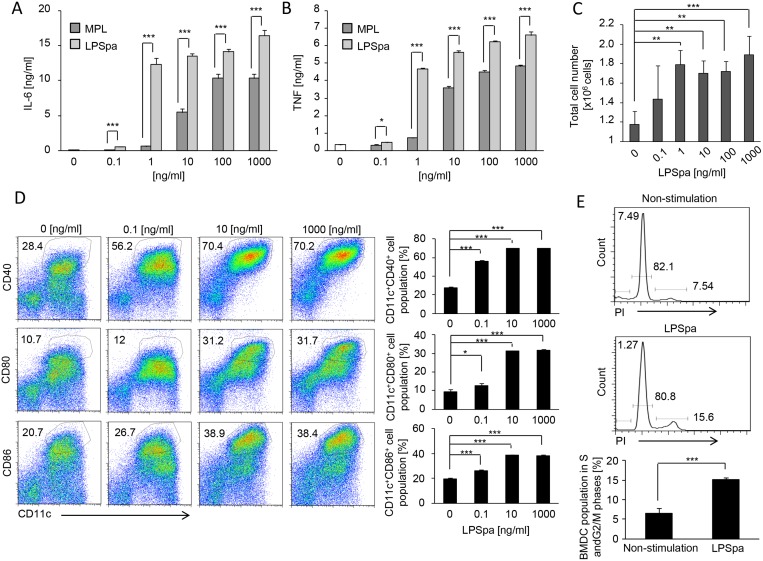
接下来,我们通过在GM-CSF(粒细胞-巨噬细胞集落刺激因子)存在下培养骨髓细胞来生成BMDCs(骨髓来源的树突状细胞)。如图6A和6B所示,对LPSpa刺激的反应中IL-6和TNF的产生也类似于腹腔巨噬细胞。在LPSpa刺激后,表达CD40、CD80和CD86的细胞数量细胞数量增加,且呈剂量依赖性(图6D)。此外,在LPSpa(0.1–1000 ng/ml)存在的情况下,BMDCs的增殖速度比非治疗组快约1.5倍(图6C)。我们检查了LPSpa对BMDCs细胞周期进展的贡献,发现在LPSpa刺激8小时后,处于S期和G2/M期的BMDCs增加(图6E)。综上所述,这些发现表明LPSpa可以激活巨噬细胞和DCs等先天免疫细胞,随后通过TLR4信号通路产生促炎细胞因子、上调共刺激分子并促进增殖。
图6、BMDCs在受到LPSpa刺激后细胞因子的产生、增殖和成熟情况。
免责声明
以上部分内容来源于外网我们重在信息分享,版权归属原作者或原刊发平台所有,如有侵权、信息有误或其他异议,请联系我们,我们将在24小时内删除或整改。
复合免疫 健康活力





























