
IBD治疗新出路:LPS从“肠道公敌”逆袭为“治愈密钥”,如何重塑免疫稳态?
探寻LPS从“引燃炎症”到“重塑稳态”的免疫逆转之谜
当我们谈论困扰数百万人的炎症性肠病(IBD)时,我们通常在谈论一场失控的“炎症风暴”。传统疗法如同不断升级的“灭火器”,虽能暂时压制火势,却难以根治,并可能带来全身免疫抑制的代价。当“消炎”只剩“抑制免疫”这一张王牌,炎症性肠病(IBD)患者被迫在反复发作与全身副作用之间艰难取舍。
但您是否想过,这场风暴的“引信”之一,或许正藏在我们肠道内最丰富的物质——脂多糖(LPS)之中?长久以来,LPS被普遍视为引发强烈炎症的“坏分子”。然而,最新的前沿研究正在彻底颠覆这一认知:
并非所有LPS都是炎症的帮凶。一种独特的“弱激动活性LPS”,非但不会火上浇油,反而能巧妙地“教导”我们的免疫系统恢复冷静与平衡。
最新研究发现,从特定肠道共生菌中提取的这种特殊LPS,能在严重结肠炎小鼠模型中,于短短两周内重建肠道免疫稳态,令所有炎症症状随之消失。它不像强效激动剂那样猛烈刺激,也不像拮抗剂那样完全阻断,而是通过诱导一种特殊的内毒素耐受状态,为过度激活的肠道免疫系统按下“重启键”。
这究竟是如何实现的?这项颠覆性的发现,又将为IBD治疗带来怎样充满希望的新范式?从“敌人”到“良药”,LPS的翻身仗或许正是IBD治疗等待已久的拐点。让我们一起走进这项开创性的研究,探寻从“引燃炎症”到“重塑稳态”的免疫逆转之谜。
弱激动活性的LPS可恢复肠道免疫稳态
由革兰氏阴性菌产生的脂多糖(LPS)是肠道内最丰富且最具免疫调节活性的物质之一。当具有激动活性的LPS与宿主髓系分化-2/Toll样受体4(MD-2/TLR4)受体复合物相互作用会激活核因子kB(NF-kB),进而引发强烈的促炎免疫反应。本研究从常见肠道共生菌普氏拟杆菌mpk(BVMPK)中分离出LPS,该菌株仅表现出微弱的激动活性。这种弱激动活性在实验性结肠炎小鼠模型中可显著缓解炎症免疫反应,与强效激动剂和拮抗剂形成鲜明对比。在这种情况下,给患有严重肠道炎症的小鼠给予BVMPK-LPS,仅需2周即可重建肠道免疫稳态,所有炎症症状随之消失。这种弱激动性LPS的抗炎特性,源于其通过肠道固有层CD11c+细胞中的MD-2/TLR4受体复合物轴,诱导了一种特殊类型的内毒素耐受。因此,弱激动性LPS有望成为治疗肠道免疫系统病理性过度激活相关疾病(如炎症性肠病)的新型潜在制剂。
引言
炎症性肠病(IBD)以慢性、反复发作的肠道炎症为特征,其中克罗恩病(CD)和溃疡性结肠炎(UC)是该疾病综合群中最常见且最具临床意义的两种类型¹。IBD的病因被认为是多因素综合作用的结果,遗传因素²、环境因素³及肠道菌群构成⁴均参与了病理过程。目前人类IBD的治疗主要集中于对症治疗,通常采用免疫抑制疗法⁵。此外,IBD患者需密集医疗干预,使其不仅成为重大健康难题,也构成了日益严峻的经济负担⁶。这种现状凸显了开发新型、低成本且创新的治疗方案的迫切需求。
目前学界普遍认为,肠道微生物群的组成影响着炎症性肠病(IBD)的进展和预后。然而,产生这些菌群效应的并不仅仅是某些特定活体微生物的存在、数量或比例。事实上,在实验性结肠炎小鼠模型中,革兰氏阴性菌脂多糖(LPS)的结构及其内毒素活性,直接决定了炎症反应的最终结果。此外,肠道LPS组的组成结构与多样性,也强烈影响其促炎或维持稳态的特性。这使得LPS成为调控失衡的肠道免疫反应颇具前景的潜在药物靶点。
脂多糖(LPS)的光滑型结构由三个独立结构域组成:(1)O-特异性多糖链(O链);(2)核心寡糖(核心OS);(3)脂质A,该成分将LPS锚定在细菌细胞壁的外层膜上。凭借其高度保守的整体结构与组成,LPS作为重要的微生物相关分子模式(MAMP),通过被宿主髓系分化抗原受体2/Toll样受体4(MD-2/TLR4)受体复合物识别,对宿主先天免疫系统识别细菌入侵起关键作用¹⁰‧¹¹。值得注意的是,LPS的化学结构——尤其是脂质A的详细组成,会显著影响其生物活性:激动型LPS能强烈激活先天免疫系统,而拮抗型LPS则会完全阻断免疫反应¹⁰‧¹²。这种差异体现在不同脂质A结构与MD-2/TLR4受体复合物的多样化结合模式中¹³。
鉴于胃肠道腔内存在大量内源性LPS,哺乳动物宿主必须避免免疫细胞的过度激活。这一目标的实现主要依靠两个关键机制:(1)紧密的肠上皮屏障可保护固有层(LP)中的免疫细胞免受腔内LPS的侵袭;(2)诱导内毒素耐受机制。
内毒素耐受是指抗原呈递细胞因首次LPS刺激导致受体脱敏,从而对第二次LPS(内毒素)刺激产生低反应性的表型。尽管这一现象已得到充分证实,但其分子机制仍未完全阐明。该现象在体外实验、动物模型及人体中均有观察到。具有内毒素耐受性的细胞表现为,无法在二次LPS刺激下表达和分泌促炎细胞因子,如白细胞介素(IL)-12、IL-6和IL-1β。不过,耐受基因的具体表达模式因细胞类型而异。值得注意的是,在内毒素耐受过程中,不仅细胞因子表达量大幅降低,T细胞激活分子(如主要组织相容性复合体II类分子和CD40.17分子)的表面表达也显著减少。
内毒素耐受的建立过程,伴随着LPS刺激的抗原呈递细胞经历成熟阶段——其特征是促炎细胞因子和MHC II类分子表面表达上调。然而,所谓“半成熟”细胞虽对二次LPS刺激表现出耐受性,却无法针对首次诱导半成熟的刺激产生促炎细胞因子。例如,已有充分研究证实的小鼠肠道共生菌Bacteroides vulgatus mpk(BVMPK)能在肠道固有层中诱导产生半成熟CD11c+细胞,这种机制被认为有助于该菌株的免疫调节特性,从而在多种实验性结肠炎小鼠模型中预防结肠炎的发生。BVMPK属于拟杆菌门,该菌门是哺乳动物肠道中最丰富的革兰氏阴性菌门。值得注意的是,不仅BVMPK,其他拟杆菌属物种如脆弱拟杆菌(BF)也具有有益的、能调节宿主免疫系统的特性。在此背景下,BF尤其值得关注,因为其优势特性已被证实源于一种结构成分——两性离子多糖A(PSA)。
本研究证实,BVMPK能显著缓解小鼠已形成的肠道炎症,并使受损的肠组织完全修复愈合。值得注意的是,发挥这一作用的并非PSA,而是另一种结构成分——LPS同样展现出类似疗效。研究发现,BVMPK来源的LPS(BVMPK-LPS)在与宿主MD-2/TLR4受体复合物相互作用时表现出弱激动活性,且纯化的BVMPK-LPS能在实验性结肠炎小鼠模型中重建肠道免疫稳态。这种LPS的弱激动特性被认为是通过诱导固有层半成熟 CD11c⁺ 细胞,从而主动缓解炎症的关键机制。因此,弱激动型LPS或将成为治疗炎症性肠病(如IBD)等肠道炎症性疾病的新型有效治疗剂。
结果
经无创体内PET成像证实:BVMPK可有效改善实验性结肠炎小鼠模型中已形成的炎症反应
我们既往研究已证实,小鼠肠道共生菌BVMPK在多种实验性结肠炎模型中均具有抗炎特性(20-22)。这些抗炎特性在疾病发生前施用BVMPK时尤为显著,可有效预防微生物群介导的肠道炎症。这一发现促使我们进一步验证:在已形成炎症的环境中,该共生菌是否仍能发挥抗炎效果。为构建长期慢性炎症模型,我们选用Rag1缺陷小鼠的T细胞移植模型(25),采用无法表达功能性T、B细胞的Rag1基因缺陷小鼠(26)。移植初始CD4+ T细胞后,这些Rag1⁻/⁻小鼠会发展出依赖微生物群组成高度相关的慢性肠道炎症(27)。
因此,我们将携带高度失调菌群(DYSM)7的Rag1小鼠与5×10⁵个初始野生型(WT)CD4⁺CD62L⁺CD45Rbʰⁱ T细胞进行移植。菌群组成详见“材料与方法”部分。在T细胞移植4周后,给小鼠持续饮用含5×10⁸ CFU/mL活BVMPK的饮用水,直至实验结束。含BVMPK的饮用水每2天更换一次,由于厌氧菌具有耐氧特性,这些条件下仍能保持活性(数据未显示)。未处理的Rag1⁻/⁻小鼠作为阴性对照,未接受BVMPK处理的T细胞移植小鼠作为阳性对照(图1A)。
图1. 经无创体内PET成像证实:活体B. vulgatus mpk给药可减轻Rag1–/–小鼠已形成的结肠炎症
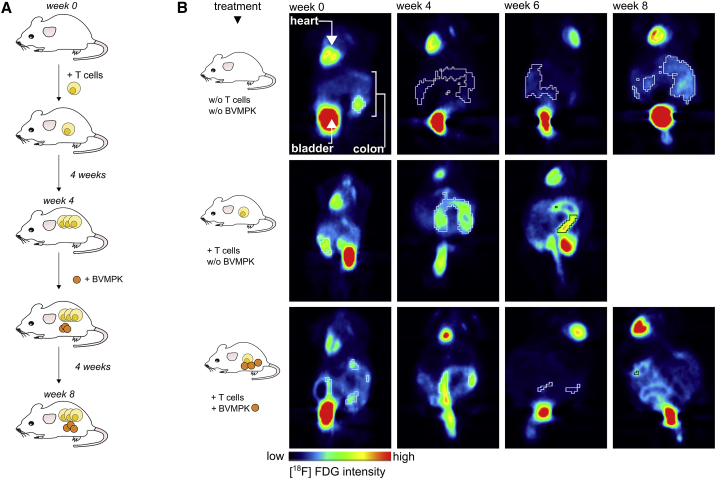
为实时监测各受试小鼠肠道炎症的进展,我们为所有实验小鼠注射了¹⁸F-氟代脱氧葡萄糖(¹⁸F-FDG),并实施无创体内正电子发射断层扫描(PET)。¹⁸F-FDG适用于活体动物炎症过程的检测,因为PET扫描中炎症部位会呈现比非炎症周边区域更高的¹⁸F-FDG摄取量(28)。但需注意,心脏和膀胱等器官通常会呈现基础水平的示踪剂摄取信号,这与它们的炎症状态无关。我们持续监测了本次实验所有小鼠结肠的¹⁸F-FDG摄取动态:在每个监测时间点(T细胞移植当天(第0周)及移植后第4、6、8周),对每只小鼠注射¹⁸F-FDG后进行PET成像(图1B)。鉴于¹⁸F的半衰期特性,所获数据均经过衰变校正,并按每只动物的注射活度进行标准化处理。
如图1B上图所示,未移植T细胞的Rag1⁻/⁻小鼠在整个观察期间均呈现较低的¹⁸F-FDG摄取,表明其结肠内未发生炎症进程。与既往研究一致[7,22],携带DYSM并接受初始T细胞移植的Rag1⁻/⁻小鼠出现严重结肠炎症,具体表现为第4周和第6周结肠区域的高¹⁸F-FDG摄取(图1B中图)。由于这些动物的炎症程度已超出伦理允许范围,故在第6周实施安乐死。第三组小鼠(图1B下图)在T细胞移植后第4周出现严重肠道炎症表现,随即通过饮用水投喂活BVMPK直至第8周。结果显示,该组小鼠在治疗2周后结肠¹⁸F-FDG摄取即显著降低,第8周的PET扫描显示其摄取水平已降至正常水平,这表明第4周可见的炎症已被BVMPK干预清除。PET结果进一步通过组织学评分降低和IL-17表达减少得到验证:与单纯移植T细胞的Rag1⁻/⁻小鼠相比,BVMPK喂养的T细胞移植Rag1⁻/⁻小鼠呈现更优的病理指标(图4B-4D)。
图4.在Rag1⁻/⁻小鼠模型中,分离自B. vulgatus mpk- LPS与活菌同样具备缓解已形成结肠炎症的能力。
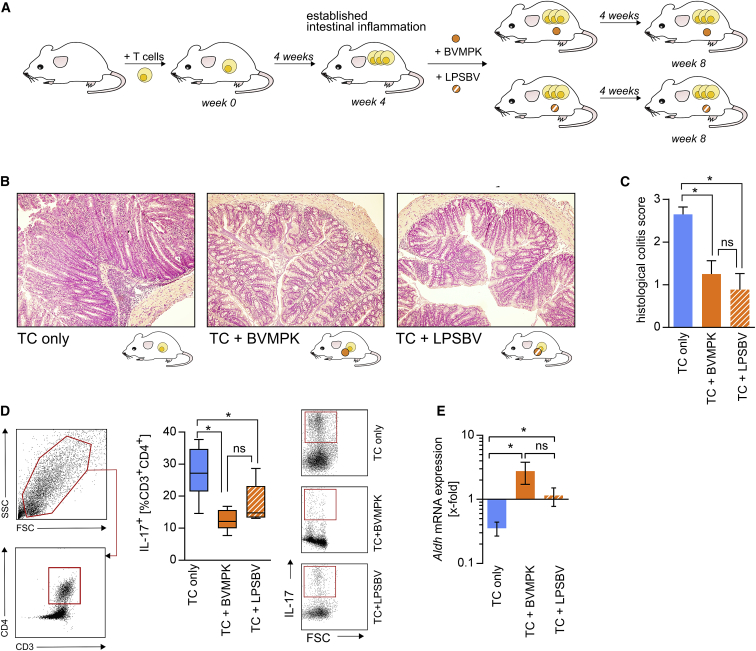
这清楚地表明,共生菌BVMPK的抗炎特性不仅能预防T细胞移植Rag1⁻/⁻小鼠的炎症诱发(如先前文献22所述),更能够主动改善已形成的结肠炎症,有效缓解该小鼠模型的结肠炎症状。
诱导CD11c⁺细胞呈低反应性是多种Bacteroides菌共有的特征
我们已证实,BVMPK 对肠道炎症的抑制作用与诱导固有层(LP)CD11c⁺ 细胞呈现低反应性(即所谓“半成熟”)表型密切相关(7,22)。我们推测,正是这种低反应性 LP CD11c⁺ 细胞在实验性结肠炎模型中发挥了预防及减轻炎症的作用。鉴于 Bacteroidetes 是人类肠道中占主导地位的革兰阴性菌门(29,30),我们进一步探究了除BVMPK外的其他 Bacteroides 菌种——包括B. dorei(BD)、B. vulgatus ATCC8482(BV8482)、B. fragilis(BF)和 B. thetaiotaomicron(BTIO)——是否同样具备诱导半成熟表型的能力。
已有研究表明,BVMPK 能在体外诱导骨髓来源树突状细胞(BMDC)进入“半成熟”状态:其特征为 IL-6 分泌量虽低但可检测,同时不分泌其他促炎细胞因子(如肿瘤坏死因子TNF、IL-12和IL-1b),且不产生抗炎因子IL-10(22,31)。同时,半成熟BMDCs(smBMDCs)仅轻微上调MHC II类分子及CD40、CD80、CD86等表面标志物的表达(22,31)。此外,LP CD11c⁺ 细胞与 BMDC 表型高度相似,均表达 CD45、CD11b、CD103,且 CD3、Ly6G、Ly6C、CD45R、CD64 均为阴性(图 S1)。因此,我们选用BMDC作为模型,以验证检测除 BVMPK 外的其他 Bacteroides 菌株是否也能诱导 CD11c⁺ 细胞出现低反应性。
BMDCs取自野生型C57BL/6小鼠的骨髓,以PBS(模拟处理)作为阴性对照,同时采用BVMPK、BD、BF、BV8482和BTIO进行16小时刺激。大肠杆菌mpk(EC)作为阳性对照用于诱导完全成熟的BMDCs(22)。所有细菌均以1的感染复数(MOI)加入BMDCs培养体系。研究数据显示:所有受试Bacteroides菌株在BMDCs中诱导了相似效应,其表现特征为IL-6低分泌、IL-10与TNF缺失、MHC II类分子和CD40表面表达仅轻微上调,这些效应与BVMPK诱导的结果相当,表明所有测试拟杆菌菌株均诱导了BMDCs的半成熟状态(图2A和图S2)。如预期所示,EC刺激可显著促进IL-6、IL-10和白细胞介素-1β(TNF)的分泌,并明显提升了MHC II类分子和CD40的表面表达水平。
图2. 诱导低应答性CD11c+细胞是多种拟杆菌属的共同特征
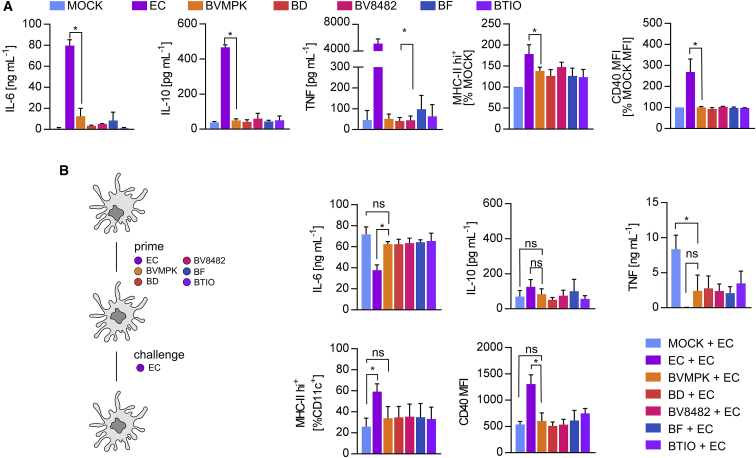
BVMPK诱导的半成熟(sm)CD11c+细胞有一个典型特征:在面对后续细菌刺激时,其在MHC II类分子、CD40、CD80及CD86的表达水平以及细胞因子(如TNF)分泌呈现低反应性,但白细胞介素-6(IL-6)分泌未受影响。因此,我们先用BVMPK、BD、BV8482、BF、BTIO或EC对BMDCs进行24小时预处理,再用EC进行二次刺激。值得注意的是,在预处理与二次刺激之间更换了培养基,以验证预处理细胞是否仍能对EC刺激产生促炎细胞因子分泌。如图2B所示,与未预处理的EC刺激BMDCs相比,经Bacteroides预处理再接受EC刺激的BMDCs其IL-6分泌并未减少。所有不同刺激组合中,IL-10分泌水平普遍偏低。然而,与未预处理的BMDCs相比,所有受试Bacteroides菌株预处理均使BMDCs在EC刺激后对 TNF 表达产生耐受性。与此一致的是,经Bacteroides预处理的BMDCs在EC二次刺激后,其MHC II类和CD40表面表达水平均显著低于EC预处理组。这些结果表明,所有受试Bacteroides菌种均能诱导BMDCs进入半成熟状态,从而对TNF及T细胞激活分子表达产生耐受性。由此可见,诱导smBMDCs并非BVMPK独有的特性。
Bacteroides菌种共享保守的脂质A合成核心
由于使用热灭活的 BVMPK 、BD、BF、BV8482和BTIO进行刺激同样能像活菌一样诱导BMDC半成熟状态(图S3),我们推测关键的起半成熟诱导作用的细菌因子是这些菌株共有的结构成分。Bacteroides属于革兰氏阴性菌,其细胞壁外膜中含有LPS。众所周知,LPS是革兰氏阴性菌中最具活性的表面分子之一,也是诱导树突状细胞(DC)成熟的重要成分。它由脂质A、核心寡糖以及由不同长度多糖组成的O抗原构成。acobson等人(32)近期研究发现BF、BV8482、BD和 BTIO 在多糖与寡糖部分存在差异。鉴于本实验中所有菌株均能诱导半成熟状态(图2),我们推测半成熟的诱导过程与LPS碳水化合物部分无关。因此,我们将研究重点放在脂质A部分。已有研究报道,BD和BF的脂质A在结构和组成上相似,均为单磷酸化状态且仅含有5条酰基链(33,34)。
表1. BVMPK 与BV8482、BD及 BTIO 之间脂质A核心合成基因的比较
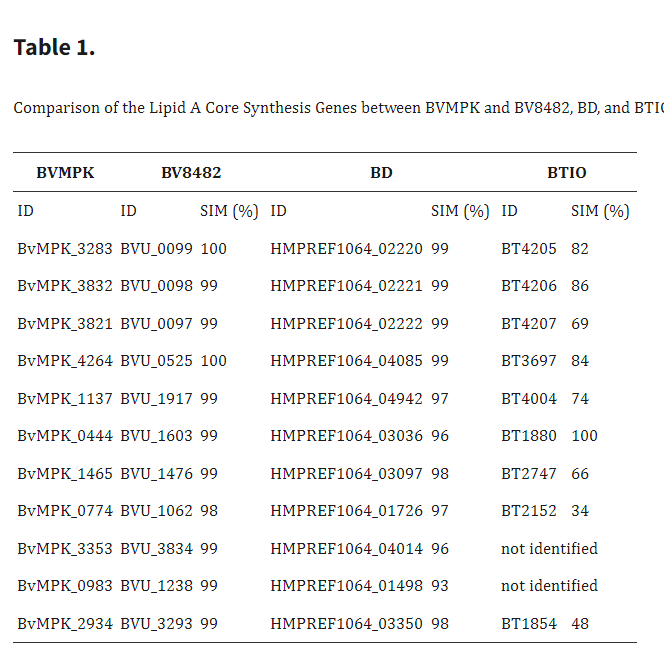
表2. BVMPK与EC MG1655之间脂质A核心合成基因的比较
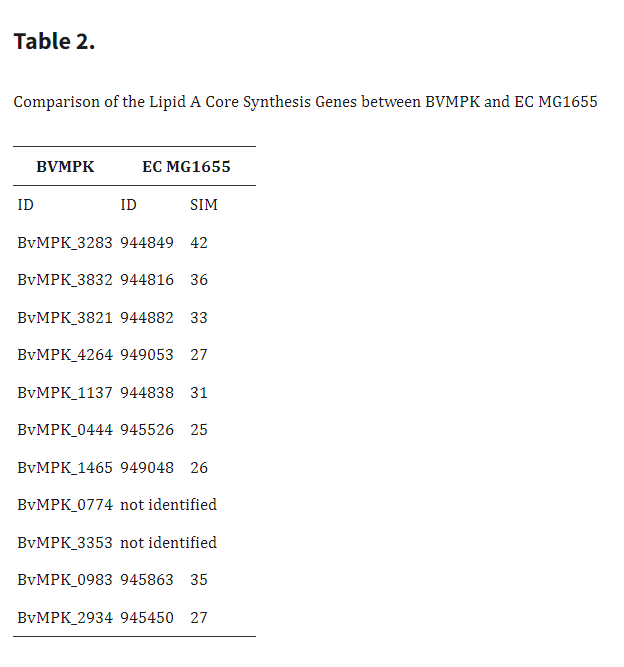
为筛选参与Bacteroides脂质A合成的候选基因,我们以BVMPK的基因为参照,对BV8482、BD和BTIO的基因组进行BLASTP比对。结果显示,所有受试Bacteroides spp.的脂质A合成基因高度同源:除BTIO个别基因外,序列相似度均超过90 %(表1)。随后,我们将BVMPK的脂质A合成基因与EC的Raetz途径进行比对(表2),发现二者差异显著:基因相似度仅在25%-42%之间,且EC基因组缺失BVMPK_0774和BVMPK_3353两基因。这些差异可能导致脂质A组成不同。BVMPK、BD、BTIO与BV8482在脂质A核心区域中观察到的基因同源性,支持了我们的假设——所有受试Bacteroides spp.对树突状细胞的免疫效应由其典型的LPS介导;而EC产生不同类型的LPS,因而诱导出截然不同的效应。总体而言,这表明拟杆菌属LPS的结构是诱导CD11c+细胞半成熟状态的关键决定因素。目前我们扔在持续解析BVMPK来源LPS(LPSBV)化学结构及其构效关系。
BVMPK分离的LPS诱导低反应性半成熟CD11c+细胞
为了验证“拟杆菌属LPS对诱导低反应性CD11c+细胞至关重要”这一假设,我们分别从BVMPK和EC(LPSEC)中分离出LPS。EC含有一种强激动性的双磷酸化、六酰化脂质A。我们利用C57BL/6野生型小鼠骨髓来源的树突状细胞(BMDCs),以MOI为1的条件,分别用活的BVMPK或EC刺激这些细胞。此外,我们还用纯化的LPSBV或LPSEC刺激BMDCs,浓度为每10⁶个BMDCs中加入50 ng LPS,刺激总时长为16小时。如图3A所示,用LPS刺激BMDCs产生的细胞凋亡表型(BMDC)与使用相应细菌来源的LPS刺激产生的表型一致。无论是 BVMPK 还是 LPSBV 刺激,均导致MHC II类分子、CD40、CD80和CD86的表达水平较低(图3A),同时IL-6分泌量减少且未检测到 TNF(图3A)。相反,用EC或LPSEC刺激BMDCs均能显著提升MHC II类分子及T细胞共刺激分子CD40、CD80和CD86的表面表达,并显著促进了IL-6和TNF的分泌(图3A)。
图3. BVMPK分离的LPS可诱导低反应性半成熟CD11c+细胞
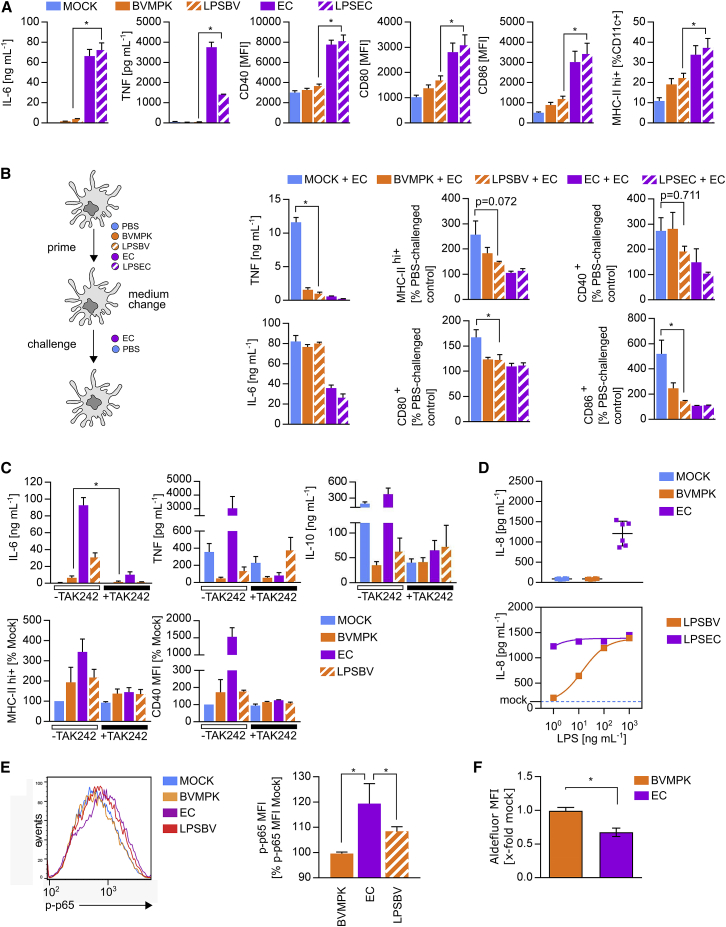
为评估细胞对二次刺激的低反应性,我们分别用PBS(模拟对照)、BVMPK、LPSBV、EC及LPSEC对BMDCs进行24小时预刺激,随后用EC或PBS作为阴性对照进行二次攻击。关键在于,我们在预刺激和挑战阶段更换了培养基,以确定预刺激细胞是否仍能具备响应EC攻击而分泌促炎细胞因子的能力。通过检测预刺激并经EC攻击的BMDCs中MHC II类分子高表达阳性(MHC class IIhi+)、CD40+、CD80+及CD86+细胞的比例,并与相同预刺激条件下PBS对照组比较,我们评估了T细胞共刺激分子表面表达对EC攻击的响应变化。因此,图中高柱形表示高反应性,低柱形则代表免疫耐受(图3B)。如图3B所示,经BVMPK或LPSBV预刺激再接受EC攻击的BMDCs,其TNF分泌量均显著降低。更重要的是,与PBS预刺激组相比,经LPSBV预刺激的BMDCs在EC攻击后,其CD80和CD86表面表达量的增幅显著降低,这表明LPSBV预刺激细胞在T细胞活化分子表面表达方面出现了低反应性。正如预期,EC和LPSEC预刺激则能引发DC的完全成熟。
为验证LPSBV与BVMPK诱导BMDCs半成熟效应的机制是否源于LPS依赖的TLR4信号通路,我们在用LPSBV、BVMPK及EC刺激前,先用竞争性TLR4拮抗剂TAK242对BMDCs进行1小时预处理(图S4),随后进行16小时刺激(图3C)。结果显示,TAK242预处理完全抑制了所有刺激物引发的细胞因子分泌,并阻断了MHC II类分子和CD40表面表达的调控。因此,我们得出结论:(1)BVMPK主要通过其LPS诱导BMDCs发生半成熟;(2)纯化的LPSBV足以诱导产生低反应性半成熟BMDCs。
TAK242被报道为一种选择性TLR4拮抗剂(35,36),我们的对照实验也证实TAK242可抑制TLR4信号通路,而不影响TLR2信号传导。然而,我们尚不能完全排除TAK242可能对其他信号通路产生潜在影响。
LPS 诱导的TLR4信号会激活核因子 κB(NF-κB),进而调控促炎与抗炎细胞因子的表达。由于BVMPK、EC以及LPSBV通过TLR4信号通路诱导不同的细胞因子分泌模式,我们比较了 BVMPK 与 EC、LPSBV与 LPSEC在激活NF-κB方面的潜能。为此,我们选用表达小鼠MD-2/TLR4受体复合体(mTLR4-HEK)的HEK细胞(图3D),并对其进行16小时刺激。通过检测IL-8分泌量间接评估MD-2/TLR4介导的NF -kB活化程度,因为IL-8分泌是TLR4介导的 NF -kB激活的直接结果(37)。实验显示,当以MOI=1的活菌刺激时,EC组IL-8分泌显著高于BVMPK组(图 3D,上图)。使用分离的LPSBV或LPSEC刺激时,在使用LPSBV的情况下,IL-8分泌量呈现浓度依赖性增加。而即使在浓度低至1 ng·mL⁻¹,LPSEC仍能诱导IL-8分泌达到饱和水平(图 3D,下图)。这种通过NF-κB活化(37)增强的IL-8分泌表明,在mTLR4-HEK细胞中LPSEC的激活能力显著强于LPSBV。此外,我们通过流式细胞术检测了小鼠BMDCs中p65 NF -kB亚基S534位点的磷酸化水平(p-p65),以此评估其转录激活活性(38,39)。结果显示,与EC刺激相比,使用BVMPK和LPSBV刺激BMDCs 30分钟后,p-p65的诱导水平显著低于EC刺激组(图3E)。
此外,我们还检测了经活体BVMPK或EC刺激16小时的小鼠BMDCs细胞内醛脱氢酶(ALDH)活性(图3F和图S5)。ALDH通过将维生素A衍生物视黄醇代谢为视黄酸(RA),进而诱导具有炎症缓解作用的Foxp3⁺ 调节性T细胞(Treg)(40)。研究证实RA是诱导Treg的关键介质,而ALDH⁺肠道树突状细胞被认为是维持免疫稳态的重要调控介质(19,41,42)。与EC刺激相比,BVMPK刺激的BMDCs表现出显著更高的ALDH活性,这表明其具有更强的Treg诱导潜能。
众所周知,LPS是MD-2/TLR4受体复合物的强激动剂。然而有研究报道,某些特殊结构的LPS(如幽门螺杆菌LPS)(43)也能激活TLR2信号通路,而牙龈卟啉单胞菌LPS激活TLR2的能力仍存在争议,可能是脂蛋白污染导致的实验假象(44)。这些发现引发双重疑问:一是TLR2信号是否参与LPSBV介导的CD11c+细胞免疫效应?二是所用LPSBV制剂是否存在潜在污染,进而可能激活TLR2受体?关于潜在污染物,除脂蛋白外,荚膜多糖的存在也需考虑。在纯化过程中,我们已通过超速离心步骤去除LPSBV制剂中的荚膜多糖。尽管如此,仍需验证溶解态LPSBV 制剂是否诱导TLR2信号——因为来自革兰氏阴性菌的两种潜在污染物(荚膜多糖45-48和脂蛋白49-51)均会导致TLR2受体激活(图S6)。实验数据显示,与TLR2缺陷型BMDCs相比,LPSBV刺激的野生型BMDCs仅表现出微量IL-6差异,表明LPSBV对TLR2存在微弱激活作用(图S6A)。然而,通过使用TLR2/BMDCs模型,我们排除了TLR2信号通路在诱导低反应性半成熟BMDCs中的贡献(图S6B)。因此,我们得出结论:LPSBV通过激活MD-2/TLR4受体信号(而非TLR2信号)在诱导BMDC半成熟过程中发挥关键作用。
综合这些结果表明,与 LPSEC 相比, LPSBV 对MD-2/TLR4受体的激活作用显著较弱,导致其诱导的NF -kB转录活性降低。但值得注意的是,与MD-2/TLR4拮抗剂的作用机制不同, LPSBV能主动诱导BMDCs进入低反应性半成熟状态,且未引发促炎细胞因子的表达。因此,我们认为LPSBV更应被归类为弱激动剂而非拮抗剂。
纯化LPSBV调控可减轻实验性结肠炎小鼠模型已建立的肠道炎症
基于以下发现:
(1) 弱激动剂 LPSBV在BMDCs中诱导半成熟的能力与活菌BVMPK相同;
(2) BVMPK在Rag1⁻/⁻小鼠中预防肠道炎症的效应与诱导半成熟固有层CD11c⁺细胞相关。
我们进一步探究验证:单独给予LPSBV是否也能在T细胞重建的Rag1⁻/⁻ 模型中发挥同等的抗炎效果。为此,我们选用已存在严重菌群失调(DYSM)的 Rag1⁻/⁻ 小鼠,并通过移植5×10⁵个初始WT CD4⁺CD62L⁺CD45RBʰⁱ T细胞以诱发结肠炎症。第4周时,受体小鼠小鼠出现便血和腹泻等明显结肠炎症状,这与监测肠道炎症的PET影像结果一致(图1B)。此后,我们开始连续4周在饮用水中添加活BVMPK(5 × 10⁸ CFU/mL)和纯化LPSBV(160 μg·mL⁻¹)(图 4A)。研究显示,携带C57BL/6遗传背景的小鼠(如Rag1⁻/⁻)每日饮水量约为6 mL(52),据此估算每只小鼠每日 LPSBV 摄入量约为1 mg。
图4B展示了实验结束时各组结肠切片的代表性H&E染色结果。如预期所示,未接受治疗的T细胞移植组动物出现严重结肠炎症(图4B,左图)。然而,与未治疗小鼠相比,接受LPSBV和BVMPK治疗组动物的肠道炎症显著减轻(图4B中图和右图,图4C)。从活BVMPK治疗的Rag1⁻/⁻小鼠结肠固有层(cLP)中分离的CD3⁺CD4⁺ T细胞,其IL-17表达量显著降低(图4D),这表明Th17反应明显减弱(53),这一现象对诱导该小鼠模型的结肠炎发病机制中起着关键作用。
此外,对结肠刮取物进行的qRT-PCR检测显示,经活BVMPK处理的动物体内ALDH mRNA的表达量显著升高(图4E),这支持了我们在体外实验中的发现,即接触过BVMPK的抗原呈递细胞具有更强的诱导调节性T细胞(Treg)的能力(图3F)。
经LPSBV处理的T细胞移植Rag1⁻/⁻小鼠,其结肠固有层(cLP)中表达IL-17的CD3⁺CD4⁺ cLP T细胞比例显著降低,同时结肠刮取物中Aldh mRNA表达水平升高。这些数据表明,无论是活BVMPK还是分离的LPSBV,都能通过下调促进Th17免疫反应的细胞因子,并创造有利于调节性Treg诱导的环境条件,从而有效地缓解改善大肠中已形成的炎症反应。
弱激动剂LPSBV并非强激动剂LPS的竞争性抑制剂
在使用Rag1⁻/⁻小鼠进行的体内实验所得结果引出一个问题:PSBV是否作为MD-2/TLR4受体复合物结合位点的竞争性抑制剂,从而阻止激动性LPS的结合,并抑制具有促炎免疫反应特征的CD11c⁺细胞完全成熟。首先,我们旨在测定并比较LPSBV与原型激动性LPSEC对小鼠MD-2/TLR4受体复合物的结合常数。为此,我们建立了光学滴定体系,利用生物素化的LPSBV(bioLPSBV)来获取测定LPSBV和LPSEC的准解离常数(KD)。此前研究已证实,bioLPSBV仍能同样激活小鼠MD-2/TLR4受体复合物(图S7),这表明生物素化修饰并未影响LPSBV的结合特性。
我们清楚地认识到,由于所使用的LPS溶液精确摩尔浓度未知,我们无法测定真实的KD值。两亲性LPS单体组装成胶束、囊泡甚至更复杂的结构,其过程高度依赖缓冲液和离子强度,因此难以预测。这加剧了LPS单体有效摩尔浓度测定的难度——只有那些能接触受体的单体才构成活性配体,从而影响KD值的计算。然而基于以下假设:(1) bioLPSBV与LPSEC的单体分子量相近;(2) 在实验条件下二者化学行为相似;(3)所有实验均采用同时孵育两种LPS的方式,我们可以认为,用g L⁻¹而非mol L⁻¹为单位的KD值进行定性比较,能够合理评估二者结合亲和力。最终,我们测得LPSBV的准KD为0.412 g L⁻¹,LPSEC为0.304 g L⁻¹(图5A,光学滴定细节见图S8)。这些数据表明:LPSBV与LPSEC对小鼠MD-2/TLR4受体复合物具有相似的结合亲和力。
图5. 弱激动性LPSBV并非强激动性LPS的竞争性抑制剂
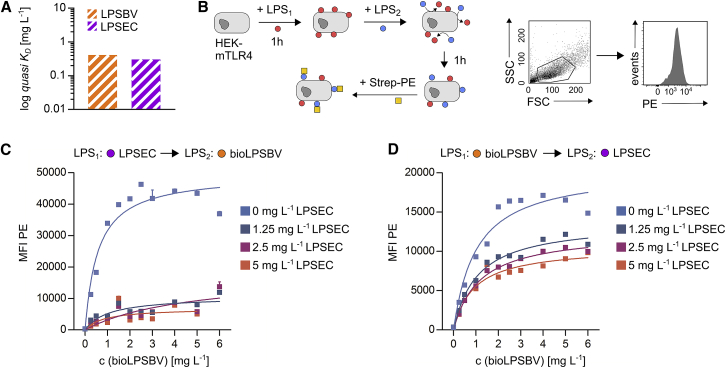
接下来,我们测试了这两种不同LPS(脂多糖)从受体复合物中移除已结合LPS的能力。具体操作是:先将mTLR4- HEK细胞分别与不同浓度的bioLPSBV或 LPSEC 共孵育1小时,随后再以不同浓度加入另一种LPS继续孵育1小时。接着通过添加藻红蛋白(PE)标记的链霉亲和素(Strep-PE)进行二次孵育,利用流式细胞术对细胞结合的bioLPSBV进行可视化检测(图5B)。实验发现:先使用LPSEC预孵育再用bioLPSBV处理时,检测到PE荧光强度始终维持在较低水平,且与所用LPSEC和bioLPSBV的浓度关系不大(图5C)。这表明,当小鼠MD-2/TLR4受体复合物被LPSEC结合后,bioLPSBV无法取代其受体结合位点。即使LPSEC的浓度低至1.25 mg L⁻¹,也能使PE信号降低至未用LPSEC预处理时的约20%(图5C)。相反,若先使用bioLPSBV预孵育细胞再加入LPSEC,则即使低浓度的LPSEC也能使PE信号(仅来源于结合的bioLPSBV)显著降低约50%(图5D)。由于我们假设检测到的PE荧光强度与结合的bioLPSBV含量成正比,因此可以得出结论:bioLPSBV仅能置换约20%的已结合LPSEC(图5C),而LPSEC可置换约50%的已结合bioLPSBV(图5D)。
我们已证实LPSBV能够在体外诱导耐受性半成熟BMDCs(图3),并在携带复杂微生物群的T细胞移植Rag1⁻/⁻小鼠中减轻已形成的肠道炎症(图4)。然而,迄今为止所有体外研究 smBMDCs的实验,在半成熟过程的前16小时内均未加入其他LPS结构的条件下进行。而在生理条件下,结肠腔内同时存在大量不同种类的共生LPS。为此,我们采用弱激动型LPSBV与原型激动型LPSEC同时以不同浓度刺激BMDCs 16小时(图6A),以探究在强MD-2/TLR4受体复合物激动剂存在的情况下,LPSBV是否仍能诱导半成熟状态。通过检测促炎细胞因子分泌以及MHC II类分子与TLR4的表面表达,我们验证了这一机制。
图6. LPSEC 诱导的 BMDC 成熟无法通过体外同时存在LPSBV来预测
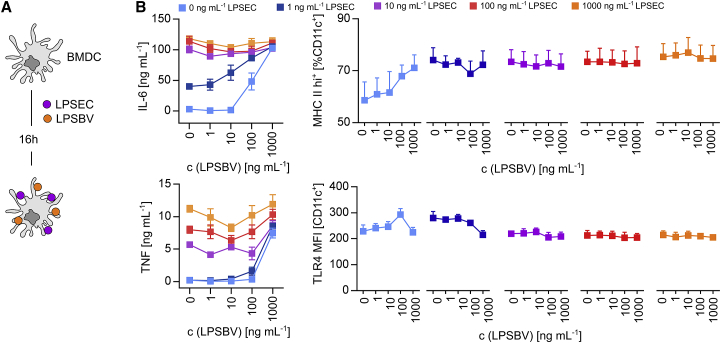
我们在未添加LPSEC的情况下, 检测到LPSBV对BMDCs的刺激呈现浓度依赖性效应(图6B中浅蓝色线条)。当LPSBV浓度达到100 ng mL⁻¹(即50 ng/10⁶ BMDCs)时可诱导半成熟BMDC表型;这与图3研究结果一致。而使用1,000 ng mL⁻¹或500 ng纯化LPSBV/10⁶细胞时,则通过高水平的TNF、IL-6和MHC II类分子表面表达表明BMDCs被强烈激活(图6B)。这进一步印证了LPSBV并非MD-2/TLR4受体复合物拮抗剂,而是一种弱激动剂,其总体浓度决定了最终的内毒素活性。当在LPSBV刺激基础上加入激动剂LPSEC后,所有浓度组的促炎细胞因子分泌率(图6B)及MHC II类分子表达(图6B)均显著增强,表明LPSBV的共存并不能阻断LPSEC诱导的成熟效应。出乎意料的是,在所有不同刺激条件的BMDCs中,细胞表面TLR4表达始终保持相对稳定(图6B),说明这两种LPS结构与MD-2/TLR4受体复合物结合后未引发显著的TLR4内吞现象,该发现与先前报道的其他肠道共生源LPS的作用机制相悖⁵⁴。
上述结果表明,当BMDCs同时接触弱激动剂LPSBV和强激动剂LPSEC时,会抑制LPSBV诱导的半成熟化进程。然而,在菌群复杂的小鼠体内,LPSBV却能减轻肠道炎症。由于LPSBV诱导CD11c⁺细胞半成熟可能是其体内抗炎效应的作用机制,我们进一步探究了 LPSBV 与内源性LPS及复杂菌群中其他微生物成分竞争的情况下,如何影响CD11c+细胞表型。为此,我们用WT C57BL/6小鼠制备BMDCs,并按前述方法用分离的LPSBV进行刺激。同时,添加经高压灭菌的粪便样本。该粪便取自T细胞移植后4周、已发生严重肠道炎症的 Rag1⁻/⁻ 小鼠(图 1B),因此代表肠道炎症状态下形成的菌群失调(DYSM)。DYSM包含多种内源性 LPS,可与LPSBV竞争结合LP CD11c⁺细胞表面的MD-2/TLR4受体位点,并含有其他免疫调节成分;同时,该DYSM正是LPSBV在炎症 Rag1⁻/⁻ 小鼠中发挥抗炎作用时所面对的菌群组成。实验显示:DYSM单独刺激BMDCs可轻微提升促炎细胞因子和T细胞共刺激分子的分泌水平,但未达统计学显著性(图7A)。这表明在所选浓度下,DYSM虽能影响CD11c⁺细胞成熟,但作用强度弱于含激动性LPSEC的阳性对照(图S9)。有趣的是,当DYSM与LPSBV联合刺激时,IL-6 和 TNF 的分泌量以及 MHC II 类分子和CD40的表面表达均显著高于任一单独刺激,表明二者协同促进了BMDCs 的激活。
图7. LPSBV介导的BMDC耐受性在缺乏激动性LPS的条件下被诱导,从而保护机体免受对失调菌群组成的促炎反应。
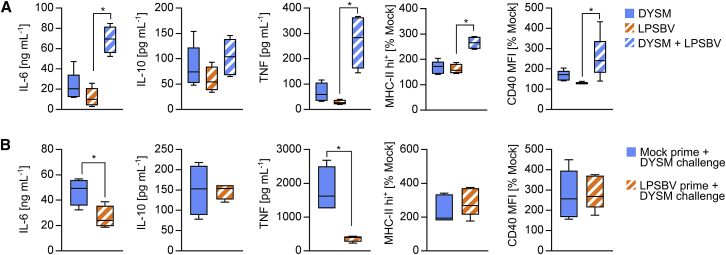
由于DYSM与LPSBV同时刺激会促使BMDCs完全成熟,我们改为先使用LPSBV对BMDCs进行24小时预孵育(致敏),再加入DYSM(激发)。如图7B所示,LPSBV预孵育可诱导细胞对IL-6和TNF表达产生耐受,从而有效抑制DYSM激发引起的促炎细胞因子分泌。然而,与未预处理、仅受DYSM刺激的BMDCs相比,LPSBV预处理并受DYSM攻击的BMDCs其 MHC II 类分子和 CD40 的表面表达水平并未发生显著变化。
这些实验表明,同时用LPSBV和内源性DYSM成分刺激CD11c+ BMDCs细胞时,并不会引发半成熟状态。因此我们得出结论:LPSBV介导的smBDMCs诱导过程,需要在半成熟诱导的初始阶段,必须排除激动性LPS的干扰。
讨论
BVMPK 属于革兰氏阴性菌门拟杆菌门,是哺乳动物肠道中两个最主要的菌门之一(29,30 )。然而,拟杆菌门在肠道微生物群中的比例取决于肠道的炎症状态。在溃疡性结肠炎患者中,拟杆菌属的比例显著降低(55),这支持了拟杆菌属在肠道微生物群中扮演重要有益菌的观点。此外,我们已证实给予BVMPK可在多种实验性结肠炎小鼠模型中预防疾病的发生,其主要机制是通过诱导结肠固有层(cLP)中产生低反应性的半成熟CD11c+细胞(smDCs)。这些smDCs负责预防促炎性免疫反应(20-22,31)。在本研究中,我们发现在Rag1⁻/⁻小鼠的实验性结肠炎模型中,给予BVMPK可显著缓解减轻已建立且持续进行的病理性肠道炎症过程。这些免疫调节特性由LPSBV介导,因为仅使用纯化的LPSBV即可获得愈合效果。因此我们提出,LPSBV可能通过恢复生理性肠道免疫稳态,成为治疗慢性肠道炎症性疾病的一种新型治疗制剂。
BVMPK并非唯一具有此类有益免疫调节特性的拟杆菌属菌株。据报道,BF菌株能在实验性结肠炎小鼠模型中预防肠道炎症(56),并在实验性自身免疫性脑脊髓炎期间抵御中枢神经系统脱髓鞘和炎症(48)。有趣的是,这些特性是通过其荚膜多糖(PSA)与宿主TLR2 相互作用介导的(48,56,57)。目前我们尚未掌握 BVMPK 荚膜多糖的化学结构,但BF与 BVMPK 的密切关联,以及BF 的PSA具有明确的免疫调节特性,促使我们探究TLR2信号通路在CD11c+细胞对 LPSBV 刺激的免疫反应中所起的作用。这一发现尤为重要,因为TLR2介导的信号传导可能源于所用LPSBV制剂中混入的荚膜多糖(45-48,56,57)和脂蛋白(49-51),也可能由LPS本身引起(43,44,58)。尽管检测到微弱的TLR2激活,但关键在于LPSBV制剂通过MD-2/TLR4受体复合物显著介导了CD11c+细胞的半成熟诱导。
在此研究背景下,我们证实,LPSBV的免疫调节特性与强TLR4激动剂(如大肠杆菌来源的原型LPS)或阻断TLR4信号传导的拮抗剂存在显著差异。由于LPSBV既不诱导CD11c+细胞产生促炎细胞因子,又能有效降低其对后续LPS刺激产生低反应性,这种特性恰好兼具TLR4拮抗剂与激动剂的双重作用,因此我们认为,LPSBV在与MD-2/TLR4受体复合物的相互作用中属于弱效激动剂。
为了阐明复杂小鼠菌群中的内源性LPS如何影响CD11c⁺细胞的表型,我们对患肠炎的Rag1⁻/⁻小鼠(DYSM)粪便进行高压灭菌处理。因此,DYSM代表了当LPSBV被给予这些炎症小鼠并表现出缓解炎症作用时所面对的内源性LPS组成及其他微生物成分。有趣的是,与单独使用任一刺激物相比,同时用DYSM和LPSBV刺激BMDCs显著提高了IL-6和TNF的表达,同时MHC II类分子和CD40的表面表达量也显著增加。这一发现很可能是由于细胞因子的诱导以及细胞表面标志物的表达遵循剂量效应关系。如图6B所示,用高浓度LPSBV刺激BMDCs会诱导TNF和IL-6的分泌。当同时加入LPSBV和 DYSM 样本时,相当于以高剂量LPS刺激细胞,从而诱导促炎细胞因子分泌及BMDC活化表面标志的表达。LPSBV的抗炎潜力在图7B中得到清晰体现:该实验先用PBS(模拟对照)或LPSBV预处BMDCs,再用DYSM攻击。实验结果明确显示,LPSBV预处理可显著降低DYSM攻击后的TNF和IL-6分泌。
关于LPSBV在有效减轻肠道炎症方面的治疗效果,我们得出结论:肠道腔内LPSBV的浓度是决定性因素,必须超过内源性激动性LPS的数量,才能在肠道固有层中诱导耐受性的半成熟CD11c⁺细胞。这种当LPSBV浓度足够高时,弱激动性LPSBV与内源性激动性LPS的比例才会增大,从而提高肠道树突状细胞仅接触弱激动性LPSBV的概率。这一点至关重要,因为我们已证实,与强激动性LPS同时接触会阻碍LPSBV诱导的树突状细胞半成熟,反而会引发促炎反应。我们进一步证实,原型激动性LPSEC能够比LPSBV更高效地从MD-2/TLR4受体复合物中置换已结合的LPSBV。
在胃肠道腔内LPSBV浓度超过阈值的情况下,这种影响被认为是不相关的。如实验所示,LPSBV 的内毒素特性与其浓度密切相关:当LPSBV浓度极高时,会促使树突状细胞完全成熟,这正是其弱激动特性与拮抗剂的显著区别。然而,我们证实,通过饮用水给予小鼠约1mg LPSBV的日剂量,可在患有结肠炎的Rag1-/-小鼠中观察到抗炎效果,表明该浓度足以超过胃肠道内源性LPS的含量,又恰好处于诱导半成熟的浓度区间。一旦诱导CD11c⁺细胞进入半成熟状态,这种表型将无法逆转,因此被认为能有效抑制肠道内T细胞的新一轮激活。这意味着,在现有炎症反应逐渐消退后,通过施用LPSBV诱导的新生半成熟树突状细胞,既能阻止持续的T细胞激活(图8),又能促进受损结肠组织的修复。
图8.弱激动性 LPSBV 通过调节肠道CD11c+细胞,影响MD-2/TLR4受体复合物激活并抑制CD4+T细胞介导免疫应答的机制
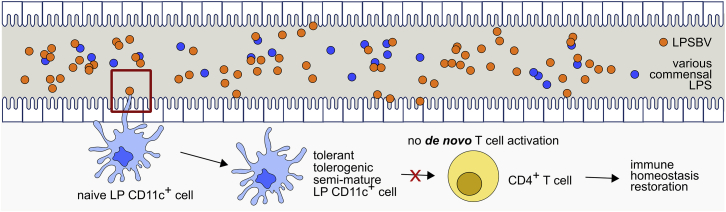
通常而言,LPS是一种强效的MD-2/TLR4受体复合物激动剂,能够引发靶细胞中强烈的细胞内信号传导,进而激活与促炎免疫反应相关的基因转录(13)。而研究表明,LPS诱导的这种细胞内信号传导强度,学界普遍认为主要由其脂质A结构域介导(59,60)。
已有研究证实,多种拟杆菌属(Bacteroides spp.)的脂质A结构含有4-5条酰基链和0-1个磷酸基团(8)。由于我们发现BVMPK的脂质A合成核心基因与其它拟杆菌属存在高度相似性,因此我们推测LPSBV与LPSEC相比,可能具有更低的酰基化和磷酸化水平。六酰化和双磷酸化的E. coli脂质A被认为是MD-2/TLR4受体复合物介导信号传导最有效的激活剂,因为有研究表明,其六条酰基链中有五条被埋藏在MD-2结合腔内,而第六条酰基链则指向MD-2表面,与TLR4胞外结构域形成疏水相互作用,这对TLR4激活至关重要(12,34)。这或许能部分解释缺乏第六条酰基链的低酰化脂质A结构为何具有较低的内毒素活性,以及低酰化LPSBV为何表现出较弱的激动活性。此外,脂质A二葡萄糖胺骨架上的1‘位和4’-位磷酸基团已被证实是激活MD-2/TLR4受体复合物的重要组成部分(13)。由于拟杆菌目菌株在还原型葡萄糖胺1‘位点仅保留一个磷酸基团(8),这可能也是其激动活性较弱的原因——研究显示缺失4’-磷酸基团会导致内毒素活性降低100倍(61)。
我们认为,LPSBV的弱激动特性正是在小鼠肠道炎症中观察到的修复愈合效果的原因。在此机制下,弱激动性LPS可诱导较弱但仍可检测的细胞内信号传导和NF-κB激活,从而提供基础性抗炎转录程序,且不会突破促炎反应阈值。此外,LPSBV还能主动诱导 CD11c+ 细胞进入低反应状态。这些特性明显区别于强激动性LPS(如 LPSEC),后者虽能诱导内毒素耐受,却会引发强烈的促炎信号。然而,弱激动性LPS也不同于拮抗性LPS,后者既不促进促炎反应,也不诱导TLR4表达细胞的耐受性。LPSBV能成为MD-2/TLR4受体复合物的有效配体同时又保持弱激动活性,本质上归因于其化学结构。我们认为,这代表了共生肠道菌群LPS的一种“化学范式”,是微生物适应宿主环境的重要机制。与此吻合的是,其他研究团队也报道过拟杆菌LPS对维持肠道稳态的贡献(8)。然而,本研究首次成功利用源自共生菌的LPS,在重度肠道炎症的小鼠模型中实现了重建恢复肠道免疫稳态的成功尝试。
然而,弱激动型LPS的免疫效应似乎具有情境依赖性。在另一项研究中,Vatanen等人发现(33),幼年期接触强激动性LPS较少的儿童,其1型糖尿病(T1D)发病率更高,且其肠道内携带低酰化、低磷酸化LPS的微生物比例也更高。与此一致的是,在非肥胖糖尿病(NOD)/Shilt小鼠出生后不久就开始持续腹腔注射大肠杆菌LPS,可延缓T1D发病,而低酰化和低磷酸化BD LPS给药则无此效果(33)。该研究支持了"卫生假说",即幼年早期接触高免疫原性微生物有助于免疫系统发育,并能保护宿主免受过敏和自身免疫性疾病侵害。乍看之下,这些观察结果似乎与我们的研究结果相矛盾。但在本研究中,我们旨在通过干预成年动物的严重肠道炎症来主动重建免疫稳态,这与通过调节婴儿肠道菌群预防自发性疾病的目标有所不同。此外,其他研究团队认为低磷酸化和低酰化拟杆菌LPS具有拮抗作用。而我们的研究明确表明,这些LPS结构实际上发挥着弱激动剂的作用。
我们的研究结果与其他团队的发现共同提出了一个重要问题:弱激动性LPS是否能成为理想的治疗手段,不仅适用于实验性小鼠模型,还能帮助 IBD 患者恢复稳态平衡。迄今为止,IBD患者的治疗主要依赖于全身性免疫抑制,这种方法通常伴随不良副作用。而基于LPS(及其衍生物)的治疗策略,有望通过仅作用于炎症局部——即肠道,从而有效规避这一问题。
尽管我们的研究结果明确表明,LPS对肠道固有层CD11c⁺细胞的直接调控是促成愈合效应的关键机制,但我们仍不能完全排除另一种可能性:肠道稳态的重建或许只是LPSBV诱导微生物群从失调状态向稳态转变后产生的次级效应。
尽管如此,我们仍致力于将纯化的LPSBV作为治疗肠道炎症性疾病或IBD的替代疗法,并通过实验证实该化合物展现的有益效应并非源于拮抗作用,而是基于其弱激动特性,从而证明其疗效优势。综上所述,本研究为IBD治疗领域提供了全新思路,有效规避了现有IBD 疗法的局限性,为相关研究开辟了新方向。
免责声明:
以上部分内容来源于外网我们重在信息分享,版权归属原作者或原刊发平台所有,如有侵权、信息有误或其他异议,请联系处理,我们将在24小时内删除或整改。
复合免疫 健康活力





























