
口服LPS泛菌糖脂质维持肠道免疫系统稳态的机制
参与肠道稳态的肠道巨噬细胞具有响应LPS的潜力
摘要
最近,人们对食物的第三种功能,即维持人体健康的功能产生了兴趣。此外,已经发现作为革兰氏阴性菌成分的脂多糖(LPS)在激活先天免疫方面非常有效,并且已经作为新的功能性食品材料被重新发现。在这篇综述中,我们根据最近的发现,讨论了LPS作为食物成分的重要性。特别强调肠道巨噬细胞对LPS反应的可塑性。根据巨噬细胞网络理论,局部巨噬细胞与其他组织巨噬细胞合作。因此,本文也讨论了信息从肠道巨噬细胞传递到全身的可能性。
关键词:肠巨噬细胞,LPS,稳态,CD14,IgA,综述。
食物既提供营养,也可能在提供调节健康的第三种功能。对这些三级功能的免疫调节可以预防某些疾病或保持和增强健康。在发达国家,人们希望能够开发这些第三功能,以抵消与生活方式有关的疾病问题,如高脂血症、糖尿病和癌症,以及与向老龄化社会过渡有关的问题。
来自食物中革兰氏阴性菌的LPS可以调节免疫力。食物中的LPS被认为是通过肠道中的巨噬细胞发挥作用的。
巨噬细胞存在于人体的每个组织中,它们被称为组织巨噬细胞。当驻留的组织巨噬细胞遇到外来物质时,它们产生细胞因子并呈递抗原,将信号传递给邻近的巨噬细胞(1)。肠道巨噬细胞存在于肠道粘膜的固有层(2),在那里它们与外部环境紧密接触。它们构成了手册中最大的巨噬细胞库(3),并被认为能够识别功能性食品。因此,我们认为体内平衡部分是由肠道巨噬细胞的这种反应调节的。
LPS存在于一些食物中,并在调节免疫中发挥作用。食物中的LPS通过肠道中的常驻肠道巨噬细胞的作用发挥作用。LPS是已知免疫增强剂中最强的巨噬细胞激活物质。食物含有约0.16至600 ng/g的LPS(4)。我们认为,这些LPS在被肠道巨噬细胞识别后具有调节免疫的功能。
在这篇综述中,我们讨论了LPS作为一种具有第三调节功能的食物成分的重要性。最近的研究发现表明,肠道巨噬细胞对LPS的反应存在可塑性。根据巨噬细胞网络理论,局部巨噬细胞与其他组织中的巨噬细胞相互协作。这可能允许信息从肠道巨噬细胞向全身传递信息。
消化道固有层粘膜中存在肠道巨噬细胞的特征
众所周知,细胞因子如干扰素(IFN)α、肿瘤坏死因子(TNF)和白细胞介素(IL)-1是在腹腔、脾脏、肺泡等组织巨噬细胞的LPS刺激下分泌的。CD14和toll样受体(TLR)4存在于巨噬细胞的细胞膜上,并识别LPS (5)。信号被传递到衔接分子,如MyD88,以激活转录因子(6,7)。这一特征被认为在巨噬细胞中很常见。然而,现在已经清楚的是,肠道巨噬细胞具有不同的特征。
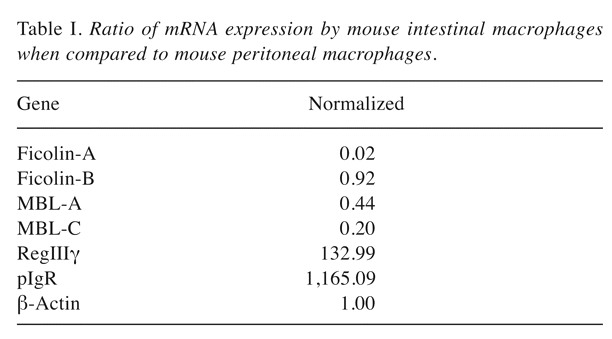
肠道巨噬细胞表达CD33、CD68和CD13标记物的方式与单核细胞和其他组织巨噬细胞相同(8,9)。然而,与其他组织巨噬细胞不同的是,肠道巨噬细胞在其细胞膜上不表达CD14或TLR4(9)。有报道称,肠巨噬细胞在LPS刺激后不分泌细胞因子(10).因此,他们被认为对LPS无反应。也有报道称,肠道巨噬细胞不表达IgA的Fc受体(CD89)或IgG (CD16、CD32、CD42),也不表达除LPS受体以外的受体复合物如CR3 (CD11b/CD18)或CR4 (CD11c/CD18)(9, 11-14)。除了抑制受体的表达,还报道了肠道巨噬细胞不产生炎症细胞因子IL-12,相反,它们产生具有抗炎作用的IL-10(15)。我们使用DNA芯片比较了肠道巨噬细胞和腹腔巨噬细胞之间的mRNA表达。无花果蛋白酶和甘露糖结合凝集素(MBL)(被称为防御凝集素)的表达(16)识别病原体相关分子模式(PAMPs);其表达量低于肠道巨噬细胞(表I)。根据这些结果,认为肠道巨噬细胞具备清除外来物质和调节炎症机制的能力。它们的反应与其他组织中的巨噬细胞不同。
然而,未观察到CD14在常驻的肠道巨噬细胞的膜上表达,最近有报道称CD14作为蛋白质形式存在于细胞内(17)。在IgA涂层的培养孔中培养肠道巨噬细胞时,CD14的表达被诱导到细胞膜上(18)。此外,当这些细胞用LPS刺激时,TNF的表达也会发生(10)。这表明了可塑性的可能性:在某些条件下,当肠道巨噬细胞中的CD14在膜上表达时,肠道巨噬细胞表现出对LPS的反应性。
表一
与小鼠腹腔巨噬细胞相比,小鼠肠巨噬细胞的mRNA表达比率。
综上所述,我们认为虽然肠系膜巨噬细胞似乎对LPS没有反应,但它们能够识别LPS。这是LPS通过肠系膜巨噬细胞维持肠道稳态的方式。
LPS作为功能性食品的一种成分
LPS作为革兰氏阴性菌细胞壁的成分通常被称为内毒素。目前,只有少数报道描述了LPS的用途有效性,包括将其添加到食物中。然而,它存在于许多食物中,据报道,麦麸(132μg/人)和麦芽(180μg/人)中含量显著,这两种食物都被称为健康食品(4)。已知革兰氏阴性菌在许多粮食作物上是共生的,例如水稻、甘薯、苹果和梨(19)。此外,生产椰果和里海酸奶需要革兰氏阴性菌的发酵,因此这些食物中含有LPS。因此,人们已经在不知不觉中消费了LPS,并可能从中受益。这些报道提供了LPS作为肠道稳态的重要分子的具体例子。首先,对通过预先施用抗生素患有溃疡性结肠炎的小鼠的存活率和病理学进行了研究(20)。结果显示,单独给予DSS后12天没有存活。相比之下,在除DSS外还给予LPS的小鼠组中,存活率为100%。在溃疡性结肠炎的病理学方面(体重减轻和便血)也获得了显著有利的结果(体重减轻和便血)。
RegIIIγ是一种凝集素,具有抑制革兰氏阳性菌(21)活性的能力。它是由肠上皮或paneth细胞分泌,并由肠道共生细菌TLR4 MyD88介导的信号诱导(21, 22).据报道,施用抗生素后RegIIIγ的产生受到抑制,并且万古霉素的耐药细菌却大量繁殖。但是,当LPS和抗生素一起使用时,万古霉素耐药细菌的扩散被抑制(23)。因此,在我们使用DNA阵列分析对肠道巨噬细胞和腹膜巨噬细胞进行的比较分析时,观察到RegIIIγ在肠道巨噬细胞中的表达高于在腹膜巨噬细胞中的表达(表一).换句话说,我们的实验结果表明肠道巨噬细胞可能产生RegIIIγ。我们推测肠道巨噬细胞通过TLR4识别LPS后产生RegIIIγ。
肠道巨噬细胞对LPS的识别
目前的研究结果表明,对LPS无反应的常驻肠道巨噬细胞,如果不接触肠道组织中的IgA,就不能获得对LPS的应答。正常情况下,常驻的肠道巨噬细胞存在于固有层粘膜(2),而IgA由肠道固有层粘膜中的IgA浆细胞以二聚体的形式产生和分泌(14)。这种二聚体IgA通过与肠粘膜上皮细胞中的分泌成分(SC)结合而形成;它分泌在粘膜表层的粘液中,有助于粘膜上的免疫(24)。因此,肠巨噬细胞和IgA被肠上皮细胞分离,彼此不直接接触。
肠道总是暴露于来自饮食和肠道细菌的抗原。虽然粘膜上皮细胞不会因这些抗原引发严重的炎症,但它们会产生抗菌肽或趋化因子来保护肠道免受感染。这种防御机制要求抗原能有效地转移到与黏膜相关的淋巴组织,如派尔氏结(Peyer’s patches)(25)。为此,M细胞通过转胞吞作用积极摄取粘膜上的抗原,并将其递送至存在于上皮细胞正下方的抗原呈递细胞(26)。如果该抗原被IgA调理,对LPS的反应可能是通过诱导CD14或TLR4在巨噬细胞膜上的表达而获得的,巨噬细胞直接存在于上皮细胞下并识别IgA。
然而,已经有报道称,识别IgA的分子CD89在肠道巨噬细胞中不表达(9, 11, 27)。因此,有研究认为肠道巨噬细胞可能表达除CD89以外的IgA受体,如IgA或IgM的Fc受体(Fcα/μR)(28, 29)、聚合免疫球蛋白受体(pIgR)(30,31),CD71(32),以及去唾液酸糖蛋白受体(ASGPR)。事实上,观察到pIgR在肠巨噬细胞中的表达高于在腹膜巨噬细胞中的表达(表一)。此外,据报道,新生儿免疫球蛋白受体(FcRn)在肠道巨噬细胞中表达(33-35)。目前尚不清楚是哪种受体能够识别IgA并诱导CD14的膜表达,但人们认为在肠道巨噬细胞中存在一些受体参与CD14的膜表达(图1).
图一
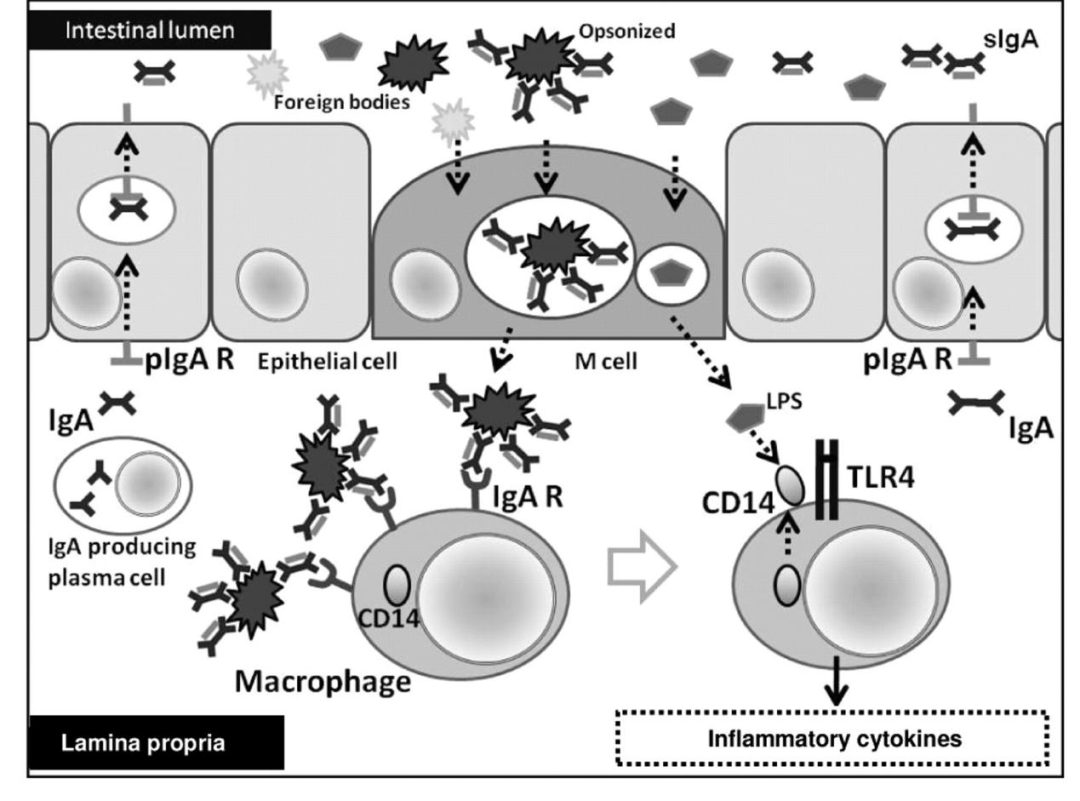
肠巨噬细胞与LPS接触的假设过程。产生IgA的浆细胞在肠固有层产生IgA。分泌型IgA (sIgA)在管腔中分泌(sIgA调理抗原)。调理抗原的胞转作用发生在M细胞中。然后肠巨噬细胞识别来自IgA的调理抗原,并被诱导表达CD14。最后,肠道巨噬细胞识别肠道固有层中侵入性LPS的存在。
消化道中肠巨噬细胞引起的全身效应
如上所述,肠道巨噬细胞对LPS的识别不仅仅是维持肠道的稳态。有报道称,局部激活的巨噬细胞通过细胞间接触向其他巨噬细胞传递信号。这被称为“巨噬细胞网络”(36)。人们认为巨噬细胞网络是体内平衡的控制系统。
众所周知,肠道巨噬细胞不会被LPS激活。但它们与外部环境有着密切接触。此外,固有层包含体内最大的巨噬细胞库。在这种情况下,认为肠道巨噬细胞成为通过巨噬细胞网络传递信息的细胞。
肠道巨噬细胞对LPS的识别被认为具有超出维持肠道的稳态。需要进一步的研究来阐明LPS与肠巨噬细胞相互作用的分子证据。
免责声明:
以上部分内容来源于外网我们重在信息分享,版权归属原作者或原刊发平台所有,如有侵权、信息有误或其他异议,请联系我们,我们将在24小时内删除或整改。
复合免疫 健康活力





























