
科学护肝新突破:这样“预处理”,让肝脏自带“抗炎结界”!
LPS预处理可改善D-GalN/LPS诱导的急性肝衰竭
熬夜、饮酒、滥用药物……我们的肝脏每天都在默默承受着各种挑战,而急性肝衰竭更是其中凶险的“无声杀手”!如何为肝脏建立起一道坚实的防线?一项前沿研究带来了突破性思路:
科学家们发现,通过小剂量的LPS(脂多糖)进行“预处理”,可以显著提升肝脏对致命损伤的抵抗能力。这好比为肝脏提前披上“防护衣”,当严重的打击真正来临时,肝脏已经拥有了强大的“免疫记忆”与内在保护机制,从而安然度过危机。接下来,一起“走进实验室”,看大鼠如何用“内毒素耐受”逃过致命一击,也为人类急性肝衰竭点亮新的治疗曙光。
脂多糖(LPS)预处理可通过TLR4信号通路改善D-GalN/LPS诱导的急性肝衰竭
摘要
内毒素耐受(ET)是一种影响炎症反应和吞噬作用的重要生理现象。低剂量脂多糖(LPS)预处理可有效保护肝脏免受对乙酰氨基酚、铜绿假单胞菌外毒素A等多种肝毒性物质的损伤。本研究旨在探讨D-半乳糖胺(D-GalN)/LPS诱导的急性肝衰竭中内毒素耐受的保护机制,以及Toll样受体4(TLR4)信号通路在此现象中的潜在作用。通过注射D-GalN/LPS诱导急性肝衰竭模型。为模拟内毒素耐受,雄性Sprague-Dawley大鼠在注射D-GalN/LPS前,连续五天每日腹腔注射低剂量LPS(0.1 mg/kg)。通过存活率评估大鼠存活情况,采用血清生化指标和肝组织病理学检查确认肝损伤。采用ELISA法检测炎症细胞因子水平,分别通过逆转录聚合酶链反应和蛋白质印迹法检测核因子κB(NF-κB)(P65)、Toll样受体4(TLR4)和白细胞介素-1受体相关激酶-1(IRAK-1)的表达。结果显示,LPS预处理显著提高大鼠存活率。与未预处理组相比,LPS预处理组大鼠血清酶(ALT、AST和TBiL)水平降低,炎症细胞因子生成减少,肝组织病理学损伤程度减轻。LPS预处理抑制了TLR4和IRAK-1的表达,也同样抑制了肝脏NF-κB的活化。这些结果表明,内毒素耐受性通过下调TLR4和NF-κB通路,对D-GalN/LPS诱导的急性肝衰竭发挥肝脏保护作用。
引言
急性肝衰竭(ALF)是肝脏遭受严重损伤后引发的病症,这种损伤会在短时间内出现凝血病和脑病,并引发累及多个器官的全身性炎症反应[1,2]。ALF的病因多样,包括感染性疾病、代谢性疾病、药物毒性及其他多种因素。虽然目前认为ALF的发病机制与机体免疫平衡失调密切相关,但具体作用机制仍不明确。研究表明,肝实质细胞(肝细胞)的大规模坏死和凋亡会释放多种炎症细胞因子,这些细胞因子直接导致急性肝衰竭、全身性炎症及免疫系统紊乱[3,4]。此外,Toll样受体(TLRs)等信号分子在炎症性坏死过程中也发挥着重要作用。
内毒素作为革兰氏阴性菌的脂多糖(LPS),能够刺激多种炎症介质的释放,这些介质会促进急性肝衰竭(ALF)的发展[5]。已有研究表明,当单核细胞/巨噬细胞等先天免疫细胞或器官预先接触少量内毒素后,会对后续的内毒素攻击产生耐受,这种现象被称为内毒素耐受(ET)[6]。尽管Beeson博士早在60多年前就描述了ET现象[7],但其具体机制至今仍未完全阐明,临床应用亦有限。然而,ET状态能显著缓解多菌感染性脓毒症、炎症性坏死及器官功能损伤,其作用机制与炎症反应减弱和吞噬功能增强密切相关[8, 9]。
Toll样受体(TLRs)是一类能够识别病原体相关分子模式(PAMPs)的膜受体,参与机体的免疫应答系统。脂多糖(LPS)作为内毒素的主要成分,可与TLR4结合。近期研究表明,TLR信号通路可能介导树突状细胞、T淋巴细胞和肥大细胞之间的相互作用,从而调节过敏性免疫应答[10]。TLR4是检测革兰氏阴性菌及其相关内毒素的主要模式识别受体(PRR)[11]。TLR4一旦被激活,会进一步激活转录因子核因子κB(NF-κB),NF-κB作为不同受体的下游细胞内分子,参与多种促炎基因(如促炎细胞因子)的表达。促炎细胞因子的表达增加又会进一步激活NF-κB。因此,TLR信号的调控在炎症反应中至关重要。例如,TLR4基因突变可通过下调NF-κB激活来减轻细胞损伤[12]。此外,白细胞介素-1受体相关激酶-1(IRAK-1)是TLR信号通路的重要正向调节因子。研究发现,IRAK-1表达增强可通过与Toll相互作用蛋白(Tollip)结合,强烈激活NF-κB[13]。Tollip通过抑制TLR激活和磷酸化,促进炎症反应终止并维持免疫细胞的静息状态。
鉴于NF-κB和TLR4在炎症反应中的关键作用,本研究通过验证:小剂量LPS能否通过调控TLR4、IRAK-1及NF-κB(p65)信号通路,改善D-GalN/LPS诱导的急性肝衰竭。从而阐明内毒素耐受(ET)在抑制炎症引发的器官损伤中的潜在保护机制。
结果
LPS预处理对急性肝衰竭(ALF)生存率的影响
我们首先研究了LPS预处理对大鼠存活率的影响。如图1所示,在急性肝衰竭(ALF)组接受D-GalN/LPS注射的10只大鼠中,共死亡6只,其中4只于前12小时内死亡。ALF组大鼠3天内的死亡率为60%。相比之下,注射D-GalN/LPS后,ET+ALF组的所有大鼠在LPS预处理的大鼠中均存活。3天内死亡率为0%。这两组之间存活率存在显著差异(P < 0.05)。
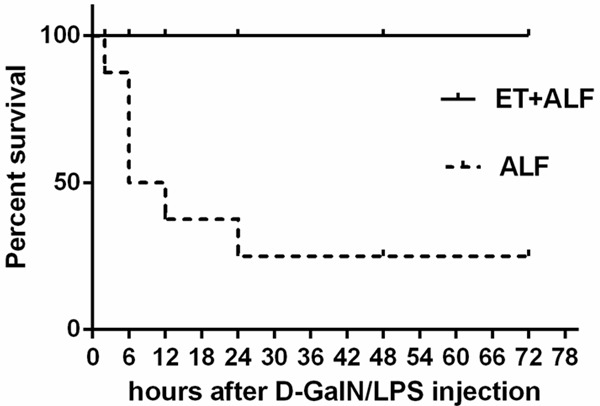
图1.LPS预处理对急性肝衰竭(ALF)大鼠存活率的影响。
LPS预处理对急性肝损伤(ALF)及细胞因子释放的影响
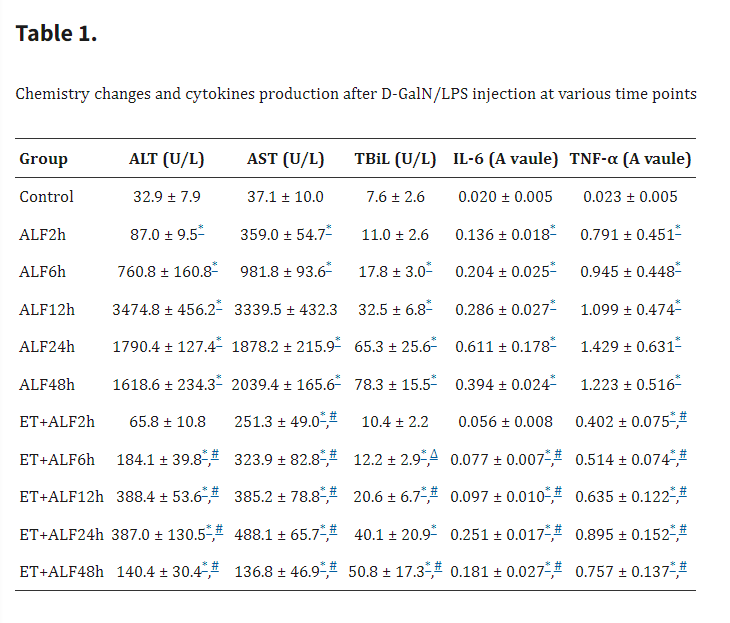
随后对ALF模型的肝损伤及细胞因子释放进行了研究。通过H&E染色观察肝组织病理学变化,对照组肝脏组织学表现正常(图2)。然而,ALF组与ET+ALF组的肝组织均呈现不同程度的损伤,且存在显著差异。ALF组肝脏组织出现严重损伤,表现为肝小叶结构破坏、肝索断裂及大量浸润性炎症细胞(以单核细胞和淋巴细胞为主),同时可观察到坏死和凋亡现象(图2)。而ET+ALF组肝损伤程度较轻,肝细胞坏死较少,肝小叶结构清晰可见,且浸润性炎症细胞数量较少(图2)。此外,我们还检测了肝损伤的血清标志物。如表1所示,腹腔注射D-GalN/LPS后,ALF组和ET+ALF组的ALT、AST及TBiL水平均升高。但ALF组各时间点的ALT、AST和TBiL升高幅度均显著高于ET+ALF组(p<0.05)。值得注意的是,两组的ALT和AST水平均在注射后12小时达到峰值,而TBiL水平则在注射后持续升高。除减轻肝损伤指标外,LPS预处理还显著降低了炎症介质(TNF-α和IL-6)的产生(表1)。虽然在ALF和ET+ALF组中注射D-GalN/LPS后,TNF-α和IL-6的表达均有所增加,但在实验的每个时间点,ET+ALF组大鼠的TNF-α和IL-6水平均显著低于ALF组(P<0.05)。
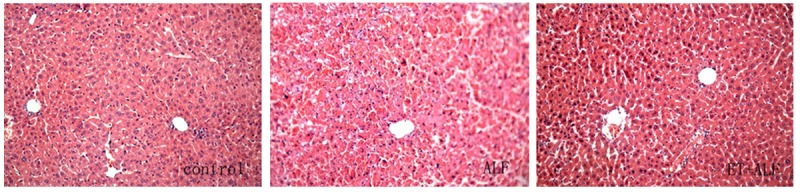
图2.肝组织切片的组织病理学检查结果。
表1.注射D-GalN/LPS后不同时间点的化学变化和细胞因子的产生
LPS预处理对急性肝衰竭中P65、TLR4和IRAK-1表达的影响
为阐明LPS预处理对存活率和肝损伤的作用影响,我们进一步研究了可能参与细胞因子释放的机制,特别是NF-κB激活情况。通过RT-PCR和Western blot分别检测了注射D-GalN/LPS后2小时、6小时、12小时、24小时、48小时P65、TLR4及IRAK-1的mRNA和蛋白水平。如图3所示,与对照组相比,ALF组和ET+ALF组均观察到P65、TLR4和IRAK-1表达量显著升高。然而,LPS预处理显著降低了ET+ALF组大鼠肝脏中P65、TLR4和IRAK-1的mRNA丰度(P<0.05)。图4通过Western blot进一步验证了肝脏组织中P65、TLR4和IRAK-1的蛋白水平。与对照组相比,注射D-GalN/LPS后ALF组和ET+ALF组的P65、TLR4和IRAK-1蛋白水平显著升高。值得注意的是,LPS预处理后,P65、TLR4和IRAK-1的蛋白丰度在实验各时间点均显著降低(P<0.05,图4)。
讨论
目前,临床上急性肝衰竭(ALF)仍属预后极差的疾病,患者死亡率居高不下。因此,亟需深入研究其发病机制以优化更有效的治疗方案。当肝衰竭发生时,肝功能严重受损并常伴有肠源性内毒素血症。已有研究证实,内毒素(如脂多糖)介导的巨噬细胞活化及炎症反应,在急性与慢性肝病中起着关键作用[14]。
D-GalN/LPS诱导的小鼠急性肝衰竭(ALF)模型,已被证实是广泛用于模拟人类ALF形成并阐明其确切发病机制的理想动物模型[15]。D-GalN可直接消耗肝细胞内的尿苷一磷酸(UMP),导致核酸、糖蛋白和脂质合成减少,细胞器破坏,肝细胞结构与功能受损,并引发肝细胞凋亡[16,17]。已有研究表明,LPS诱导的肝损伤与肝窦隙内皮细胞和Kupffer细胞的活化密切相关[18]。因此,D-GalN与LPS联用可通过影响生物大分子合成、刺激肝细胞凋亡、促进自由基生成及脂质过氧化等多种机制,加剧肝损伤。本研究中,通过检测血清ALT、AST、TBiL水平的变化及肝病理学改变建立的肝损伤动物模型,与临床观察到的ALF患者表现高度吻合。我们的研究结果与其他课题组采用D-GalN/LPS建立ALF模型的研究结论一致。
与既往研究报道一致,D-GalN/LPS诱导的肝细胞凋亡主要由TNF-α介导 [19]。此外,GalN/LPS诱导的急性肝功能衰竭(ALF)模型中,TNF-α水平与大鼠存活率及肝细胞凋亡程度密切相关[20]。临床研究亦表明,危重ALF患者常因持续而强烈的免疫与炎症反应,导致肝损伤进一步加剧 [21]。本研究发现,炎症细胞因子(TNF-α和IL-6)的表达水平与肝损伤程度密切相关,且这两种细胞因子在免疫调节中亦发挥着重要作用。
免疫耐受的形成可受多种因素影响,如反应性细胞缺失、受体下调、信号传导受阻及细胞因子抑制等[22]。研究表明,内毒素耐受可通过抑制肝脏单核细胞浸润、减少促炎细胞因子生成并诱导内源性抗炎细胞因子产生,从而发挥肝脏保护作用[23,24]。提前数日给予大鼠无毒剂量的LPS预处理,可有效减轻D-GalN/LPS诱导的肝损伤。该保护作用被认为与炎症细胞因子(包括TNF-α和IL-6)的减少密切相关。然而,亦有研究指出,某些细胞因子(如IL-10)的过表达可能与内毒素耐受相关[25,26]。本研究发现,LPS预处理显著降低了D-GalN/LPS处理组大鼠血清中TNF-α和IL-6水平。鉴于TNF-α在肝衰竭中起关键作用,而IL-6是炎症反应的核心介质,LPS预处理对D-GalN/LPS诱导的肝衰竭的保护作用,可能源于其抑制细胞因子生成及其信号通路等炎症反应的机制。
NF-κB信号通路是启动炎症细胞因子表达的关键途径。研究表明,LPS暴露可诱导NF-κB从细胞质向细胞核转位,并结合DNA上的NF-κB启动子位点,从而激活TNF-α的转录[27]。此外,抑制NF-κB激活已被证实可有效减轻炎症反应和细胞凋亡[15,28]。TLR4作为结构多样的微生物分子(如LPS)最重要的信号转导受体之一,能够激活NF-κB通路进而调控炎症细胞因子表达及免疫反应。本研究结果与既往报道一致:D-GalN/LPS显著诱导TLR4表达,同时激活NF-κB信号通路并促进炎症细胞因子表达,最终导致肝损伤。这些发现与TLR4基因敲除研究结果相互印证,后者表明TLR4敲除小鼠的炎症反应和肝损伤减轻,表现为NF-κB激活减少和TNF-α水平降低[29]。此外,沉默TLR4表达可显著抑制LPS诱导的IL-6和 IL-8产生[30]。因此,本研究证实,LPS 预处理能有效提高动物存活率并缓解 D-GalN/LPS诱导的肝损伤。我们推测,其机制在于LPS预处理下调TLR4表达和抑制 NF-κB 激活,从而保护肝脏免受D-GalN/LPS诱导的损伤。
此外,IRAK-1 作为LPS介导的 TLR4 通路中的关键分子,能够与细胞膜上的TLR4相互作用并激活LPS信号传导,这一机制与髓样分化因子88(MyD88)介导的信号转导类似。抑制IRAK-1可通过下调炎症介质表达来减轻炎症反应 [31,32]。我们的结果与相关研究一致——在LPS预处理条件下,IRAK-1表达显著降低。值得注意的是,信号通路常呈现双向调控特性。最新研究表明,抑制TNF-α可有效抑制TLR4和NF-κB信号通路的激活[33]。因此,LPS预处理可能在调控免疫平衡的信号通路相互作用中发挥重要作用。此外,LPS预处理可能影响IRAK-1和TLR4等信号分子的自磷酸化,从而促进复杂信号通路的整合。或调控信号蛋白表达可能是保护肝脏组织免受过度免疫反应损伤的关键机制。更重要的是,深入理解内毒素耐受的具体机制,将有助于完善急性肝衰竭(ALF)的病理生理学认知,并为未来临床治疗提供新思路。
综上所述,LPS预处理能显著提高存活率,并有效保护肝脏免受D-GalN/LPS诱导的急性肝衰竭所导致的肝损伤。其作用机制可能与LPS预处理通过TLR4信号通路(如NF-κB、IRAK-1等关键分子)抑制炎症因子产生有关。尽管LPS预处理的时机对急性肝衰竭干预效果至关重要,但本研究至少为该疾病的治疗干预提供了新的靶点与治疗方案。
免责声明:
以上部分内容来源于外网我们重在信息分享,版权归属原作者或原刊发平台所有,如有侵权、信息有误或其他异议,请联系处理,我们将在24小时内删除或整改。
复合免疫 健康活力





























