
从背锅侠到免疫新宠,口服LPS获科学验证,长期安心之选!
长期口服LPS不会增加小鼠的炎症或诱导代谢失调
听说过“LPS”脂多糖(泛菌糖脂质)吗?这个被宣传为“激活免疫力”的明星成分,背后一直存在一个争议:长期服用会不会反而加剧体内炎症?特别是对于日常饮食油腻的人群,它是否会雪上加霜?口服LPS补充剂,究竟安不安全?是时候刷新我们对LPS的认知了!
传统观点常将脂多糖(LPS)与炎症、代谢紊乱划上等号,尤其在高脂饮食的背景下,它更是被视为健康的“潜在威胁”。然而,一项严谨的动物实验直面了这一担忧,给出了定心丸:研究证实,长期口服LPS,并不会引发持续的全身性炎症,也不会导致代谢失调——即使是在高脂饮食喂养的小鼠身上也是如此。
该研究指出,LPS引发的初期炎症反应仅是短暂且轻微的,并不会持续累积。真正的健康风险,或许更多地来自于不健康的饮食模式本身,而非我们口服摄入的LPS。这一结论为LPS的安全性与其作为先天免疫调节剂的潜力,提供了强有力的科学背书。这意味着,我们或许可以更安心地利用LPS来为免疫健康加分。
长期口服LPS不会增加小鼠的炎症或诱导代谢失调
简介:有研究认为,肠道内的脂多糖(LPS)在摄入高脂饮食后会进入血液循环,并通过名为"代谢性内毒素血症"的过程引发全身性炎症和代谢失调。本研究旨在明确探讨小鼠口服LPS对饮食诱导的慢性低度炎症早期阶段的作用。
方法:我们在饮用水中添加大肠杆菌来源的LPS,分别饲喂高脂西式饮食(WSD)和标准饲料(SC)的小鼠,持续7周(每组n=16-17只)每周记录体重变化。通过不同时间点对NF-κB活性进行活体成像评估全身炎症状态,并在研究临近结束时通过胰岛素敏感性试验和葡萄糖耐量试验评估葡萄糖调节功能。通过检测血浆中LPS结合蛋白(LBP)和抗LPS抗体水平间接评估全身LPS暴露水平,并采用LPS敏感的细胞报告基因实验直接测定LPS水平。
结果与讨论:我们的研究结果表明,LPS对体重发育与葡萄糖调节均无影响。在两个饮食组中,我们观察到肝脏区域的NF-κB活性存在短暂的LPS依赖性上调现象,该反应在LPS给药第一周内即消失,并在后续研究期间持续维持低位。然而,与标准饲料(SC)组相比,西式饮食(WSD)组小鼠在所有时间点的NF-κB活性整体更高,且该现象与LPS给药无关。我们的研究结果表明:对于高脂西式饮食喂养的小鼠而言,口服LPS对全身性炎症及代谢紊乱的影响甚微甚至可忽略;我们质疑肠道来源的LPS是否能够通过健康且未受损的肠道引发全身炎症,即使在高脂饮食条件下也是如此。
引言
脂多糖(LPS)是革兰氏阴性菌外膜的主要成分,天然存在于人体肠道菌群中。LPS由多糖和名为脂质A的脂质成分构成。宿主先天免疫系统通过识别LPS(脂质A)来抵御潜在病原体入侵。这种识别通常始于与LPS结合蛋白(LBP)的初始结合,随后LPS会被递送至由CD14、MD-2和Toll样受体4(TLR4)组成的复合体(1)。LPS与TLR4的相互作用会引发炎症反应,其特征是通过转录调节因子核因子-κB(NF-κB)介导的促炎细胞因子水平升高。根据LPS的浓度和分布位置,这种反应可能表现为急性局部反应或全身性反应(2,3)。研究表明,循环系统中LPS的轻微升高会引发低度炎症,这与胰岛素抵抗和超重等代谢失调现象相关(4-6)。
在健康人群的循环系统中,似乎可以检测到极低浓度的LPS。有研究指出,在摄入某些特定饮食模式后,LPS可能通过肠壁转移至循环系统,导致全身性LPS水平升高,这一现象被称为"代谢性内毒素血症"(4)。在摄入高脂、高热量或高碳水化合物饮食后,LPS从肠道向血液的转移可能会增加(6-8)。目前,膳食脂肪是已知促进肠道LPS转移的主要膳食因素(9–14),而高糖饮食似乎会增强这种作用(15)。尽管科学界普遍认同这一观点,但关于饮食、血液LPS水平升高与低度炎症之间的关联机制仍未明确。值得注意的是,最初证明LPS导致代谢性内毒素血症的研究,是通过植入式渗透泵全身输注LPS进行的,从而绕过了肠道来源LPS的生理途径(4)。相反,Dalby等团队的研究表明,饮食诱导的肥胖并不依赖TLR4或分化簇14(CD14)信号通路(16),这对LPS在引发或促进代谢性内毒素血症中的重要性提出了质疑。大多数支持高脂饮食诱导代谢性内毒素血症的研究,主要基于鲎试剂溶解物(LAL)检测法测定的血液样本中LPS水平升高的实验结果(4, 6, 17)。然而LAL检测法的实用性存在争议,因为该检测无法区分LPS对TLR4的刺激特性。血液样本中LPS的检测被认为困难且易受误差影响,其结果会受到抑制和增强因素的显著干扰(详见Boutagy、McMillan(18)以及Gnauck、Lentle和Kruger(19)的综述)。此外,这些综述还指出,文献报道的人类血液LPS浓度范围差异很大,这使得难以确定正常状态与炎症状态之间的可量化阈值。
循环系统中LPS的主要来源可能是胃肠道(GIT)内的共生菌群,该区域是革兰氏阴性菌的富集区(20)。通过摄入常见食品,肠道外LPS也可能从外界环境进入(21-23)。Erridge团队发现,多种常见加工食品含有显著量的TLR4刺激物(21-23),这表明以加工类和预包装食品为特征的现代饮食模式,与TLR4激动剂(如LPS)经口暴露增加有关。不过也有研究指出,不同菌群产生的LPS类型存在差异,其中某些类型通过经典LPS受体TLR4引发炎症反应的可能性较低(24, 25),这与健康小鼠回肠中TLR刺激物浓度偏低的观察结果一致(26)。
据我们所知,目前鲜有研究系统性地探讨在数周时间内,通过口服途径给予小鼠LPS是否会影响高脂饮食引发的代谢与炎症反应。鉴于小鼠对LPS的耐受性高于人类,我们通过饮用水向采用高脂肪西式饮食(WSD)或标准低脂饲料(SC)的小鼠投喂了高剂量但具有生理相关性的大肠杆菌源LPS。我们的主要目标是确保小鼠面临显著的LPS刺激,并检验LPS能否诱导全身性的低度炎症。此外,我们提出假设:摄入高脂西式饮食会促进LPS向循环系统的易位,从而加速LPS暴露对低度炎症发生发展的影响。
我们的研究结果表明,肠道来源的LPS确实能够引发全身性炎症反应,但这种效应较为温和且短暂。长期暴露于LPS并未影响代谢稳态,这一点从小鼠正常的体重增长和血糖调节功能正常得以证实。因此我们得出结论:在生理相关条件下,当LPS的施用方式未超越肠道屏障相关的保护机制时,则不太可能主动参与促进代谢功能障碍和慢性低度炎症的发生。
结果
外源性LPS可抵达小肠,且小鼠持续口服耐受良好
我们首先评估了口服LPS的耐受性和接受度。将纯化的大肠杆菌LPS(0.33 mg/mL;约2 mg LPS/只/天)溶于饮水中给予小鼠,持续1、4或8天。通过每日观察和客观测量饮水量、体重变化及整体健康状况,均未发现LPS可能产生毒性作用的迹象。为验证口服LPS是否抵达肠道,我们采用mTLR4转染报告细胞(HEKBlue™ TLR4细胞)定量检测小肠腔内LPS含量。结果显示:与未暴露LPS的对照组小鼠相比,接受LPS处理组的小鼠小肠内LPS水平显著升高,且大约在LPS暴露4天后达到稳态浓度(十二指肠p=0.001,回肠p<0.001)(图1A)。
图1. HEK-Blue™TLR4检测法测定的LPS含量及小肠基因表达情况。
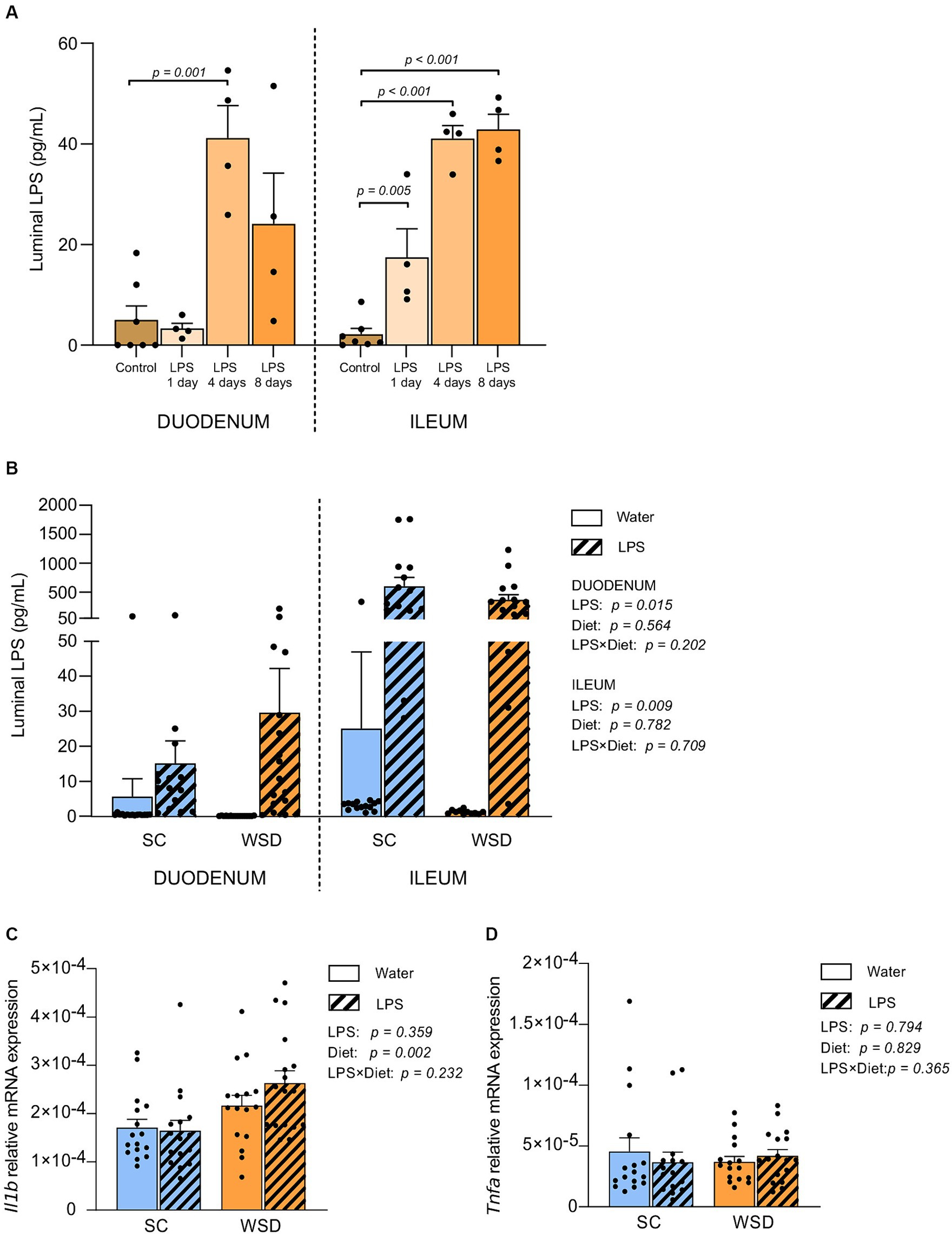
接下来,我们检测了长期口服LPS联合WSD实验中,小鼠肠道内具有生物活性的LPS(即能被HEK-Blue™-4细胞TLR4识别的LPS)水平。与未接触LPS的小鼠相比,连续35天口服大肠杆菌LPS后,两种饮食组小鼠的十二指肠(p=0.015)和回肠(p=0.009)腔内生物活性LPS水平均显著升高(图1B)。
西式饮食(WSD)而非口服LPS,可显著提升小肠黏膜中IL-1βmRNA的表达水平,但增幅较小。
炎症细胞因子是先天免疫细胞释放的信号蛋白,在调控微生物暴露引发的免疫反应中起关键作用。为探究回肠中升高的LPS水平是否会影响局部炎症细胞因子表达,我们对采用西式饮食(WSD)组和低脂标准饲料(SC)组进行了为期5周的LPS干预实验。通过检测回肠黏膜组织中TNFα和IL-1β的表达水平(32),结果显示:LPS处理对TNFα和IL-1β的表达均无显著影响(图1C、D)。但值得注意的是,与SC组相比,WSD组动物IL-1β基因表达出现统计学显著升高(p=0.002;图1C);而TNFα在WSD与SC饲喂组间未呈现表达差异(图1D)。
西式饮食(WSD)促进体重增长,但口服LPS对体重变化或摄食量无额外影响。
图2.评估小鼠在喂食WSD或SC饮食7周以及口服LPS给药35天(0.33 mg/mL,估计每只小鼠每日摄入2 mg LPS)期间的体重和食物摄入量。
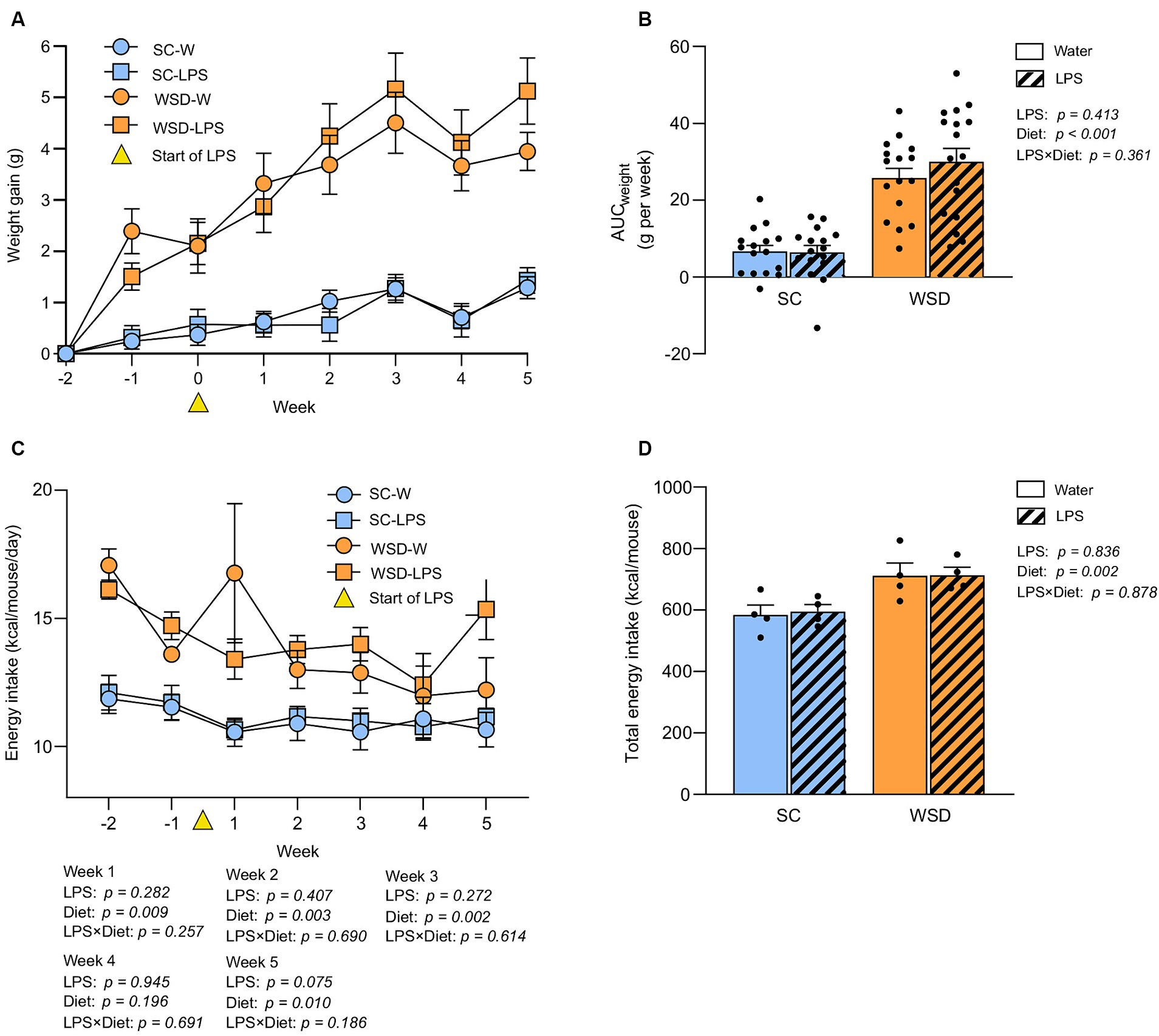
正如预期,在为期7周的饮食干预期间,采用西方饮食(WSD)的小鼠(WSD-W和WSD-LPS组)比采用标准饲料(SC)的小鼠(SC-W和SC-LPS组)体重增长更为显著(图2A、B,p<0.001)。然而,LPS处理对体重增长无显著影响(p=0.413)。总体而言,体重增长与总能量摄入相关——WSD组小鼠能量摄入高于SC组(p=0.002,图2D),而LPS处理对能量摄入亦无显著影响(p=0.836,图2D)。在整个实验过程中,接受WSD的小鼠每周能量摄入均最高(除第4周外各组无差异),且该现象与是否接触LPS无关(图2C)。
全身葡萄糖代谢与肠道IAP活性均未受口服LPS或西式饮食(WSD)的影响
图3.小鼠喂食WSD或SC饮食7周,并口服LPS (0.33 mg/mL,约每只小鼠每日2 mg LPS)35天的口服葡萄糖耐量试验(OGTT)与腹腔胰岛素耐量试验(IpITT)。
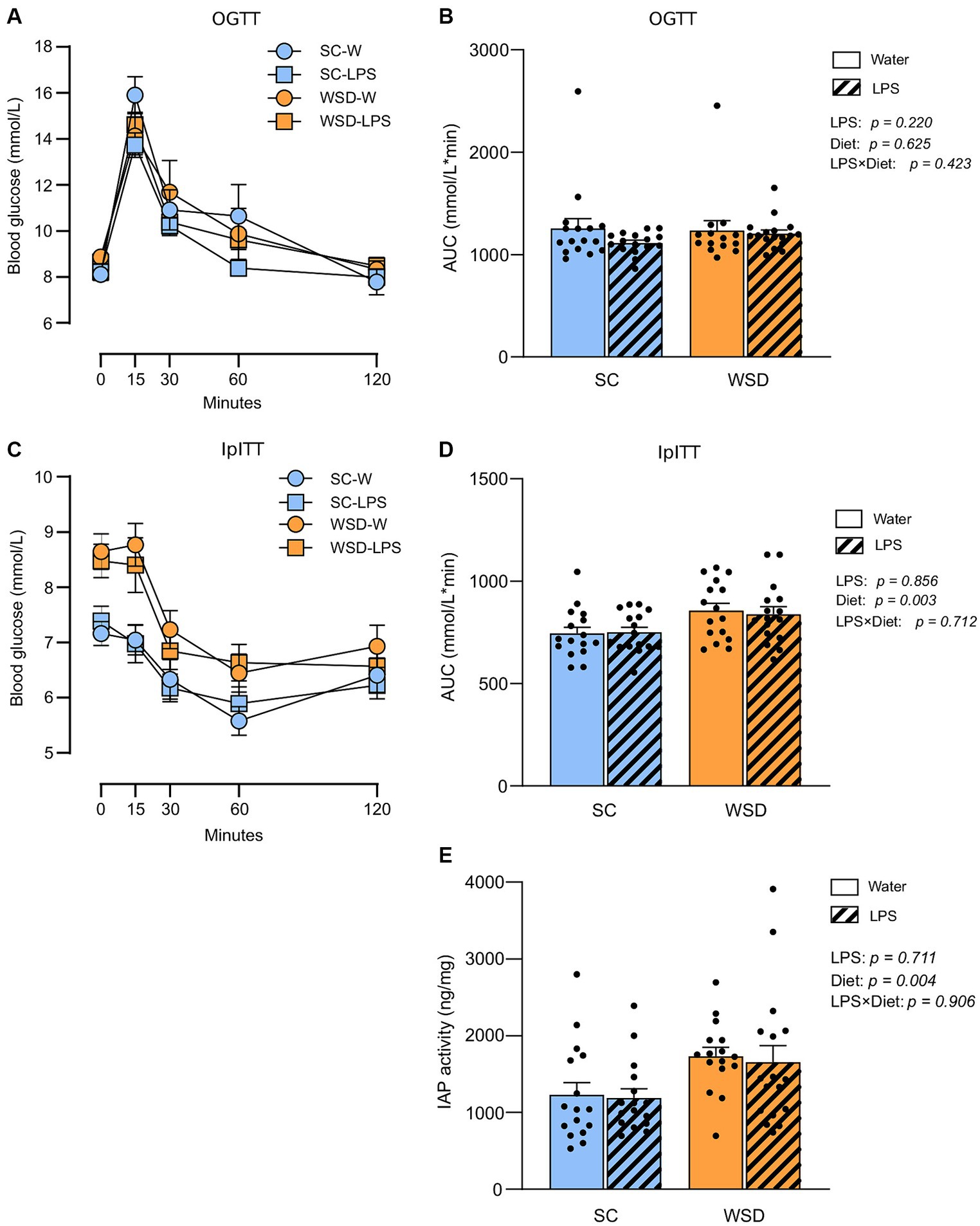
我们假设,长期口服LPS会升高血浆LPS水平并诱发胰岛素抵抗,因为这将充分挑战小鼠对LPS的耐受能力。为此,我们评估了长期口服LPS对血糖调控和胰岛素抵抗的影响。通过口服葡萄糖耐量试验(OGTT)和腹腔注射胰岛素耐量试验(IpITT)分别评估葡萄糖调节和全身胰岛素敏感性(图3A-D)。OGTT结果显示:不同饮食类型(p=0.625)或LPS处理(p=0.220)之间均未引起显著差异,饮食与LPS暴露的联合效应亦不显著(p=0.423;图3A,B)。在IpITT中,胰岛素注射后的葡萄糖曲线下面积(AUC)显示饮食类型有显著影响(p=0.003),其中高脂饮食(WSD)组小鼠的数值显著高于标准饲料(SC)组,但LPS暴露无显著影响(p=0.856),且两因素间无交互作用(p=0.712)。WSD喂养组观察到的AUC值显著升高,很可能源于进行IpITT时观测到的空腹血糖水平差异:与SC组相比,WSD组动物空腹血糖显著更高(单因素方差分析p=0.001)。
肠道碱性磷酸酶(IAP)通过去除脂质A部分的磷酸基团来解毒LPS,从而抑制LPS与TLR4的相互作用(33)。早期研究曾报道,高脂饮食喂养的啮齿动物中IAP活性升高(34-36),也有研究发现小鼠小肠腔内LPS浓度升高与IAP活性增强相关(37)。我们据此假设,随着肠腔内LPS水平升高(37, 38)以及高脂摄入(39),IAP分泌量会增加。但实验结果显示,LPS处理对IAP活性无显著影响(p=0.711),且饮食与LPS之间无交互作用(p=0.906)(图3E)。然而,与低脂SC组相比,高脂饮食组(WSD)的IAP活性显著更高(p=0.004)。
口服LPS与西式饮食(WSD)可短暂上调肝脏及腹部区域的NF-κB活性
转录因子NF-κB是炎症反应的主要调控因子,其激活与肥胖相关的促炎状态及胰岛素抵抗的有害影响密切相关(2,40)。我们假设,西方饮食(WSD)喂养的小鼠会表现出NF-κB信号通路的整体激活增强,而LPS暴露将进一步提升NF-κB活性。通过利用NF-κB活性的转基因报告模型(NF-κB luc)(27),我们采用活体成像技术,对所有实验组小鼠在整个实验过程中多个时间点的NF-κB活性进行了系列评估。
图4 .在饮用水中给予LPS(0.33 mg/mL,估计每日2 mg/只)35天期间的体内NF-κB激活的活体成像。第0天表示开始口服LPS给药。图表显示代表肝脏区域NF-κB活性的感兴趣区(ROIs)光子发射强度。
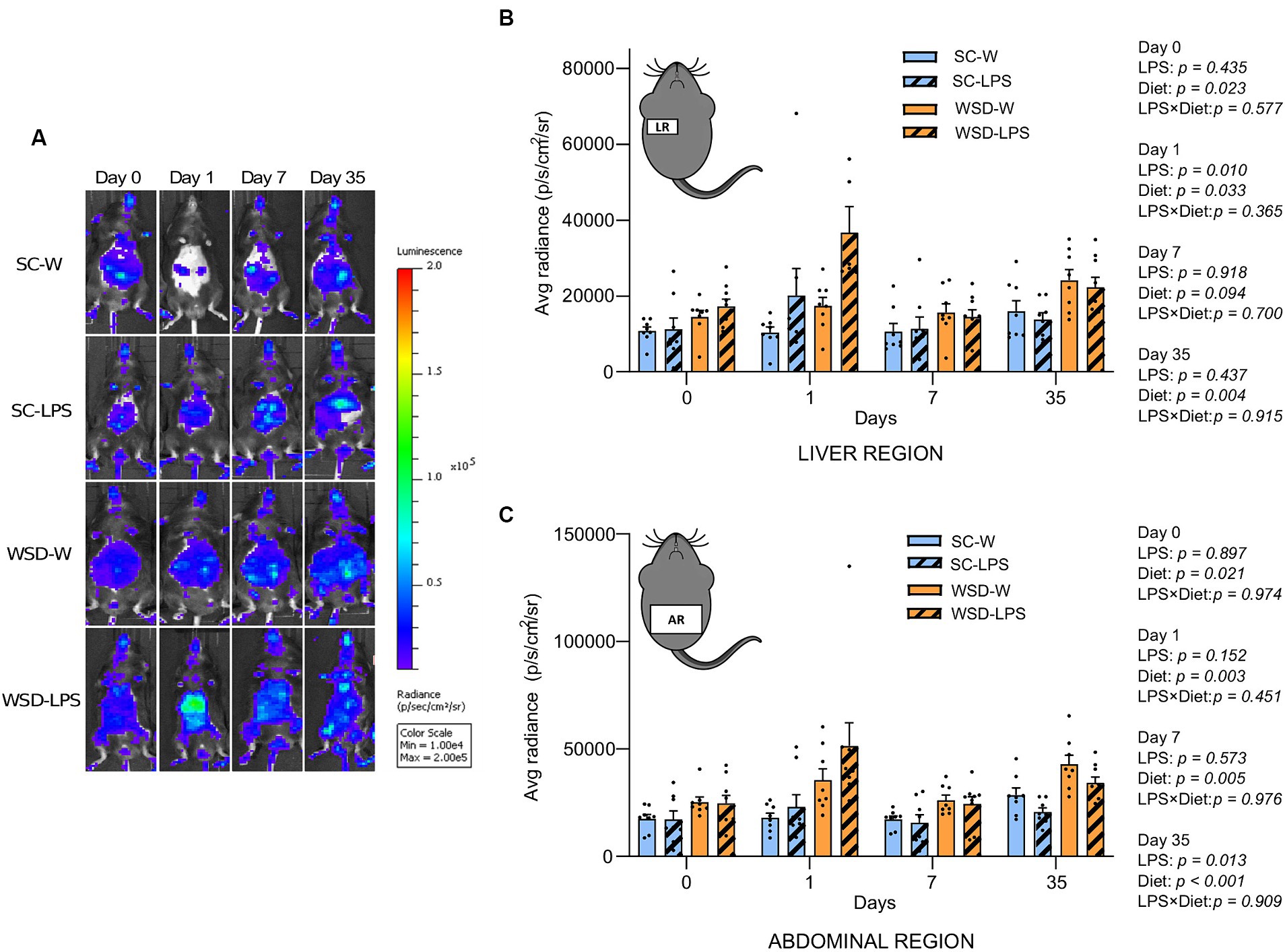
我们观察到,在口服LPS 24小时后,与仅接受纯水的小鼠相比,LPS组小鼠肝脏中的NF-κB活性出现显著且短暂的升高(p=0.010)(图4A,B)。此外,西方饮食(WSD)组在此时间点也显著增强肝脏NF-κB活性(p=0.033),但分析显示饮食与LPS之间未呈现交互作用(p=0.365),这意味着LPS诱导的肝脏NF-κB活性增强不依赖于WSD。通过各实验组间比较发现,仅SC-W组与WSD-LPS组存在显著差异(p=0.006),但在第1天(p=0.059)观察到两个WSD组间呈趋势性差异,一周后各组间未再观察到差异。然而在第35天,我们再次发现WSD组小鼠的NF-κB活性相较于SC对照组出现显著升高(p=0.004)。腹腔区域包含与肠系膜相连的肠道,肠系膜组织富含淋巴结,是肠道微生物物质进入淋巴系统的“首过”器官。这种对肠道腔内物质(如LPS)的直接暴露,可能触发淋巴免疫细胞中NF-κB的激活。我们的研究结果显示,在整个实验期间,WSD喂养的小鼠腹部区域的NF-κB活性持续升高(图4B),且LPS未引起额外增强。有趣的是,我们反而观察到LPS处理在第35天降低了腹部NF-κB信号(p=0.013),这引发了我们关于机体随时间的推移对LPS暴露产生代偿效应的推测。
图5 .血浆中LBP、IL-6、免疫球蛋白和LPS水平的检测结果。
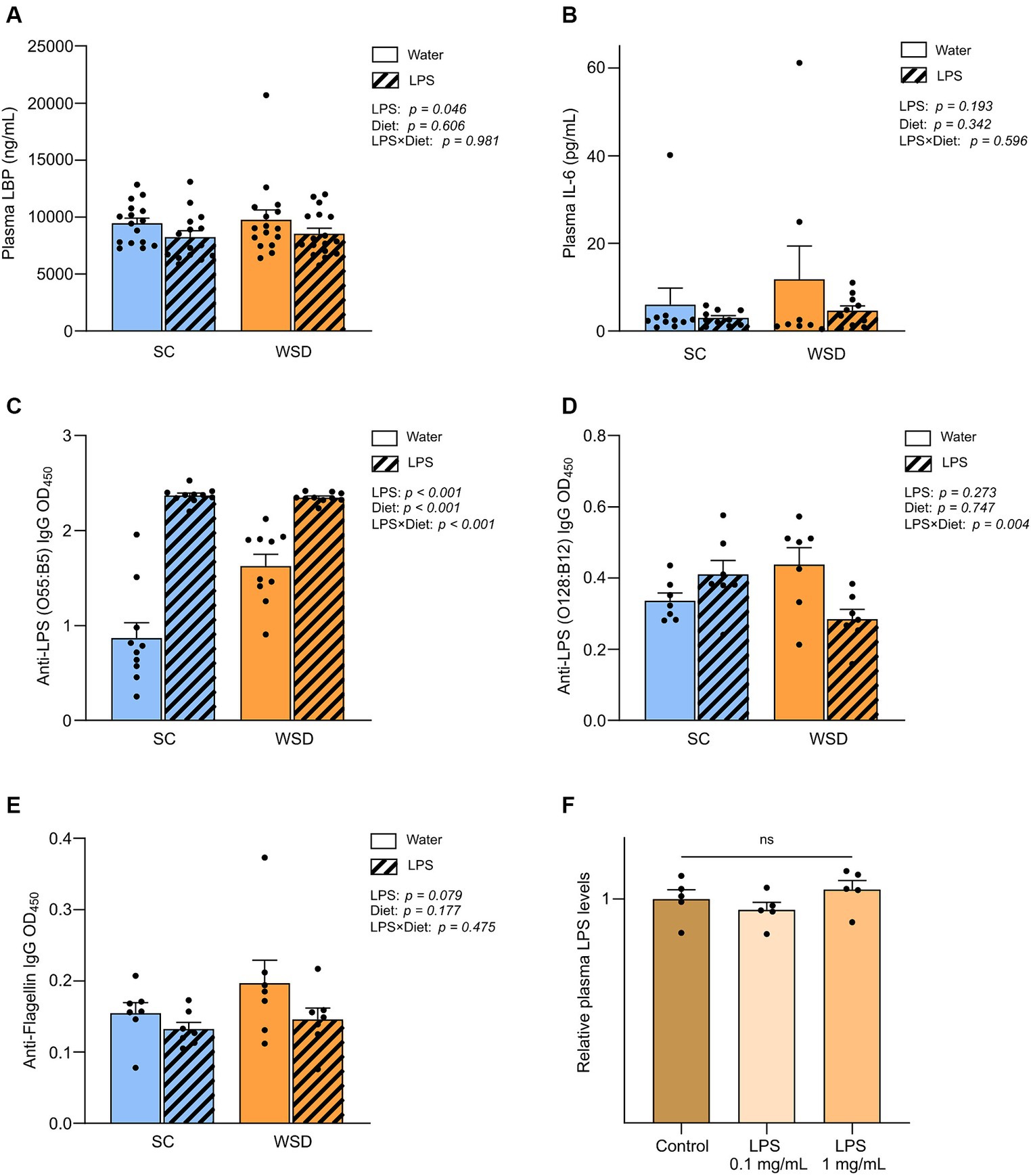
鉴于体内还存在独立于NF-κB活性的其他炎症通路,为探究不同处理对全身炎症的影响,我们检测了第35天的血浆IL-6和TNFα水平。结果显示,所有实验组小鼠的血浆IL-6水平均处于成年小鼠正常范围内(41, 42),且各组间未呈现显著差异(图5B)。而血浆TNFα因所有样本含量均低于检测限故无法进行定量分析。
口服LPS降低血浆中脂多糖结合蛋白水平,但循环中未检出LPS
脂多糖结合蛋白(LBP)在血液中稳定性强,且半衰期较LPS更长,因此被视为循环系统中LPS暴露的有效生物标志物(43–45)。血浆LBP测定结果显示:首先,饮食本身对LBP水平无影响(p=0.606)(图5A)。然而与假设相反的是,与未接触LPS的小鼠相比,LPS暴露导致循环LBP水平显著降低(p=0.046)。为深入探究LBP水平意外下降的现象,我们增设了一项小规模后续实验:在连续8天口服LPS(0.1 mg/mL与1 mg/mL,预估日摄入量分别为0.5 mg和5 mg)后,采用mTLR4转染细胞的比色分析法直接测定血浆LPS水平。由于所有样本检测值均低于检测限(0.001 ng/mL),我们未能成功量化任何组别的血浆LPS浓度,这表明LPS要么不存在于循环系统,要么处于结合状态,导致LPS分子无法与TLR4受体发生反应。组间平均值的相对比较显示,血浆LPS水平无显著差异(p=0.288)(图5E)。
口服LPS的动物体内抗LPS(大肠杆菌O55:B5)的血浆抗体水平升高,但细菌鞭毛蛋白抗体并未因口服LPS或西方饮食喂养而发生改变。
由于细菌蛋白鞭毛蛋白和LPS通常不会被肠道上皮吸收,当肠道屏障功能受损时,LPS和鞭毛蛋白可能穿过肠粘膜转移,从而激活适应性免疫应答,产生抗鞭毛蛋白和抗LPS抗体。鉴于鞭毛蛋白和LPS特异性免疫球蛋白G(IgG)的循环水平可作为长期系统性暴露于鞭毛蛋白和LPS的标志物,我们通过检测血浆样本中这些抗体的存在情况,间接评估长期肠道渗漏的情况。由于实验使用的是大肠杆菌血清型O55:B5来源的LPS,因此我们特别检测了针对该型LPS的抗体。同时,我们还检测了针对相关LPS(大肠杆菌O128:B12血清型)和鞭毛蛋白的抗体,后两者被选作肠道渗漏的代表性指标。结果显示,与对照组相比,口服LPS的小鼠体内抗大肠杆菌O55:B5 LPS的抗体水平显著且大幅升高(p<0.001)(图5C)。有趣的是,在比较不同饮食组和LPS暴露组时,针对LPS血清型O128:B12或鞭毛蛋白的抗体水平均未发生显著变化(图5E)。更引人深思的是,我们观察到口服LPS小鼠的抗鞭毛蛋白抗体水平实际上呈现低于对照组的趋势(p=0.079),这一发现与我们对LBP水平的观测结果相一致。
讨论
高脂肪、低纤维的西方饮食(WSD)与肥胖、低度炎症及血糖控制不良密切相关,这通常归因于“肠漏”假说——即肠道细菌或其代谢产物可能引发全身性炎症(6,46,47)。我们曾预期,WSD饮食中较高的脂肪含量会促进LPS穿过肠壁,导致饮用LPS水的小鼠引发全身性低度炎症。我们假设持续口服LPS会进一步加剧WSD的促炎效应,甚至可能在标准饲料(SC)喂养的小鼠中引发代谢性疾病症状。然而,在检测葡萄糖耐受性和胰岛素抵抗时,LPS补充并未对葡萄糖代谢产生任何不良影响。此外,除在口服LPS暴露第一天观察到LPS摄入小鼠的 NF-κB 活性出现短暂上调外,我们并未检测到明显的低度炎症迹象。这些发现与一项综合性的研究(涵盖小鼠和人类)结果一致,该研究探讨了口服LPS对肠道屏障功能和全身性炎症的影响(26)。该研究者发现,长期口服LPS会促进肝脏炎症,尽管其对能量摄入、体重增长、肠道炎症标志物、肠道屏障功能或通过 HOMA-IR 评估的血糖控制均未产生实质性影响。综上所述,我们的研究结果表明,对于摄入WSD或SC饮食的动物,存在于肠道内的LPS并不能引发全身性低度炎症。
目前,仅有少数研究探讨了高脂喂养模型中小肠LPS浓度与循环LPS水平之间的直接关联。除前述Faraj等人的研究(26)外,以及另一项与我们工作相关的研究:该研究给高脂饮食小鼠灌胃定植不同LPS表达强度(强或弱)的大肠杆菌。结果发现,仅大肠杆菌定植本身就会引发脂肪组织炎症并扰乱糖代谢调节失调,但这一效应并不依赖于LPS,这一发现与我们的研究结果在很大程度上相互印证(48)。然而,源自肠道的LPS仍被认为在代谢性内毒素血症和低度炎症中起着关键作用(4, 6, 49, 50)。我们对小肠腔内LPS含量的检测显示,无论是短期还是长期口服大肠杆菌来源LPS的小鼠,其腔内TLR4刺激物数量均显著增加;而未暴露组小鼠肠道中仅存在微量TLR4刺激物。这些发现可能表明,在我们的实验动物中,肠腔内大多数内源性LPS变体并非TLR4的有效激活剂,这一观察结果与其他研究结论一致,即正常肠道革兰阴性菌绝大多数属于拟杆菌科,这类菌群不会激活TLR4信号通路(24,25)。因此,在我们的实验体系中,摄入的大肠杆菌来源LPS确实促进了小肠内TLR4刺激环境的形成。
尽管我们在小鼠小肠中检测到大量LPS,但通过直接检测方法并未在血浆中发现具有生物活性、可激活TLR4的LPS。需要指出的是,目前大多数支持高脂饮食诱导代谢性内毒素血症的研究都基于鲎试剂法(LAL)的检测LPS评估结果(4, 6, 17)。该方法仅依赖脂质A组分的特性,并不能反映LPS通过TLR4信号通路诱发炎症的能力。这与我们采用的细胞实验方法不同。因此,LAL测试可能会高估实际水平,并且在建立循环LPS水平与代谢炎症的关联时容易产生误导,因为所检测到的LPS很可能无法激活人体内的促炎通路(51)。
为了进一步探究饮食和LPS暴露是否会引起肠道的其他异常,我们评估了细菌产物向循环系统的渗漏情况。为此,我们检测了血浆中针对以下成分的抗体水平:与饮水中所给完全相同的O55:B5血清型LPS;大肠杆菌来源的鞭毛蛋白;另一种大肠杆菌LPS(O128:B12)。后两者代表肠道细菌的普遍产物。既往研究曾在短肠综合征(SBS)和炎症性肠病(IBD)等慢性肠道疾病中,已观察到抗鞭毛蛋白和抗LPS Ig水平升高(31, 52)。由于直接在血液中检测鞭毛蛋白或LPS波动较大,以其特异性抗体作为长期暴露的标志,更能准确反映肠道长期渗漏(31)情况。结果显示,两组接受LPS的小鼠体内抗O55:B5 LPS抗体均显著升高,表明饮用水中的LPS确实以足够剂量进入循环系统,引发了针对该特定LPS的免疫应答。然而,该结果也提示,循环系统中的LPS随后被中和或激活了内毒素耐受机制。对于鞭毛蛋白和LPS(O128:B12),我们未观察到LPS给药导致抗体水平升高。这表明LPS干预导致肠道屏障功能普遍受损。相反,我们观察到投喂LPS的小鼠体内抗鞭毛蛋白抗体的生成量反而降低。综合实验结果表明,即使在高脂饮食条件下,口服LPS仅引起极少量LPS及其他细菌产物进入循环,且实验动物能迅速适应较高的LPS暴露,这表明其已形成获得性耐受机制。
支持“获得LPS耐受”这一观点的是意外发现的结果:表现为与未接受LPS的对照组相比,口服LPS小鼠的LBP水平意外降低。这一发现初看似乎矛盾,因为LPS会促进肝脏及其他组织(包括肠道)合成LBP(53–55),且外源性高剂量LBP已被证实可保护正常小鼠免受LPS攻击(56)。我们推测,低LBP水平可能是长期LPS给药引发获得性耐受的结果,这在急性与慢性LPS暴露的大鼠模型中已得到验证(57)。内毒素耐受被定义为细胞在初次接触LPS刺激后,再次遭遇同类刺激时反应能力减弱(58, 59)。这一概念最初被提出时,研究重点主要集中在低剂量LPS处理如何预防败血症和发热的致命后果。随着对多种慢性炎症性疾病(60,61)及癌症免疫治疗(58,62)等特定领域更具体的研究深入,我们对其有了更全面的理解。内毒素耐受可分为早期与晚期两种机制。早期耐受通常在LPS处理后数小时内出现,可持续约一周,其机制涉及细胞活化状态改变,表现为抑制细胞因子产生,且不依赖抗体生成(63,64)。相比之下,晚期耐受则在LPS治疗开始数天后、早期耐受通常已消退时出现。内毒素耐受的分子特征包含多种机制,如TLR4表达下调和NF-κB信号通路中间激活物减少(58)。此外,多种负调控分子(如IRAK-M、A20)在内毒素耐受细胞中表达上调,从而抑制TLR信号通路的激活发挥作用(58,65,66)。除上述机制外,研究显示免疫刺激型LPS暴露可通过调节免疫系统反应性,为预防免疫介导疾病提供保护(25)。根据"卫生假说",生命早期暴露于强效免疫激活型LPS可通过内毒素耐受实现免疫教育,相比暴露于低炎症亚型LPS,能更有效预防自身免疫性疾病。
若在LPS暴露起始阶段就检测LBP浓度,我们可推测其水平在急性应激(如LPS攻击)后的初始阶段会因保护机制而升高(53),随后因LPS耐受形成而下降。此外,我们的研究结果表明,血浆LBP水平完全不受所分配的饮食类型及小鼠最终体重的影响,这与诸多报道“高脂饮食会提升血液LBP水平”的研究形成反差(16, 37)。然而,一项人类干预研究与我们的观察结果一致:尽管高脂饮食导致体重显著增加,但LBP水平却并未升高(11)。
关于十二指肠IAP酶的研究,我们最初假设,口服LPS暴露后该酶活性会增强,以抵御LPS的毒性作用(38,67,68)。但出乎意料的是,尽管小肠内LPS水平相较于未暴露组动物有所升高,但十二指肠的IAP活性并未因长期LPS暴露而受到影响。相反,我们观察到,在未暴露于LPS的情况下,西式饮食(WSD)喂养的小鼠小肠IAP活性显著高于标准饲料(SC)喂养的小鼠。既往研究表明,IAP可调节肠道脂质吸收(34, 69, 70),并能抑制高脂饮食小鼠的体重增长(69)。此外,高脂饮食小鼠的IAP表达量确实会增加,但部分研究表明,这种适应性机制似乎不足以抵消高脂饮食诱导的LPS肠道易位(33,70)。
NF-κB是一类调控炎症反应的关键转录因子,对脂多糖(LPS)具有高度敏感性。我们观察到,在接受WSD-LPS饮食的小鼠肝脏中,仅在喂食期一天后就出现了NF-κB激活的短暂炎症诱导。本研究使用的转基因NF-κB小鼠对LPS含量的微小变化极为敏感,通过生物发光成像技术可检测到0.1–0.4 ng/mL范围内的LPS水平(未发表数据)。这表明,若经口摄入的LPS进入血液循环,其在5周时的水平应低于 0.1 ng/mL,这与我们使用 HEK-Blue 法(检测限 0.001 ng/mL)直接在血浆中未检出LPS的阴性结果相符。实验后期两个WSD组均出现的NF-κB活化增强,是否意味着初期非全身性的低度炎症启动,目前我们仅能推测。该假说部分得到另一项 C57BL/6 小鼠研究的支持:该研究显示高脂饮食引发的炎症反应分为两个不同阶段——最初几天内出现急性期反应,随后在 12–16 周后再次增强,并与白色脂肪组织和肌肉炎症相关(71)。研究者提出,初始反应源于急性且短暂的炎症及肝细胞激活,这与我们的发现相符。鉴于尚存在不依赖 NF-κB活化的其他炎症通路,我们进一步检测了两种核心促炎细胞因子——TNF-α 和 IL-6 的血浆水平。结果再次支持了我们的总体结论:未发现存在持续的低度全身性炎症的证据。
我们的实验结果表明,无论是否伴随高脂饮食,口服LPS均不会损害肠道屏障功能或引发慢性低度全身性炎症。为降低实验因素可能引发局部肠道炎症进而发展为低度全身性炎症的风险,我们通过检测小肠黏膜促炎细胞因子的基因表达水平来评估肠道炎症状态。已有研究发现,在小鼠肠道炎症模型中,TNFα和IL-1β在急性期具有保护作用,但在炎症后期则表现为纯促炎功能(32)。除高脂饮食与LPS作用机制的研究外,对于肠道屏障功能受损的受试者(如克罗恩病或溃疡性结肠炎等炎症性肠病患者),肠道内LPS或其他细菌产物渗漏很可能对全身性或低度全身性炎症产生显著影响(见引言)。既往研究已证实,无论是接触西式饮食(72,73)还是肠道LPS(74,75),都可能通过多种机制加剧肠道炎症。但我们在评估小肠黏膜局部炎症状态时,并未发现西式饮食喂养或口服LPS会引起肠道免疫防御相关促炎因子发生变化。
我们的研究结果并未排除LPS从肠道进入循环系统的可能性,但结果表明动物的防御系统能有效应对入侵的LPS,并阻止或延缓低度全身性炎症的发展。需要强调的是,这些实验小鼠处于代谢健康状态,且很可能具有健全的肠道屏障。代谢综合征及相关疾病的特征在于血脂异常状态。最新研究表明,LPS是脂质代谢领域的重要调节因子,如调控血浆脂质水平(76)和激活胆固醇代谢过程(77),进一步将LPS与血脂异常和全身性炎症联系起来。尽管我们的研究结果表明几乎未出现代谢紊乱,但本研究的局限在于未探讨LPS对脂质代谢的影响,也未检测持续炎症的标志物(如肝脏基因表达或血浆相关生物标志物)。另有观点认为,现代生活方式中的其他因素,如摄入富含特定食品添加剂(乳化剂等)的加工食品,可能导致"肠道渗漏",进而引发心血管疾病、癌症和2型糖尿病等生活方式相关疾病(30, 78)。因此,长期摄入不健康饮食时,肠道对细菌或其他外来分子的通透性失控增加,可能在疾病发展过程中起重要作用。然而,本研究为肠道黏膜对促炎性LPS与膳食脂肪暴露的耐受水平提供了新见解,表明驻留于肠道内的LPS可能不似宣称的那般有害。未来需进一步研究以阐明LPS暴露后免疫应答恢复的机制。
免责声明:
以上部分内容来源于外网我们重在信息分享,版权归属原作者或原刊发平台所有,如有侵权、信息有误或其他异议,请联系处理,我们将在24小时内删除或整改。
复合免疫 健康活力





























