
Fn-LPS共定位:滑膜中一种调控“骨关节炎症”稳态的新型保护机制!
评估LPS在关节中的作用:纤维连接蛋白作为一种新的保护机制
在骨关节炎的研究中,炎症机制与关节退行性变化长期以来备受关注。脂多糖(LPS)作为众所周知的强效炎症激活剂,长期被视作潜伏的“纵火犯”,但其在关节疾病中的作用却尚未明确。传统观点倾向于将LPS视为可能的炎症驱动因子,然而,其在人体关节腔内的实际活性和调控机制仍存在争议。我们的最新研究揭开了滑膜组织里一道隐秘的“防火墙”:纤维连接蛋白(Fn)。
本研究通过对大量临床样本的系统分析,结合体内外实验,借助56例OA、类风湿与创伤患者的滑液图谱、大鼠32天全身挑战以及3D滑膜模型,我们首次证实,LPS并非关节退变的直接主谋;相反,Fn-LPS共定位形成的新型保护轴,才是决定炎症状态的“隐形开关”。
纤维连接蛋白(Fn)作为一种关键的中和因子,在滑膜环境中通过与LPS结合、限制其迁移与炎症效应,发挥新型保护机制的作用。这一发现不仅挑战了以往对LPS在关节中作用的传统认知,也为针对LPS精准调控的炎症防治策略提供了新的理论基础与潜在靶点。
评估LPS在关节中的作用:纤维连接蛋白作为一种新的保护机制
摘要
目的:研究骨关节炎(OA)患者滑液(SF)中脂多糖(LPS)的存在及其生物活性,并阐明调控其炎症潜能的作用机制。
方法:对56例骨关节炎(OA)、7例类风湿性关节炎及39例创伤患者的滑液样本进行分析LPS浓度和生物活性。采用液相色谱-质谱联用技术(LC-MS)检测脂质A成分。通过大鼠模型进行为期32天的全身性LPS给药,评估其对关节退变的影响。采用体外实验和3D滑膜模型,研究LPS与滑膜蛋白(尤其是纤维连接蛋白Fn)的相互作用。
结果:
在所有滑液(SF)样本中均检测到LPS,且各组间浓度和脂质A谱特征相似。液相色谱-质谱(LC-MS)检测表明,其LPS含量高于标准内毒素测定结果,提示传统检测方法存在局限性。尽管LPS含量升高,但生物活性检测却显示其促炎反应微弱,表明滑液(SF)中可能存在中和LPS的内在因子。体内实验表明,长期全身暴露于LPS并未诱发大鼠关节类似骨关节炎(OA)的病变。值得注意的是,LPS与纤维连接蛋白(Fn)在滑膜中呈现共定位现象,体外实验显示,Fn结合可显著降低LPS生物活性并抑制其迁移。
结论:
脂多糖(LPS)普遍存在于各种关节疾病的滑液(SF)中,但其生物活性较低,表明LPS并非关节炎症的主要驱动因素。纤维连接蛋白(Fn)在滑膜环境中通过捕获并中和LPS发挥关键作用,形成对抗LPS诱发炎症的保护机制。这些发现不仅凸显了精准检测LPS技术的重要性,更为调控关节炎症提供了潜在治疗靶点。
引言
脂多糖(LPS)又称内毒素,是革兰氏阴性菌细胞外壁的组成部分。其结构由保守的脂质A(将LPS锚定在细胞壁上)和结构多变的多糖表面层组成(1)。不同细菌种类和菌株的LPS存在差异,这些结构变异会影响宿主的炎症反应,并可用于鉴定LPS从其中脱落的细菌种类(2)。脂质A是LPS的主要免疫刺激区域,能强烈激活Toll样受体4(TLR4)(3)。当被激活时,它会触发激活的B细胞的核因子κB(( NF-κB)向细胞核的转移,从而引发先天免疫信号级联反应(4)。NF-κB信号通路参与关节炎的病理过程(5)。当肠道通透性增加时(8,9),LPS可从肠道转移至血液中(6,7)。
已有研究表明,血液中的LPS水平与关节炎存在相关性(10-12)。骨关节炎(OA)和类风湿性关节炎(RA)是两种不同的关节疾病,但均会导致关节功能受损。骨关节炎是一种由炎症与机械损伤相互作用引发的慢性多组织病变,而类风湿性关节炎则属于系统性自身免疫性疾病(13),这两种疾病均会显著降低患者的生活质量(13–15)。Loeser等人分析了骨关节炎患者和健康对照组的血清样本,发现骨关节炎患者的血清中的LPS水平升高,但未观察到LPS浓度与关节疼痛之间的相关性(16)。相反,另有研究指出血清中的LPS浓度与膝关节间隙变窄的放射学表现(11)、膝关节骨赘的严重程度以及滑膜巨噬细胞数量存在关联(12)。文献表明,骨关节炎患者肠道通透性增加(17)会导致血浆中LPS浓度升高(12),这可能与骨关节炎病理机制相关(11 ,12)。同样,类风湿性关节炎患者的血清LPS生物活性与疾病活动度及缓解可能性相关(10)。
目前关于滑液(SF)中LPS的研究甚少,而该领域在骨关节炎(OA)的发病机制中具有重要作用(18 19)。已有研究表明,骨关节炎患者的滑液中存在LPS,且其含量与膝关节骨赘严重程度及WOMAC总评分相关(12)。Kasperkiewicz等团队也曾在幼年特发性关节炎患者的滑液中检测到抗LPS抗体(20)。然而,据我们所知,目前尚未有研究将滑液中的LPS浓度与任何对照组进行比较,也未曾探究其生物活性。血清和滑液中LPS的存在及其与关节炎病理的相关性,表明其可能在关节炎症中发挥作用。然而,内毒素血症以及关节内LPS对关节炎症或退变的直接影响,目前仍缺乏明确结论。
由于LPS是免疫系统的强效激活剂且广泛存在,血清和肝脏中存在能够降解LPS并抑制其生物活性的酶与蛋白质(21)。抵抗素(Resistin)以及高浓度的LPS结合蛋白(LBP)和可溶性TLRs已被证实能阻断血清中LPS介导的炎症反应(22–24)。我们推测滑液(SF)中也可能存在类似的保护机制——因为滑液是血浆的超滤液(18),且在骨关节炎(OA)患者的滑液中已发现可溶性TLRs水平升高(25)。滑液中另一影响细菌粘附和毒力的成分是纤维连接蛋白(Fn)(26-28)。Fn存在于健康滑液中,并在骨关节炎(OA)滑液中显著升高(26,29)。在关节炎研究中,瓜氨酸化Fn及其片段已被证实具有促炎特性(30-33),但其在关节内与LPS的相互作用机制仍有待探索。
我们假设:LPS可能参与关节炎症过程,但其生物活性可能受滑液(SF)中某些因子的调控。为了将该研究应用于临床,我们定量并比较了终末期膝骨关节炎(OA)患者与创伤性膝关节损伤患者滑液中的LPS水平及生物活性。同时,我们通过体内实验,验证了诱导内毒素血症对膝关节软骨降解、骨赘形成和滑膜炎的影响。此外,我们还深入探究了滑液中可能存在的LPS效应保护机制。
研究参与者
本研究共招募了103名年龄在18–90岁之间的受试者,纳入标准如下:
骨关节炎(OA)组:骨关节炎患者(男性和女性)接受全膝关节置换术;
类风湿关节炎(RA)组:类风湿性关节炎患者(男性和女性)需确诊为类风湿性关节炎;
创伤组:受试者无骨关节炎或类风湿性关节炎诊断,但存在因创伤性损伤导致滑液渗出和手术中需清除滑液/软骨/滑膜的患者;
若受试者同期接受其他治疗、患有感染或非风湿性全身炎症性疾病,则予以排除。所有入选样本均进行了多项分析(表1)。
表1.患者临床数据
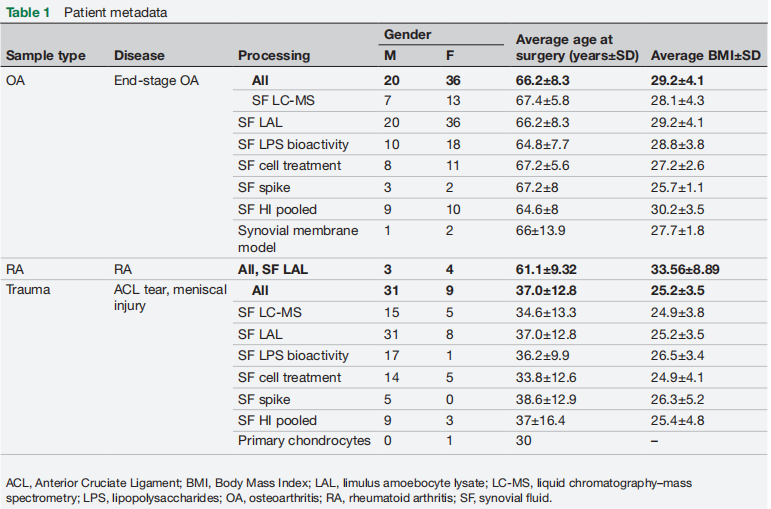
结果
在人类关节炎和创伤性膝关节滑液(SF)中发现高浓度但低生物活性的LPS
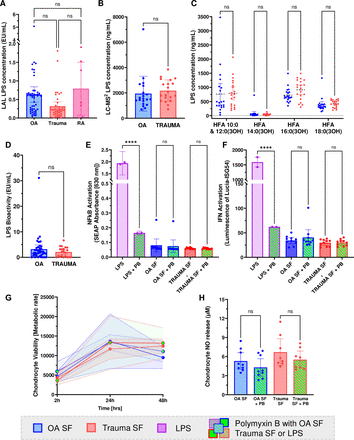
我们采用液相色谱-质谱联用技术(LC-MS)对膝骨关节炎(OA)和创伤性膝关节滑液(SF)中的总LPS浓度进行定量分析,并依据脂质A的羟基脂肪酸链(HFA)组成分析了LPS类型。两组的LPS浓度无显著差异:骨性关节炎组平均LPS浓度为1942 ng/mL(95%CI 2584.5至1299.5),创伤组平均LPS浓度2172.3ng/mL(95%CI 2573.7至1770.9)(图1B)。所有纳入变量(疾病类型、年龄、性别、体重指数BMI)均未显示与LPS浓度存在统计学显著关联(所有预测因子p>0.3),表明研究组间的人口统计学差异未对患者分组与滑液LPS水平的关系造成干扰(图S1)。LC-MS测得的浓度高于标准内毒素定量试剂盒的检测结果(图1A,B)。使用标准内毒素定量试剂盒检测时,创伤组、骨关节炎组和类风湿性关节炎组膝关节滑液的LPS浓度未观察到显著差异(图1A)。两种技术的检测结果无相关性(图S2,S3)。骨性关节炎组与创伤组在脂质A HFA(反映细菌种属来源)的数量和组成上均无显著差异(图1C)。值得注意的是,在大肠杆菌中常见的14:0(3OH)型HFA的LPS在两组样本中含量最低,而16:0(3OH)、10:0及12:0(3OH)型HFA含量最高(图1C,图S4)。随后,采用HEK TLR4报告细胞检测滑液中LPS的生物活性。细胞对LPS的反应浓度比LC-MS定量值低1000倍(图1B,D)。骨关节炎组与创伤组滑液的LPS生物活性无差异。为深入评估滑液LPS的细胞反应,我们用添加或不添加多粘菌素B(PB)的滑液处理THP1报告细胞24小时。PB可结合并中和LPS,从而区分LPS与SF中其他潜在TLR激活分子的效应。与PB处理对照组相比,未观察到NF-κB信号通路或干扰素激活的显著上调,且两组患者间也无显著差异(图1E,F)。此外,我们在原代人软骨细胞中重复该实验发现:与滑液+PB处理组相比,滑液LPS对软骨细胞活力和一氧化氮(NO)释放均无显著影响(图1G,H)。
图1.低炎症活性的LPS存在于人类SF中。
内毒素血症不会加速体内膝关节退变
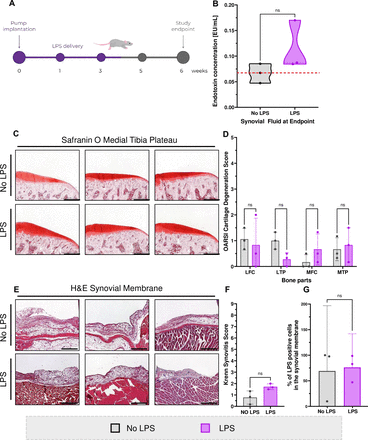
我们在Wistar大鼠皮下植入可释放LPS的微量泵,持续32天以诱导建立内毒素血症模型,并研究观察其对滑液LPS浓度及膝关节退变的影响(图 2A)。通过采集大鼠膝关节滑液测定LPS浓度发现:与对照组(0.07 EU/mL,95% CI 0.02-0.11)相比,LPS组关节内LPS浓度略有升高(平均值:0.11 EU/mL,95% CI -0.01至0.23),但差异无统计学意义(p=0.20)(图 2B),这表明滑液阻断LPS的能力在大鼠和人类中具有保守性。我们对股骨和胫骨标本进行番红O染色包埋,并采用OARSI软骨退变评分系统进行组织学分级评估。所有样本均未观察到明显软骨退变,且各骨骼区域样本评分均未超过5分量表中的2分(图2C,D)。根据Krenn滑膜炎评分标准,LPS组未出现滑膜炎(平均值:1.72,95% CI 1.09-2.35),其评分与对照组相近(平均值:0.78,95%CI −0.67至2.22;p=0.10)(图2E,F)。两组滑膜组织中LPS+细胞百分比亦无显著差异(图 2G)。所有大鼠均未出现骨赘。通过µCT扫描测量软骨下骨厚度和小梁骨体积,除胫骨内侧平台骨体积占总体积百分比外,其余骨参数均无显著变化(图S7)。
图2.内毒素血症不会加速体内关节退变。
滑膜中的纤维连接蛋白(Fn)层可结合LPS并阻止其迁移
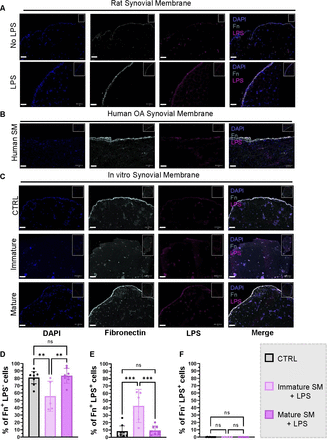
LPS的功能之一是通过在细菌外表面提供电荷,从而影响表面黏附及生物膜形成(41)。纤维连接蛋白(Fn)常见于滑液(SF)中,已被证实可抑制细菌对关节假体的黏附(42)。Fn作为普遍存在的分子,广泛分布于滑膜组织中。我们通过免疫荧光染色技术,对大鼠及人类骨关节炎(OA)滑膜组织进行LPS与Fn的联合检测,结果显示LPS存在于滑膜中并与Fn在内衬层形成共定位(图3A、B)。在衬里层未检测到任何不与Fn共定位的LPS(Fn⁻LPS⁺),且LPS处理组与对照组之间无显著差异(图S10)。为验证“滑膜内衬层的Fn层可作为LPS屏障”这一假说,我们从3例骨关节炎(OA)患者中分离滑膜样成纤维细胞,构建3D人体滑膜组织模型(图S9,表S2),分别培养7天(未成熟组,无Fn衬里层)和20天(成熟组,形成与天然滑膜相似的Fn层)(图3A,C)。经LPS处理6小时后对样本进行LPS与Fn染色检测,结果显示:LPS不能穿透具有成熟Fn层的构建体,但可穿透无Fn层的未成熟构建体(未成熟组vs成熟组p=0.0005;对照组vs成熟组p=0.9821)(图3E,F)。
图3.关节滑膜中的纤维连接蛋白层结合LPS并阻止其迁移。
Fn可以结合LPS并阻断其生物活性
为了验证Fn是否能直接与LPS结合,我们通过微量热泳动技术进行了结合亲和力检测,结果显示这两种分子可以发生化学结合(图S6,表S1)。为探究这种结合对LPS体外生物活性的影响,我们用LPS和Fn处理THP1细胞。我们采用两种处理方式:同时加入两种分子或预混合后再加入细胞。由于已知某些Fn结构域是TLR4激动剂(40),我们需要区分其分别与TLR4和LPS的结合作用。即使经过预混合处理,Fn仍能作为TLR4的部分激动剂发挥作用。在两种实验处理条件下,Fn均能降低LPS依赖的NF-κB活化(LPS组0.14A,95%CI 0.1-0.18;LPS+Fn组0.1A,95%CI 0.06-0.14;p=0.01),尤其在预混合条件下效果最显著(0.07A,95%CI 0.06-0.08,p=0.0004),这表明Fn具有直接结合LPS的能力(图4A)。进一步实验显示,Fn的热失活处理,降低了其在THP1细胞中抑制LPS依赖性NF-κB激活的能力,表明这种结合具有空间构象依赖性(图4B)。为研究LPS与Fn的相互作用,我们通过计算机模拟分析,预测其结合位点。结果显示,大肠杆菌B6型LPS结合在Fn的III结构域的亚基间区域,其中吉布斯自由能为-4.9 kcal/mol的结合位点被列为最优结合位点(图4C,D,图S11)。进一步实验证实,Fn的III结构域可单独结合LPS——当单独使用时,与LPS预混的THP1细胞中LPS依赖性NF-κB激活水平显著降低(p=0.0002),这有力佐证了该结构域的功能活性(图4E)。
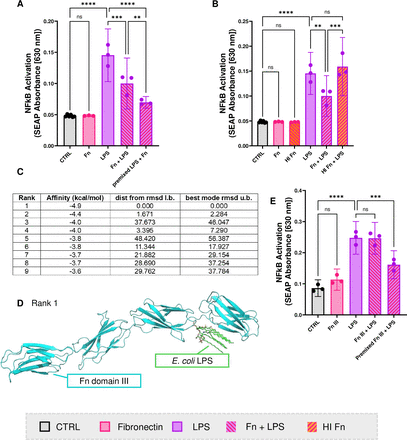
图4.纤维连接蛋白结合LPS并阻断其生物活性
讨论
本研究发现,关节炎(骨关节炎、类风湿性关节炎)与创伤性损伤患者的滑液中LPS浓度相当(图1A,B),这表明LPS天然存在于滑液中。通过液相色谱-质谱联用技术(LC-MS)分析脂质A高丰度脂肪酸(HFA)组成的分析显示,创伤组与骨关节炎组的成分一致(图1C),表明两组中LPS来源的菌门类及修饰过程具有相似性。大肠杆菌来源的高免疫原性脂质A(HFA 14:0(3OH))在两组中的浓度均处于最低水平,这与我们体外实验数据相印证——滑液中的LPS生物活性较低(图1D)的结论。值得注意的是,通过液相色谱-质谱联用技术测得的LPS水平显著高于既往内毒素定量检测报道的数据(12),且与本研究采用相同方法测得的数据高度吻合(图1B)。这表明,人体滑液中LPS的总量虽然极高,但经过修饰后被阻断,无法在相同浓度下被细胞或内毒素定量检测中的酶系统所识别。这两种检测方法采用不同的计量单位,为便于比较,需注意根据FDA建议(43),1 EU/mL约等于0.1–0.2ng/mL。值得注意的是,标准内毒素定量试剂盒基于鲎试剂(LAL)检测法,目前尚不清楚凝血酶对LPS的识别如何转化为生理相关性。这些酶无法检测所有类型的LPS,且对不同LPS的反应强度各异,因此LAL法并非LPS检测的精确方法(图S1和S3)(44)。此外,AL法在诊断革兰氏阴性菌脓毒症时会出现假阳性反应,因其会对β-葡聚糖而非LPS产生反应(45)。这些矛盾数据导致FDA至今未批准将LAL检测法用于血液内毒素检测。
值得注意的是,LPS生物活性检测显示其浓度比LC-MS法低1000倍(图1A、D)。这种低生物活性是由已知机制引起的:包括肝脏酶对LPS的分解(21)以及血浆因子的阻断作用(46)。我们的研究数据显示,滑液同样具备阻断LPS的能力(图1A-F)。我们通过HEK TLR4报告细胞检测生物活性,并利用野生型THP1细胞研究细胞反应,从而更全面地了解细胞响应机制。THP1细胞对滑液LPS未表现出NF-κB和干扰素应答反应(图1E,F)。此外,滑液经热灭活处理后,在阻断LPS检测和抑制炎症方面的能力显著下降(图S5)。这表明某种热敏蛋白可能正在掩盖或阻断LPS的检测。结合天然滑液样本未能引发强烈免疫反应的现象,这表明滑膜蛋白(s)通过蛋白质介导的方式掩盖了LPS,同时证明了人源滑膜液阻断LPS炎症效应的潜力。
与上述结果一致,我们的体内实验表明诱导内毒素血症并不会加速健康大鼠类OA样的膝关节破坏。数据显示LPS被有效中和且生物活性受损——与对照组相比,处理组血浆和滑液中仅观察到小幅度的LPS浓度上升(图2B,图S6)。此外,LPS处理组并未出现OA样症状,软骨和滑膜组织均未受到显著影响(图2C-G)。两组的临床评分均显示关节组织未发生退行性病变;但由于实验动物数量有限,统计分析效能较低。本研究亦不排除LPS可能在已受损关节中加剧潜在炎症的可能性。
通过进一步研究LPS阻断因子,我们发现LPS与纤维连接蛋白(Fn)在大鼠滑膜中存在共定位现象。该现象在人类骨关节炎滑膜组织中也得到验证(图3B)。在三维滑膜模型中,我们观察到富含Fn的滑膜层可能形成屏障,有效阻止LPS迁移(图3C-F),并通过隔离或间接相互作用降低其促炎潜力(图4A-D及图S10,S11)。值得注意的是,经预混LPS-Fn复合物处理的单核细胞,其促炎反应强度显著低于单独使用LPS刺激的单核细胞(图4A),这表明LPS与Fn的共定位对滑膜细胞功能影响有限。本研究报道的Fn新型保护功能令人意外——鉴于既往研究认为,只有当Fn以碎片化形式存在时才会参与骨关节炎的病理过程(47)。图4E显示,未与LPS预孵育时,单独使用Fn的III结构域无法有效抑制NF-κB活化,提示裂解型Fn可能削弱其抑制LPS介导NF-κB活化的能力。但Fn已被证实在细菌感染中发挥作用(27),表明其与LPS存在关联。我们推测滑液中的Fn(26)可能是隔离LPS并降低其促炎活性的因子之一。我们提出假说:LPS会持续结合滑膜中的可用Fn直至达到平衡状态,因此Fn在组织中的保护效应可能存在剂量依赖性关系。我们不能忽视LPS与已知的TLR4激动剂Fn EDA结合后,可能增强或加剧其促炎活性的可能性。虽然LPS也可能诱导Fn自身的转录,但我们的大鼠模型中并未观察到内毒素血症组Fn表达升高。既往研究表明,LPS可刺激Fn受体生成,从而促进单核细胞向组织迁移并与基质中的Fn结合(48,49)。LPS通过肠道通透性介导从肠道转移至关节(50),该机制已被证实在骨关节炎(特别是代谢性OA)中发挥作用(9,51)。鉴于Fn在肠道上皮中大量存在,并且通过与CD137、CD36的相互作用影响肠道通透性(52 ,53)。因此,Fn与LPS之间的关联相互作用可能进而调控“肠道-关节轴”。若Fn表达紊乱,可能影响其在肠道及关节中的保护作用。我们希望本研究能激发更多关于LPS与Fn之间复杂生物学关系的探索。
本研究存在以下局限性:首先,缺乏健康人体滑液(SF)样本作为对照,若能获取此类样本,将有助于我们判断LPS渗入究竟是损伤与退变驱动的过程,还是健康关节中普遍存在的正常生理过程。虽然使用创伤样本作为对照组存在人口统计学差异的缺陷,但这些样本不存在慢性炎症状态,且混杂因素对滑液中LPS浓度的影响无统计学显著影响(图S1)。另一局限性在于LPS定量方法,我们对比了两种已发表的LPS检测方案,发现其结果存在显著差异。这不仅提出了关于选择合适检测方法的必要性,更期待能激发更多研究者在样本筛选上精益求精。
总体而言,我们的研究结果表明:高分子量纤维连接蛋白(Fn)能够结合LPS并有助于限制其炎症效应发挥作用,我们提出这种潜在机制可能是滑膜关节中一种新型的保护性防御机制。同时,我们期待这一发现能激发更多相关研究——由于LPS与Fn生成可能存在相互作用,这将有助于进一步阐明这些因素在与肠道通透性改变和内毒素血症相关的风湿性疾病恶化过程中的具体作用。
免责声明:
以上部分内容来源于外网我们重在信息分享,版权归属原作者或原刊发平台所有,如有侵权、信息有误或其他异议,请联系处理,我们将在24小时内删除或整改。
复合免疫 健康活力





























