
应对老龄化挑战,通过口服LPS膳食干预维护血流健康的循证新方案
连续摄入含LPS泛菌糖脂质的补充剂3个月对维持成人血流正常的影响
在日本出生率持续下降、人口深度老龄化的背景下,如何延长健康预期寿命并降低医疗成本已成为重要的公共卫生议题。在此背景下,作为最经济、可持续的自我健康管理手段,通过膳食干预实现自主健康管理的策略日益受到重视。
LPS泛菌糖脂质作为一种具有免疫调节功能的天然物质,自Inagawa等人于1992年首次报道其生理效应以来,既往研究证实LPS作为革兰氏阴性菌细胞壁的核心成分,这种“天然来源”的LPS并非毒素,而是关键的免疫调节因子,可通过激活先天免疫系统中的巨噬细胞发挥调节作用(Inagawa, Kohchi & Soma, 2011),其健康价值逐渐受到科学界关注。
目前,虽然已有研究表明LPS可能通过促进血管内皮生长因子表达、增强毛细血管生成等机制改善血流,但针对健康人群的临床证据尚显不足。本研究采用平行、双盲、随机对照试验设计,旨在探讨评估连续3个月摄入含LPS泛菌糖脂质的补充剂对维持健康成人血液参数正常化的影响,为通过营养干预手段维护血液循环健康提供循证依据。
中文翻译:
连续摄入含LPS泛菌糖脂质的补充剂3个月对维持成人血流正常的影响:一项平行、双盲、随机对照研究。
摘要
本研究通过平行分组随机双盲试验,探究评估了含LPS泛菌糖脂质(每片含LPS 201.5 μg)的膳食补充剂对维持正常血液指标的作用。研究实施前已进行筛选,选取血液参数处于正常值至临界值范围(即健康受试者)且具有参考值的成年男女受试者。服用该补充剂3个月后,结果显示:糖化应激标志物HbA1c的变化率(以基线值为1的比率)在LPS补充组显著降低。与对照组相比,指尖毛细血管数量也显著增加。这些结果表明,通过摄入LPS可有效维持血液指标的正常水平。
引言
在日本,随着出生率下降和人口老龄化加剧,从延长健康预期寿命和降低医疗成本的角度来看,通过饮食摄取实现自我健康管理的重要性日益凸显。
在此背景下,LPS作为一种食品成分,被认为对维持健康具有潜在价值(Inagawa等,1992)。LPS作为革兰氏阴性菌细胞壁的构成物质成分,通过调控先天免疫细胞——巨噬细胞发挥作用(Inagawa、Kohchi和Soma,2011)。LPS通过附着于可食用植物或悬浮在空气中的形式存在于环境中,最新研究表明,人体免疫系统可通过饮食摄入环境中的LPS,也可通过自然呼吸接触LPS(Braun-Fahrlander等,2002)来实现调控。鉴于在中药材和食用植物中发现了LPS存在,Inagawa团队(1992)重点研究了天然摄入LPS的生理作用,并采用来自革兰氏阴性菌成团泛菌的LPS泛菌糖脂质进行口服和透皮摄入的安全性及效果研究。
在针对成团泛菌源LPS泛菌糖脂质生理作用的研究中,四项临床试验结果如下:
(1) 开放性研究(Nakata等,2009):98名30-60岁成年受试者(男性和女性)连续3周每日摄入含LPS 48.6μg 复合酢橘汁后,肩颈僵硬、倦怠、乏力、视疲劳及便秘症状得到显著改善。
(2) 双盲试验(Nakata等,2011):47名40-70岁血糖血脂异常患者连续2个月每日摄入含LPS 500μg Salacia茶后,糖化血红蛋白(HbA1c)与低密度脂蛋白(LDL)指标显著下降。
(3) 双盲试验(Nakata等,2014):52名40-79岁女性受试者连续 3 个月每日饮用含LPS 600μg 的豆奶后,骨密度降低趋势得到有效抑制。
(4) 开放性研究:20名20-65岁成人受试者(男性和女性)连续1个月每日摄入含LPS 1200μg 饮品后,甘油三酯指标下降,且肩颈僵硬、倦怠、乏力、视疲劳与便秘症状呈现改善趋势。
由于这些研究结果已证实口服LPS的安全性,以及从改善(1)和(4)中观察到的肩颈僵硬和视疲劳等症状体现出对维护健康的有用价值,因此表明LPS很可能通过促进血液循环系统的改善发挥关键作用。
LPS可调控巨噬细胞活性。众所周知,巨噬细胞能产生具有血管扩张作用的一氧化氮(NO)。虽尚未有研究明确报道巨噬细胞源性NO对血管扩张的具体贡献,但这种可能性是存在的。
此外,巨噬细胞通过吞噬作用清除体内异常代谢物质。基于此机制,LPS可能通过增强巨噬细胞的吞噬功能,帮助清除血管内蓄积的变性异物,例如晚期糖基化终末产物(AGEs)、糖化血红蛋白(HbA1c)、氧化低密度脂蛋白(LDL)或甘油三酯等物质,从而有助于改善血流。
此外,血液循环功能与毛细血管数量密切相关。研究表明,巨噬细胞在 LPS 刺激下会产生血管内皮生长因子(VEGF)(Cattin 等,2015;Spiller 等,2014)。因此,摄入LPS可能通过增强巨噬细胞的VEGF分泌,促进毛细血管新生,从而改善血液循环功能。
本研究为验证LPS在维持正常血流中的功能,采用含LPS的补充剂和对照组,检测了糖化应激标志物HbA1c、氧化应激标志物氧化LDL以及指尖毛细血管数量,并同时评估了安全性指标。
结果
1.受试者
本研究共纳入55名受试者完成筛选。研究启动后,共有三名受试者因以下原因退出:(1)研究开始后发现存在应排除的病情;(2)受试者因检查时间安排不便而主动退出;(3)助理研究者经访谈评估判断不宜继续参与研究。最终共有52名受试者(LPS补充组26人,对照组26人)参与数据分析。
两组受试者性别比例均为男性9人,女性17人。LPS补充组的平均年龄为37.8 ± 7.2岁,对照组的平均年龄为34.6 ± 9.9岁(表3)。
表3.研究人群的基线特征
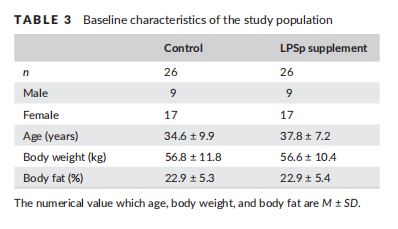
开始摄入时,LPS补充组的体重为 56.6 ± 10.4 kg、体脂率为 22.9 ± 5.4%,对照组分别为 56.8 ± 11.8 kg 和 22.9 ± 5.3%。两组内及组间的体重与体脂率均未观察到显著变化(表4)。
表4.体重和体脂测量
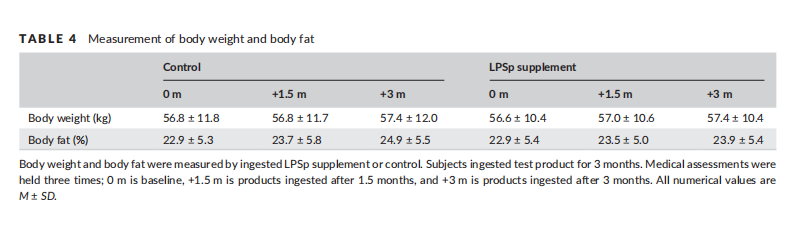
2. 血液检测
本研究结果显示:依据日本Ningen Dock标准(2014年4月1日修订版),在LDL、甘油三酯(TG)、白细胞计数(WBC)、丙氨酸氨基转移酶(ALT)、肌酐及C反应蛋白(CRP)等血液学参数中,各指标处于临界值或更高异常值的受试者人数为1-2例(表5)。
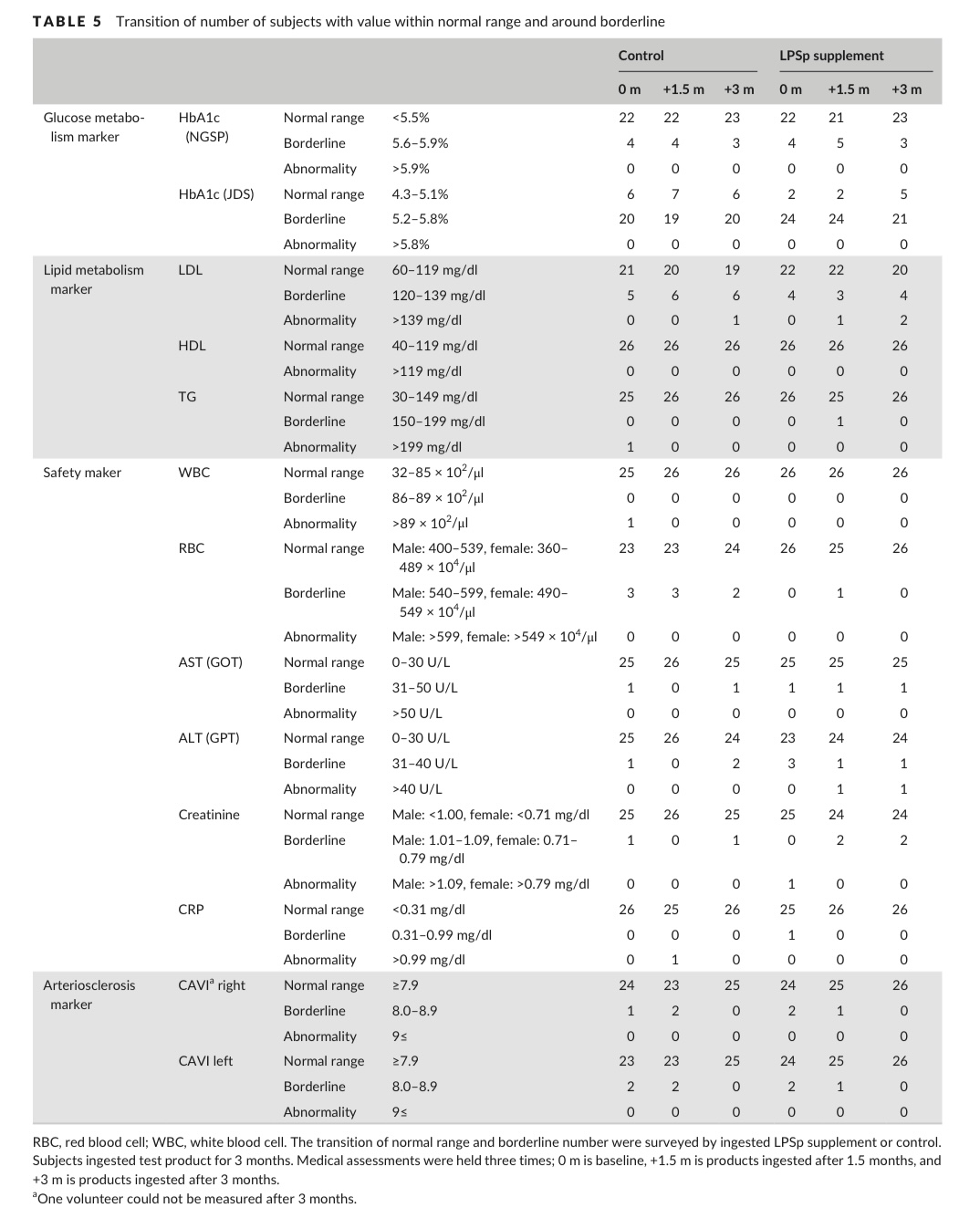
表5.数值处于正常范围和临界值附近的受试者数量变化
根据 JDS 标准,基线时HbA1c(糖化应激标志物)处于临界值范围内的受试者,LPS补充组有 24 人,对照组有 20 人。包括临界值受试者在内,LPS补充组在摄入3个月后HbA1c水平显著降低(表 5–7,图2)。
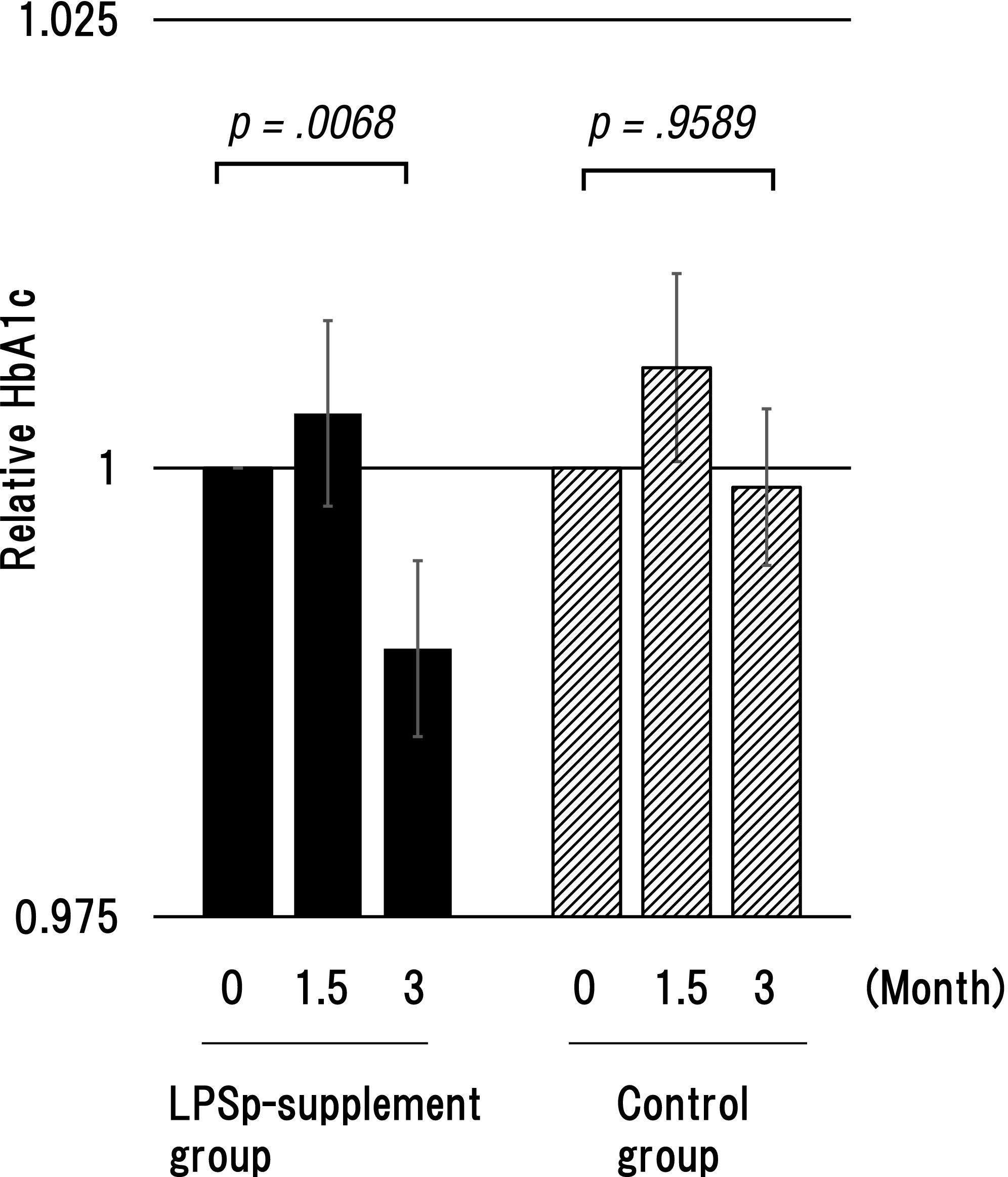
图2. LPS补充组与对照组HbA1c水平变化对比。检测时间点包括开始摄入前(0)、摄入后1.5个月及3个月。
在LPS补充剂组与对照组中,低密度脂蛋白(LDL)、高密度脂蛋白(HDL)、甘油三酯、白细胞计数(WBC)、红细胞计数(RBC)、天冬氨酸氨基转移酶(AST)、丙氨酸氨基转移酶(ALT)、肌酐及C反应蛋白(CRP)等参数,在组内及组间均未呈现显著变化,且这些参数的所有波动均维持在正常范围内(表5-7)。
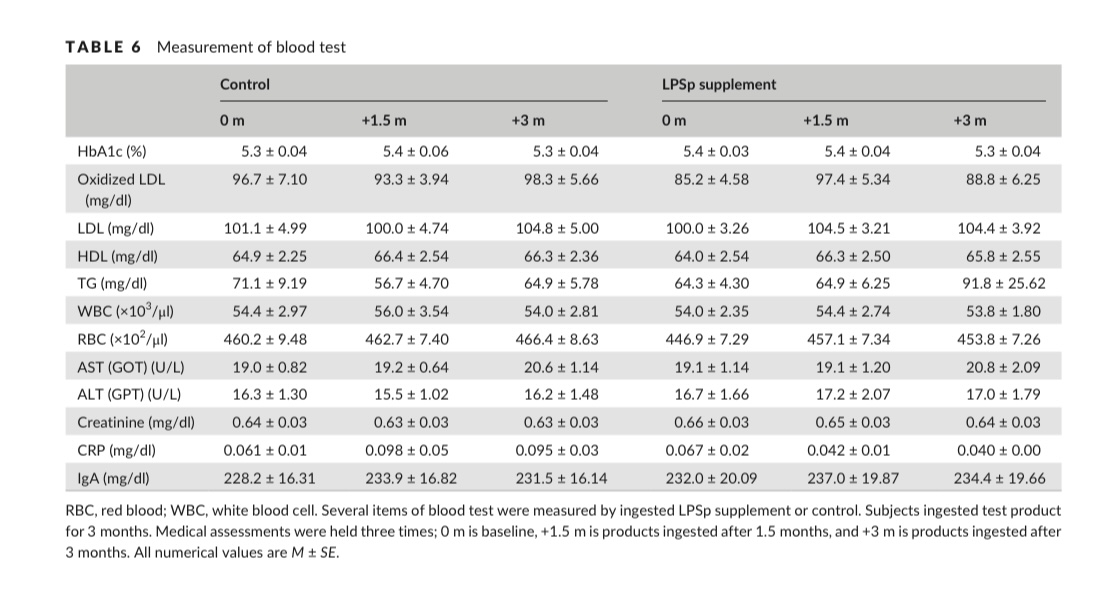
表6.血液检测的测量
在氧化型低密度脂蛋白(oxidized LDL)与免疫球蛋白A(IgA)的检测中,未设定正常/临界值范围,其测量结果在组内及组间均未观察到显著变化(表6,表7)。
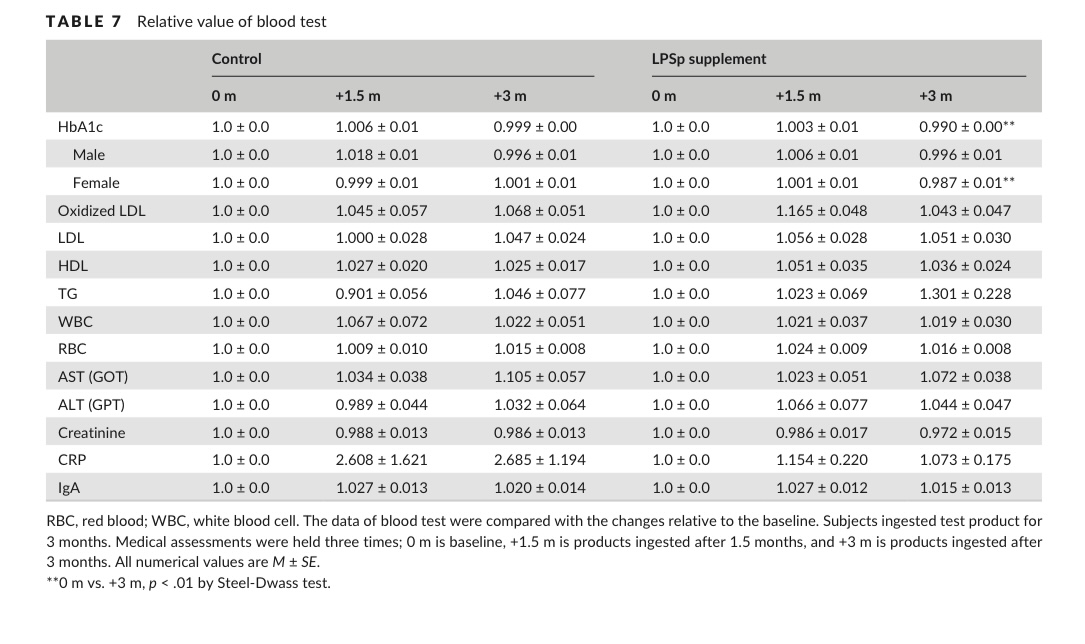
表7.血液检查相对值
在本研究的3个月摄入期间,作为安全性标志物测定的白细胞计数(WBC)、红细胞计数(RBC)、天冬氨酸氨基转移酶(AST/GOT)、丙氨酸氨基转移酶(ALT/GPT)、肌酐、C反应蛋白(CRP)及免疫球蛋白A(IgA)等参数的实测值均未发生显著变化,因此证实LPS补充剂不存在安全性问题。
3. 血流
表8.CAVI的测量
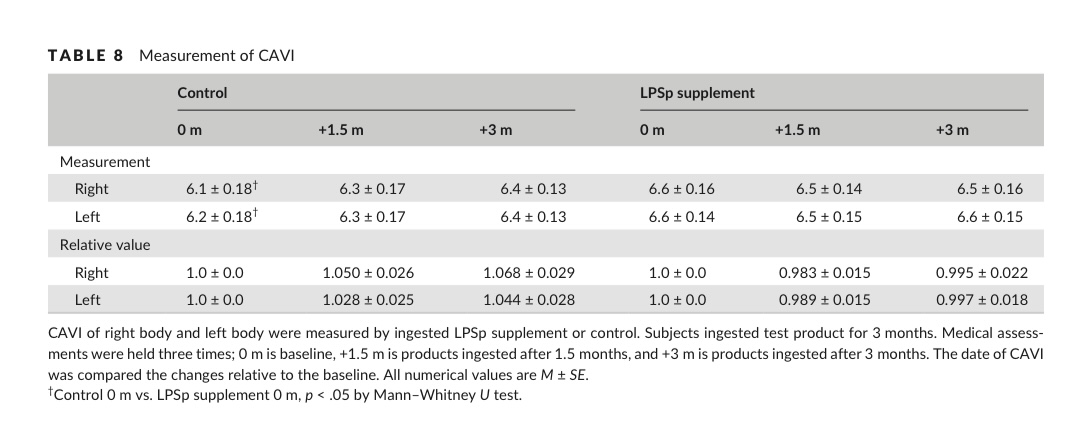
在LPS补充组和对照组中,组内和组间CAVI(心踝血管指数)均未发现显著变化,且该参数始终保持在正常范围内,虽然基线时对照组的CAVI显著较低,但3个月后无显著差异(表8)。
表9.指尖毛细血管数量
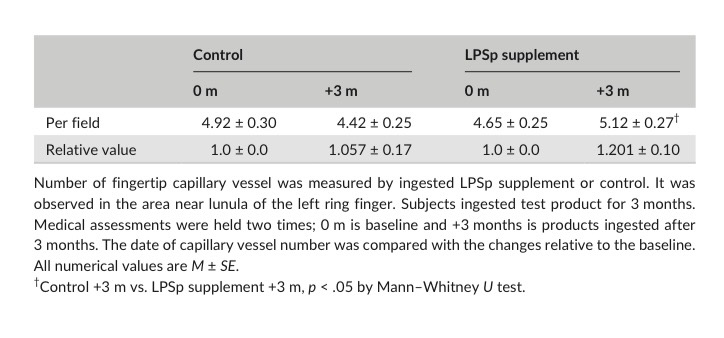
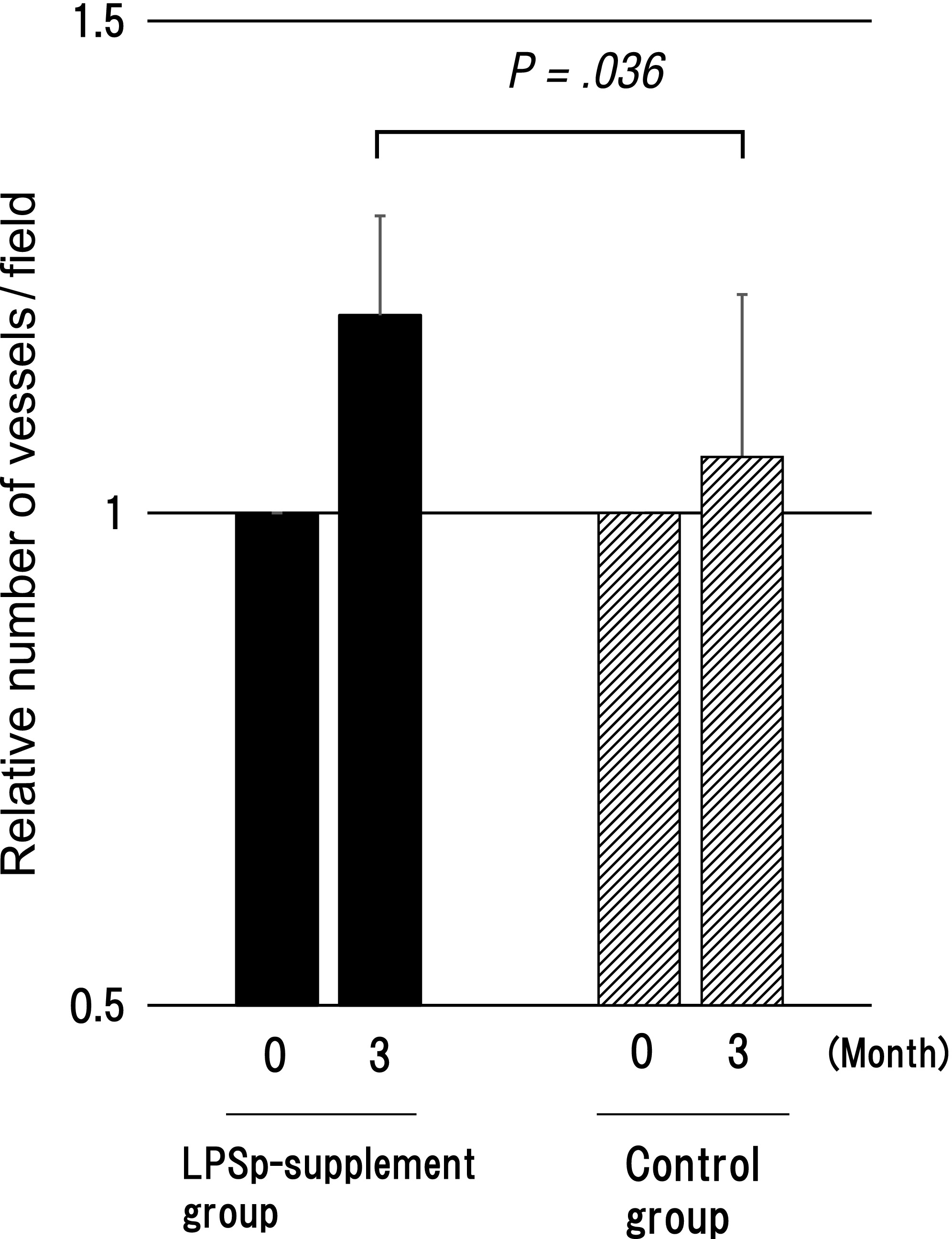
通过使用毛细血管血流评估系统,在指定视野内可确认的指尖毛细血管数量作为指标时,发现LPS补充剂组在3个月后指尖毛细血管数量与对照组相比显著增加(表9,图3)。
图3.LPS补充组与对照组各实验中血管数量的相对变化。
4. QOL(健康相关生活质量)
在整个研究期间,各组间受试者的生活质量(QOL)各维度参数在组内及组间均未发现显著差异。然而,在LPS补充组中,服用初期出现肩颈僵硬的受试者,其症状在3个月后呈现改善趋势(表10)。此外,服用初期“不畏寒”的受试者仅有5人,而3个月后该群体数量翻倍至10人。
讨论
本研究为验证口服LPS补充剂对维持正常血流的作用,采用双盲法进行LPS补充剂的摄入实验。由于本研究旨在评估食品的功能特性,因此受试者人群同时包含健康个体及代谢指标临界值者(如HbA1c/血脂临界人群)。
众所周知,LPS是一种内毒素,当革兰氏阴性菌感染时释放到血液中会引起严重炎症反应,另一方面,LPS又是一种普遍存在于环境中的物质。研究表明,经口服或经皮摄入的LPS并无毒性,反而有助于激活先天免疫。
本研究使用的LPS(泛菌糖脂质)源自小麦共生菌成团泛菌(Pantoea agglomerans)。该LPS的O-抗原部分由鼠李糖和葡萄糖构成,其糖链长度较大肠杆菌更短(Inagawa等,1992)。通过染色体畸变试验(1.5mg LPS/板)、细菌回复突变试验(1.5mg LPS/mL)、单次给药毒性试验(600mg LPS/kg/天)以及28天重复给药毒性试验(300mg LPS/kg/天),均已证实该LPS的安全性(Taniguchi等,2009)。本研究结果还证实,在健康受试者与临界状态受试者中,每日口服500 μg LPS均未发现任何不良事件。
Wiesner等人(2010年)在血液研究中指出,巨噬细胞及腹腔注射的LPS(一种巨噬细胞激活剂)可能加剧动脉粥样硬化。但本研究发现,作为动脉粥样硬化指标的CAVI在两组中均未发生变化。由于本研究对象为健康志愿者,我们虽不能否定Wiesner的研究结论,但至少通过口服给药方式而言,LPS可能并非动脉粥样硬化的致病因素。此外,其他身体指标和血液学指标也未呈现显著差异。
本研究重点探讨了口服LPS对血液功能的改善作用。糖化血红蛋白(HbA1c)是血红蛋白与葡萄糖结合形成的晚期糖基化终末产物(AGEs)。本次研究中,两组中分别有18.2%的受试者处于HbA1c临界值范围。补充LPS经过3个月后,LPS组的HbA1c变化率显著下降(p=0.007),且女性群体的改善效果更为显著,这可能是因为女性群体中处于HbA1c临界值的人数多于男性。该结果与Nakata等人(2011)的研究结果一致。由于巨噬细胞会识别并清除AGEs等变性蛋白(Ott等人,2014),HbA1c的降低可能与口服LPS激活巨噬细胞的吞噬消除作用有关。另一方面,作为氧化标志物的氧化低密度脂蛋白(LDL)在两组中均未发生变化。本研究表明,两组受试者的LDL水平均处于正常范围。
本研究对指尖毛细血管数量与血液循环的关联性进行了探讨。高血压患者常表现为毛细血管密度降低,这一指标常被用于评估降压药物等治疗效果(Penna等,2008)。糖尿病患者同样表现出毛细血管密度下降的特征(Spiller等,2014)。由于毛细血管密度的增加与疾病改善密切相关(例如:胰岛素刺激下组织对葡萄糖的摄取效果依赖于毛细血管,或骨骼肌组织的氧扩散能力增强),因此毛细血管密度常被用作评估指标。在排除疾病因素的日常生活中,由于压力或衰老会导致毛细血管数量减少,因此通过检测观察毛细血管的数量和状态,可以有效评估抗压能力及血流改善情况。
本研究发现,LPS补充组的指尖毛细血管数量显著增加。由此我们提出新的假说:LPS可能通过刺激巨噬细胞产生血管内皮生长因子(VEGF)来促进血管生成,从而有助于改善血流。
此外,本研究还将黏膜产生的免疫球蛋白A(IgA)作为次要指标进行检测。这是因为已有研究表明,舌下摄入的LPS不仅能增强流感疫苗的免疫效果,还能促进作为黏膜免疫关键因子的IgA全身性诱导(Fukasaka 等,2015)。本研究中未观察到IgA水平升高,可能是因为实验期间未接触抗原所致。
近期研究表明,口服和经皮摄入LPS对健康维护和疾病预防具有多重作用。已有报道指出,口服LPS可改善特应性皮炎小鼠的脱毛状况(Wakame、Komatsu、Inagawa 与 Nishizawa,2015),同时研究还发现,在人类真皮乳头细胞中,LPS刺激会以剂量依赖性方式显著提升血管内皮生长因子(VEGF)的基因表达水平(Wakame 等,2016)。更有研究证实,62.5%(16例癌症患者中10例)处于缓解或改善状态的癌症患者通过口服LPS得到改善(Morishima 与 Inagawa,2016)。综合这些研究结果表明,LPS能根据不同疾病,有效促进症状缓解和改善。
本研究结果显示,健康受试者口服LPS后,毛细血管数量增加且出现抗糖应激效应。由此表明,口服LPS有助于维持正常血流。然而,仍需进一步研究以确定维持血流所需的LPS最佳剂量。
免责声明
以上部分内容来源于外网我们重在信息分享,版权归属原作者或原刊发平台所有,如有侵权、信息有误或其他异议,请联系处理,我们将在24小时内删除或整改。
复合免疫 健康活力





























