
口服LPS激活巨噬细胞排钠通路,破解盐负荷高血压预防困局!
口服LPS对高血压大鼠盐负荷模型的预防作用
高血压及其并发症已成为全球范围内威胁人类健康的主要公共卫生问题,其中高盐饮食被广泛认为是诱发和加重高血压的关键因素之一。近年来,研究发现植物共生革兰氏阴性菌——成团泛菌(Pantoea agglomerans)来源的LPS泛菌糖脂质可通过激活宿主免疫、调节代谢及改善肠道微生态,对高脂血症、糖尿病、动脉粥样硬化等多种生活方式相关疾病发挥预防作用。然而,LPS在高盐摄入所致高血压中的潜在保护机制尚未阐明。鉴于高血压是生活方式相关疾病的典型代表,本研究利用自发性高血压大鼠(SHR)建立盐负荷模型,系统评估口服LPS对血压动态变化、血液生化指标及肠道菌群结构的影响,旨在为通过膳食干预防治盐敏感性高血压提供新的实验依据与理论支持。
口服LPS对高血压大鼠盐负荷模型的预防作用
摘要
背景/目的:已有研究表明,口服成团泛菌(Pantoea agglomerans)来源的LPS对多种生活方式相关疾病具有预防作用。因此,本研究考察了其对高血压的预防效果——这种疾病是生活方式相关疾病的典型代表。
材料和方法:以自发性高血压大鼠(SHR)和WKY大鼠(正常血压对照组)从6 ~ 16周龄开始饲养。给SHR口服100 μg/kg LPSp和0.1% NaCl(模拟盐负荷),分别在第6、10、13和16周测量血压。此外,在16周龄时,测量血液生化指标并分析了微生物群落组成。
结果:SHR随年龄增长出现高血压症状,且盐负荷加剧了高血压的发展。单纯给予LPS的SHR血压几乎无下降,但在盐负荷条件下,LPS显著抑制了13–16周龄时的血压上升。
结论: 口服LPS对盐负荷引起的高血压具有预防作用。
高血压是全球最普遍的疾病,患者约占全球人口的30%(1)。在日本,估计约有4300万人患有高血压(2)。近年来,除了腰围指标(男性≥85厘米,女性≥290厘米)外,收缩压(最高值)≥130 mmHg和/或舒张压(最低值)z85mmHg也被纳入代谢综合征的诊断标准(3)。因此,高血压被视为代谢综合征的一个重要指标。高血压是多种疾病的危险因素,例如高血压会引发血管内皮功能障碍、缺血性心脏病、中风和肾衰竭等病症;血压越高,患病率和死亡风险就越高(4-7)。
目前,高血压的主要治疗方法包括使用利尿剂、钙拮抗剂、血管紧张素转换酶抑制剂、血管紧张素Ⅱ受体拮抗剂或交感神经抑制剂等进行药物治疗。然而,药物治疗常伴随副作用,因此,除非需要紧急治疗,在开始药物治疗前应优先改善生活方式。特别是对于血压正常和轻度高血压患者而言,非药物依赖性预防措施尤为重要。
高血压是一种由遗传和环境因素共同决定的复杂性状,由于其发病率高且会显著增加心血管疾病风险,已成为重大的公共卫生问题(8)。在与高血压相关的环境因素中,膳食盐摄入量是最常见且最重要的危险因素(9)。此外,高盐摄入引起的高血压的缓解与巨噬细胞产生的血管内皮生长因子C(VEGFc)及其通过淋巴管从体内清除盐分有关;反之,巨噬细胞功能低下则会在高盐摄入后引发高血压(10)。
本研究考察了源自植物共生革兰氏阴性菌--成团泛菌(Pantoea agglomerans)的LPS泛菌糖脂质及其对多种疾病的预防作用(11-14)。LPS其生理作用通过宿主细胞表面的Toll样受体4(TLR4)介导实现(14)。此外,在动物实验中,口服LPS可改善多种生活方式相关疾病,包括改善兔子的高脂血症、肥胖小鼠的糖尿病、阿尔茨海默病小鼠的认知功能,并能抑制小鼠的动脉粥样硬化病变(17-20)。因此,LPS被认为对多种疾病具有预防作用。口服LPS还能改善与葡萄糖和脂质代谢相关的指标参数。口服LPS的功效可能涉及巨噬细胞的活化(21)。由高盐摄入引起的高血压可能通过巨噬细胞的激活得到改善。本研究在高盐饮食的自发性高血压大鼠模型中验证了口服LPS的降压效果。
结果
WKY-DW(健康对照)组、DW组(正常对照)和LPS组血压随时间的变化对比。与WKY-DW组相比,DW组和LPS组的收缩压(SBP)、舒张压(DBP)和平均动脉压(MBP)均显著升高,但DW组和LPS组之间无显著差异(图1)。
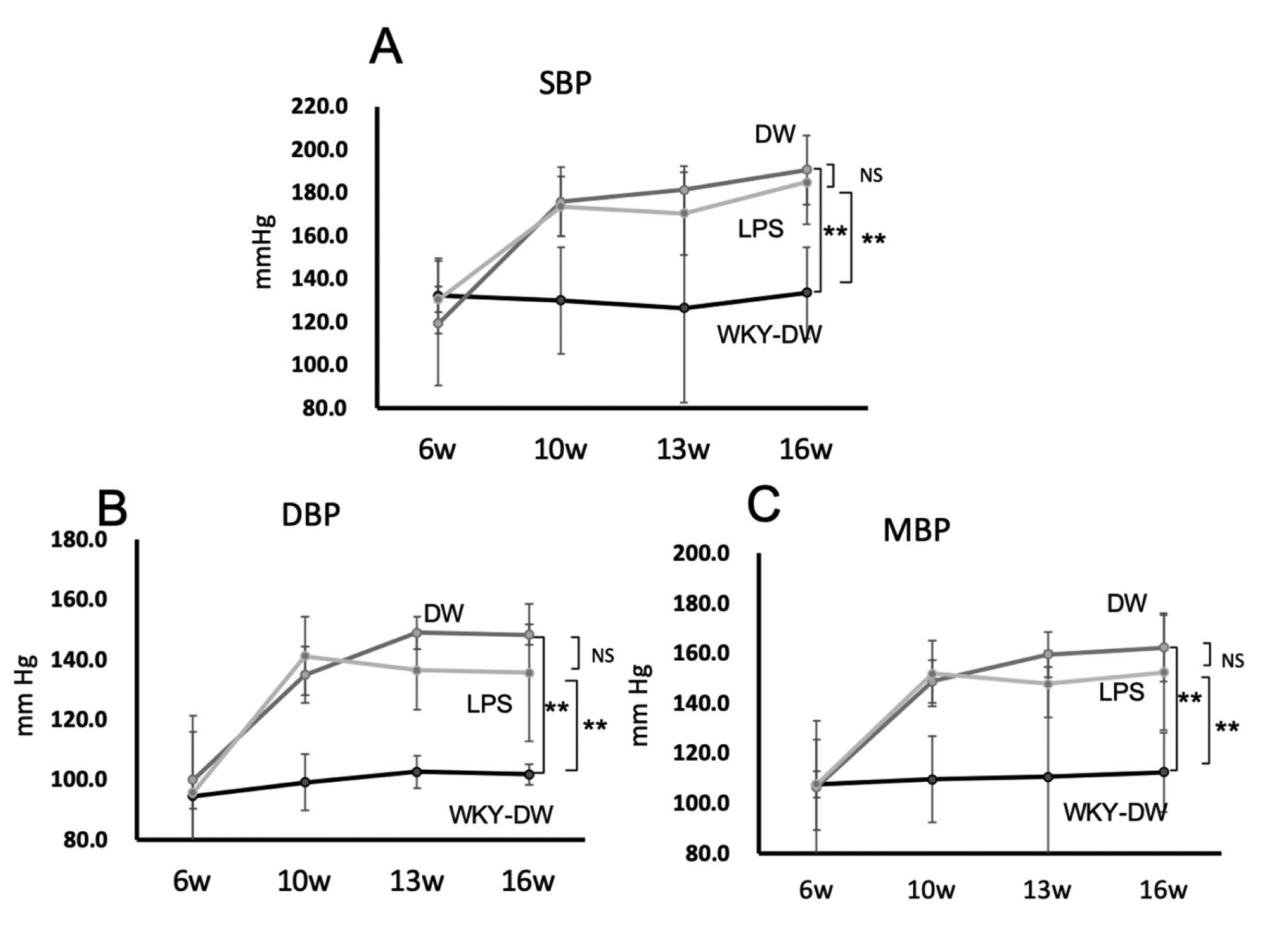
图1.WKY-DW组、DW组和LPS组大鼠血压随时间变化曲线。
WKY-DW(健康对照)组、Na(高盐)组与Na(高盐)+ LPS组血压随时间的变化趋势对比。相较于WKY-DW组,Na组和Na+ LPS组的收缩压(SBP)、舒张压(DBP)及平均动脉压(MBP)均显著升高。在舒张压方面,DW组与Na+ LPS组存在显著差异,但在收缩压和平均动脉压方面,DW组与LPS组无显著差异。此外,与Na组相比,Na+ LPS组的SBP、DBP和MBP有所下降,但未观察到显著差异(SBP:p=0.0587,DBP:p=0.1421,MBP:p=0.1546)(图2)。
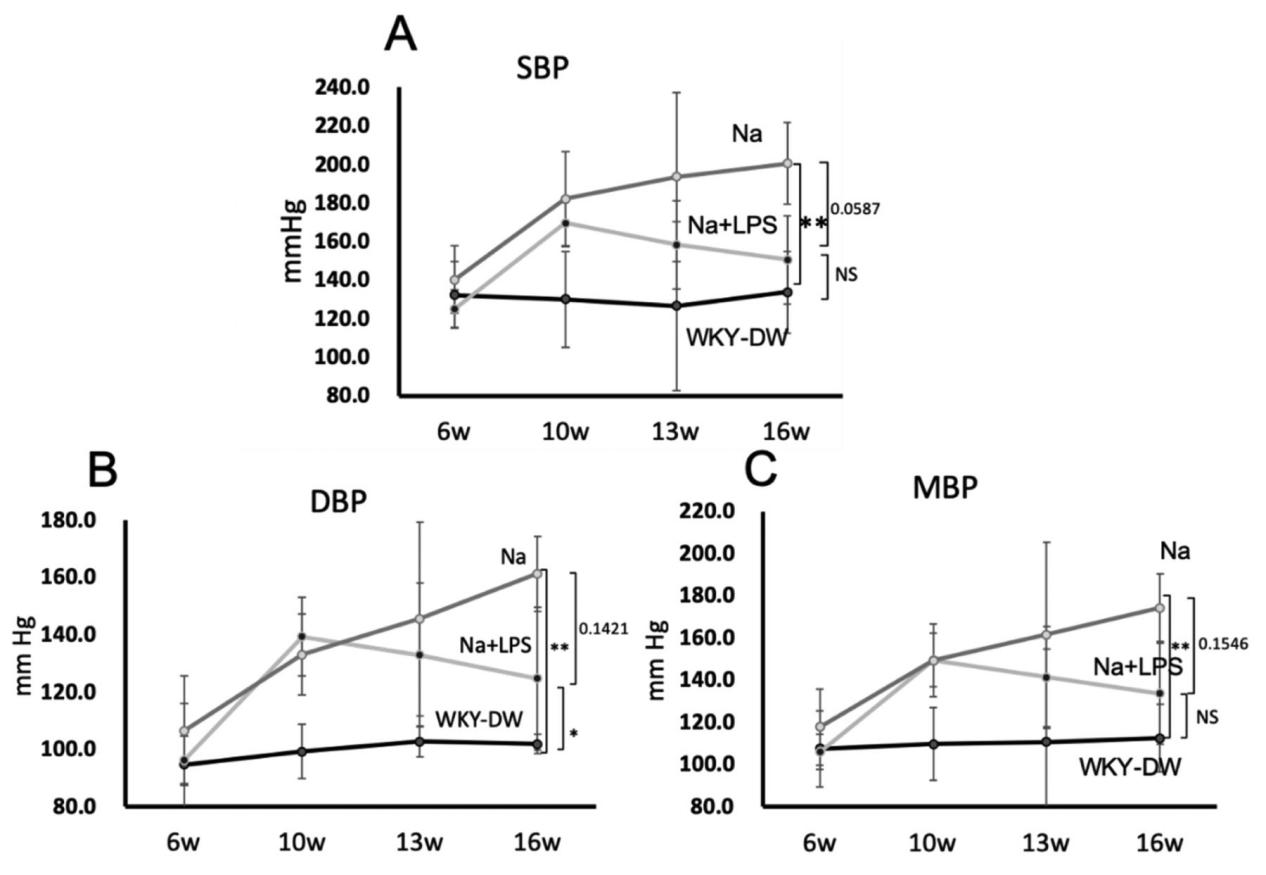
图2.WKY-DW组、Na组和Na+ LPS组大鼠血压随时间变化趋势。
DW(正常对照)组、LPS组、Na(高盐)组及Na+LPS组的生化指标分析。对DW组、LPS组、Na组和Na+LPS组的多项生化指标进行了评估。研究发现,总蛋白(TP)、丙氨酸氨基转移酶(ALT)、血糖(GLU)和淀粉酶(AMY)四项指标未呈现显著差异。在甘油三酯(TG)方面,与DW组相比,LPS组和Na组均显著降低。在天门冬氨酸氨基转移酶(AST)方面,与LPS组相比,Na+LPS组呈下降趋势,而Na组呈上升趋势,但差异均未达到统计学意义。在高密度脂蛋白胆固醇(HDL-C)方面,与Na组相比,Na+LPS组有升高趋势,但差异同样不显著(图3)。
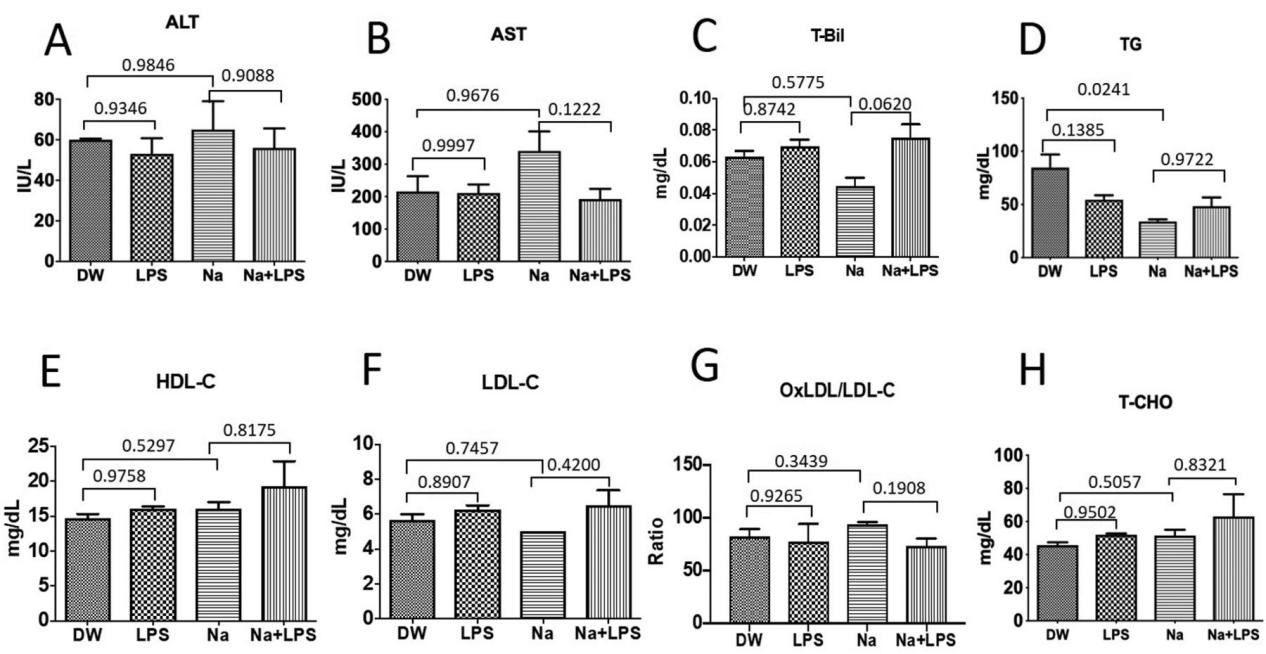
图3.对DW组、LPS组、Na组及Na+LPS组的生化指标进行对比分析。
肠道菌群群落分析。通过提取粪便样本中的微生物DNA,我们对肠道菌群组成进行了分析。如图4A所示,我们在门水平上计算了细菌的相对丰度。DW(正常对照)组与LPS组在此方面没有差异,但Na(高盐)组的丰度较这两组有所增加。与Na组相比,Na+LPS组的厚壁菌门/拟杆菌门相对丰度有所下降,但差异不显著(图4B)。此外,我们采用加权UniFrac分析计算了DW组与LPS组(图4C)、Na组与Na+LPS组(图4D)粪便样本间的距离。通过主坐标分析(PCoA)生成三维(3D)散点图,以可视化输入系统发育树中各实验组的微生物群落是否存在显著差异。该方法能通过距离呈现数据的异质性。DW组与LPS组的粪便微生物群落组成未发现显著差异(图4C),而Na组与Na+LPS组则表现出明显差异(图4D)。在主坐标分析(PCoA)图中,代表Na组和Na+LPS组微生物组成的两个聚类间呈现出明显分离,表明两者具有截然不同的肠道环境。
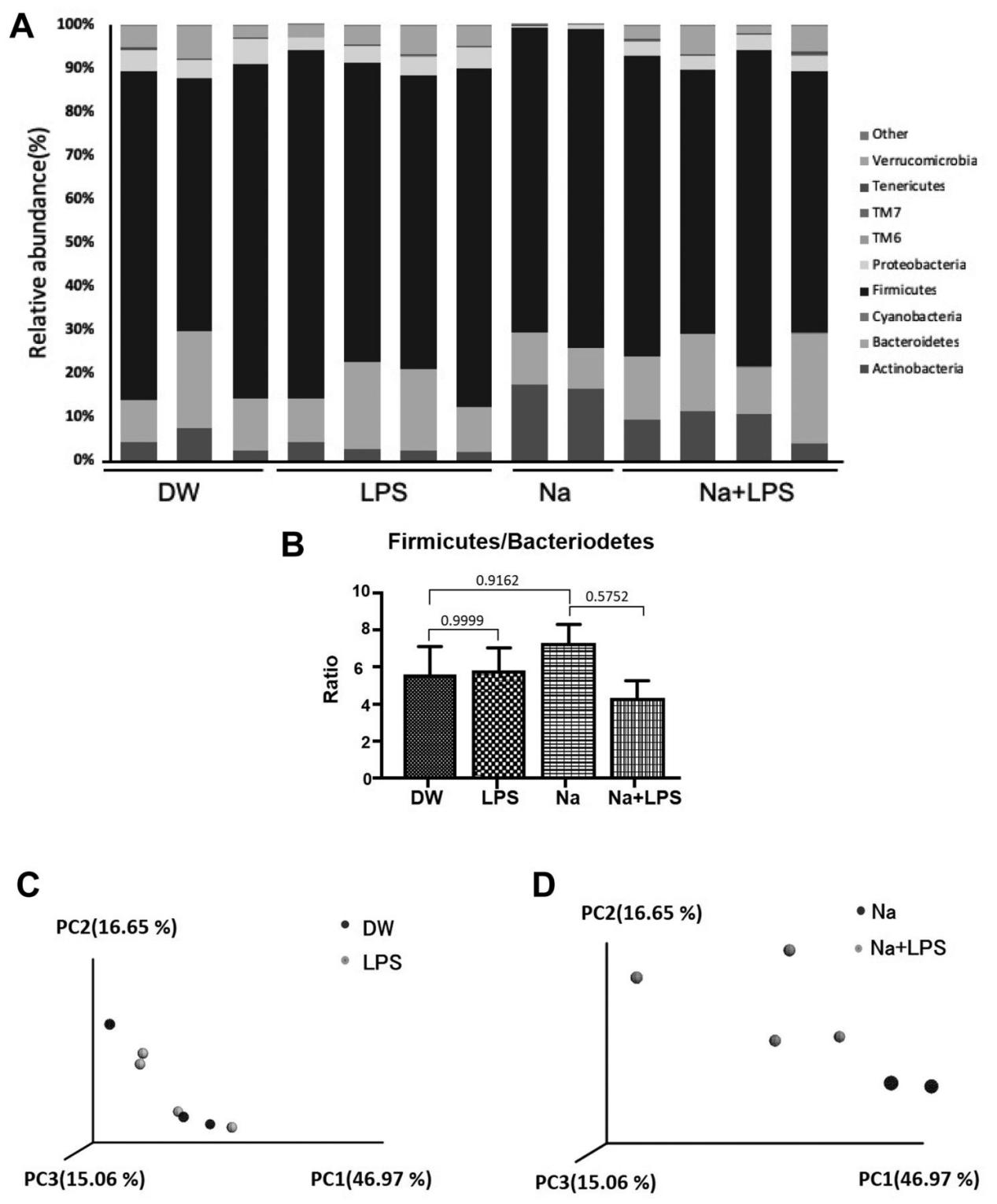
图4.DW组、LPS组、Na组及Na+LPS组的肠道菌群组成。
讨论
流行病学研究表明,高血压是中风、心血管疾病、糖尿病、衰老及血脂异常的危险因素。常用的SHR高血压模型大鼠不仅存在脂质代谢异常,还伴有自发性高血压(4-7)。本研究发现,虽然收缩压(SBP)、平均动脉压(MBP)和舒张压(DBP)随时间推移持续升高,但口服0.1mg/kg LPS后血压略有改善(图1)。值得注意的是,当Na(高盐)组以0.1mg/kg 剂量口服LPS时,相较于未处理的Na组,其血压升高幅度受到显著抑制(图2)。
高盐摄入与高血压和心血管疾病风险增加密切相关(9)。大量基础与临床研究表明,过量摄入盐分会升高血压。盐分摄入不仅作用于血液动力学,还作用于巨噬细胞,而巨噬细胞在调节皮内钠离子浓度方面发挥关键作用(10)。
当盐摄入量超过肾脏的排盐能力时,多余的钠盐主要蓄积在皮下组织。这些皮下积聚的钠离子随后通过巨噬细胞调控的血管内皮生长因子(VEGF)介导,经淋巴管排出体外(10)。因此,若巨噬细胞功能下降,就可能导致血压升高。本研究发现,口服LPS能有效预防高盐饮食引发的高血压。据此推测,LPS通过维持并增强巨噬细胞功能,促进钠盐的排出,从而抑制高血压的发生。
近年来,关于肠道菌群与疾病发生关系的研究不断增多(22)。一项关于肠道菌群与肥胖症的研究表明,在同一环境中饲养的肥胖小鼠与正常小鼠,其肠道菌群组成存在差异:肥胖小鼠中厚壁菌门(Firmicutes)丰度增加,拟杆菌门(Bacteroidetes)丰度降低,导致厚壁菌门/拟杆菌门(F/B)比值升高(22)。此外,在高血压大鼠模型中,F/B比值与肥胖症患者相似且呈上升趋势,并且肠道菌群多样性下降(23)。然而,口服LPS可使F/B比值恢复至与DW组相同的水平。NaCl处理降低了拟杆菌门的含量水平,而通过口服LPS则使其恢复正常(图4B)。在动脉粥样硬化模型中,对ApoE缺陷型小鼠口服LPS后,与对照组相比,其肠道菌群数量显著减少,且拟杆菌门含量水平增加(19)。本研究也获得了类似的结果。
高血压主要是由肥胖和肾损伤引起的。然而,与DW(正常对照)组和Na(高盐)组相比,LPS的给药并未导致生化指标(如脂质代谢和肝脏代谢指标水平)发生显著变化(图3)。尽管LPS改善高盐摄入诱导的高血压的机制尚未明确,但巨噬细胞可能参与促进钠排泄。基于上述数据结果,我们计划进一步解析巨噬细胞在钠排泄中的调控作用。
免责声明:
以上部分内容来源于外网我们重在信息分享,版权归属原作者或原刊发平台所有,如有侵权、信息有误或其他异议,请联系处理,我们将在24小时内删除或整改。
复合免疫 健康活力





























