
四氢姜黄素:天然护肝新选择,轻松破解脂肪肝困局!
四氢姜黄素改善游离脂肪酸诱导的肝脂肪变性并改善HepG2细胞的胰岛素抵抗
在如今快节奏的生活里,你是否也陷入了“肝”着急的健康困境?
高糖高脂的饮食、久坐少动成为常态,这些不良习惯就像一颗颗“定时炸弹”,悄悄给我们的肝脏埋下了隐患。非酒精性脂肪性肝病(NAFLD),作为全球最常见的慢性肝病之一,正悄然威胁着越来越多人的肝脏健康。更令人担忧的是,它与心血管疾病、恶性肿瘤等严重健康问题紧密相连,堪称潜伏在身边的“健康刺客”。当肝脏中游离脂肪酸(FFA)水平持续飙升、甘油三酯异常堆积,肝脂肪变性的“警报”便已拉响。这不仅影响肝脏的正常运转,还会进一步加剧胰岛素抵抗,形成“脂质异常-胰岛素抵抗”的恶性循环,甚至诱发更严重的肝脏病变,让代谢紊乱雪上加霜。然而,目前针对NAFLD的有效治疗手段仍十分有限:既缺乏特效药物,严苛的生活方式干预又难以长期坚持。
不过,希望之光并未熄灭。在天然活性成分的研究领域,姜黄素的健康益处早已被广泛关注,而作为其主要还原代谢产物的四氢姜黄素(THC),凭借其更优的稳定性、亲水性和药理活性,逐渐成为科研人员关注的焦点。近日,一项发表于学术期刊的前沿研究证实:四氢姜黄素(THC)在改善肝脂肪变性和胰岛素抵抗方面展现出惊人潜力。它不仅在抗氧化、抗炎、抗糖尿病等方面表现卓越,还被证实对代谢性疾病具有潜在保护作用,有望成为未来NAFLD治疗的全新突破口。不过,截至目前,四氢姜黄素对肝脂肪变性的具体治疗效果及作用机制,仍有待进一步明确。
基于此,我们开展了相关研究,以油酸诱导的HepG2细胞为脂肪变性模型,探究四氢姜黄素对肝脂肪变性的改善作用及潜在分子机制,期望能为非酒精性脂肪性肝病的临床治疗提供新的思路和潜在候选药物,解锁天然成分守护肝脏健康的新可能。
那么,这一天然化合物究竟如何作用于肝细胞,破解脂质与糖代谢的紊乱困局?它背后的分子机制又隐藏着怎样的科学密码?今天,就让我们一同走进这项前沿研究,揭开天然产物守护肝脏健康的科学面纱。
四氢姜黄素改善游离脂肪酸诱导的肝脂肪变性并改善HepG2细胞的胰岛素抵抗
摘要
肝脏中游离脂肪酸(FFAs)水平升高,无论是由于脂肪分解增加还是游离脂肪酸通量失衡所致,都是肝脂肪变性的关键致病因素。本研究旨在探讨四氢姜黄素(THC)——一种天然存在的姜黄素类化合物及姜黄素的代谢产物——对油酸(OA)诱导的人肝癌细胞脂肪变性的治疗作用,并阐明其潜在机制。研究采用油酸孵育HepG2细胞以建立脂肪变性模型,随后用不同浓度的四氢姜黄素进行处理。结果显示,四氢姜黄素处理显著减少了油酸诱导的HepG2细胞中的脂质积累,其机制可能与抑制脂肪生成相关蛋白的表达有关,包括固醇调节元件结合蛋白1(SREBP-1c)、过氧化物酶体增殖物激活受体γ(PPARγ)、脂肪酸合酶(FAS)和脂肪酸结合蛋白4(FABP4)。此外,THC以酸腺苷激活蛋白激酶(AMPK)依赖的方式减弱了油酸(OA)诱导的肝脏脂肪生成,这一效应可被AMPK抑制剂预处理所逆转。THC促进脂肪分解,并上调参与β-氧化的基因表达。在OA处理的HepG2细胞中,葡萄糖摄取和胰岛素信号传导受损,经四氢姜黄素(THC)处理后这些症状得到改善,包括胰岛素受体底物1(IRS-1)/磷酸肌醇3-激酶(PI3K)/Akt的磷酸化及其下游信号通路——参与糖异生的叉头框蛋白O1(FOXO1)和参与糖原合成的糖原合酶激酶3β(GSK3β)。综上所述,这些结果证明了四氢姜黄素(THC)对抗肝脂肪变性的新型治疗益处,因此有望成为非酒精性脂肪性肝病(NAFLD)的潜在治疗方法。
引言
肝脂肪变性被定义为肝脏甘油三酯(TG)异常累积超过5%,是非酒精性脂肪性肝病(NAFLD)的标志性特征[1]。大量流行病学研究表明,NAFLD与心血管疾病、恶性肿瘤及其他代谢紊乱密切相关。肝脏脂质代谢失调由多种因素引起,例如脂肪组织脂解或膳食摄入导致的血浆游离脂肪酸(FFAs)水平升高、肝脏新生脂肪生成增加、β-氧化减少以及极低密度脂蛋白(VLDL)输出不足,从而导致肝脏TG异常积聚[1,2]。尽管NAFLD的发病机制尚未完全阐明,但肥胖和胰岛素抵抗被认为是关键的致病因素,因为它们会促进脂解作用增强、肝细胞中血浆FFAs水平及摄取增加、脂肪酸代谢改变以及脂肪生成增强,这些因素共同最终导致肝脂肪变性[1,2]。肝脏中FFA流入、促炎细胞因子和脂质中间产物的增加,通过干扰胰岛素受体底物的磷酸化而加剧肝脏胰岛素抵抗[3]。研究表明,肝脏胰岛素抵抗通过加重肝脂肪变性对NAFLD的代谢失调至关重要,其特征表现为胰岛素介导的肝脏葡萄糖生成减少和肝脏糖异生增加[4]。
酸腺苷活化蛋白激酶(AMPK)是一种细胞营养传感器,也是包括肝脏、脂肪组织和骨骼肌在内的大多数组织和器官能量稳态的核心调节因子。AMPK通过对参与脂质代谢的基因进行转录调控,或直接磷酸化代谢蛋白或酶(如固醇调节元件结合蛋白1(SREBP-1)、碳水化合物反应元件结合蛋白(ChREBP)、HMG-CoA还原酶(HMGCR)、乙酰辅酶A羧化酶1(ACC1)和脂肪酸合酶(FAS))来协调肝脏能量代谢[5]。此外,肝脏AMPK通过下调糖异生基因(如编码磷酸烯醇式丙酮酸羧激酶(PEPCK)和葡萄糖-6-磷酸酶(G6Pase)的基因)的表达来维持全身葡萄糖稳态[5,6]。大量研究表明,体外和体内AMPK 激活可预防NAFLD并逆转胰岛素抵抗,因为它能促进脂肪酸氧化,抑制肝脏脂肪生成、胆固醇合成和葡萄糖产生[7,8]。因此,AMPK激活作为对抗NAFLD的治疗策略已引起广泛关注[9]。
四氢姜黄素(THC)由Holder等人于1978年首次发现,是姜黄素的主要还原代谢产物,天然存在于Zingiber mioga、Zingiber officinale和Curcuma zedoaria中[ 10 – 12 ]。研究表明,THC具有广泛的治疗和化学预防特性[13,14]。 尽管THC的药理特性与姜黄素相似,但研究表明,THC作为抗氧化剂、抗炎、抗癌、抗糖尿病和神经保护剂比姜黄素更具活性[14]。更具体地说,THC具有更优的抗氧化活性,并能上调抗氧化酶水平和自由基清除活性,这些特性使其在抗动脉粥样硬化[15]、高血压[16,17]、糖尿病[18]、高脂血症[19]和肾毒性[20,21]方面发挥作用。此外,THC在中性pH的0.1 M磷酸盐缓冲液和血浆中比姜黄素更稳定[22]。其在细胞培养基和血浆中的半衰期显著长于姜黄素[23]。从结构上看,由于化合物额外的氢分子,THC比姜黄素更具亲水性[24]。综上所述,这些特性表明,由于其独特的化学性质和稳定性,THC可能比姜黄素对人类疾病更具效力和疗效。
体内研究表明,四氢姜黄素(THC)对氯喹和砷诱导的肝毒性具有潜在的保护作用[25,26]。研究人员在链脲佐菌素诱导的2型糖尿病大鼠中,THC对代谢功能障碍的疗效得到验证,结果显示其可降低血浆胰岛素和糖异生酶水平,并改善血糖和肝脏碳水化合物代谢[27,28]。除降血糖活性外,THC还被报道具有降血脂活性,可降低血清和肝脏胆固醇、甘油三酯(TG)、游离脂肪酸(FFA)水平以及HMGCR活性[18,19]。这些研究阐明了THC对糖尿病和血脂异常等代谢性疾病的治疗作用,更重要的是,与姜黄素相比,其抗糖尿病和抗高血脂作用更有效。尽管有证据表明THC对代谢性疾病具有潜在保护作用,但其对肝脂肪变性的疗效仍不清楚。在本研究中,我们旨在通过使用细胞脂肪变性模型评估THC对肝脂肪变性的抑制作用,并阐明其潜在机制。
结果
1.THC减少油酸诱导的HepG2细胞内脂质蓄积
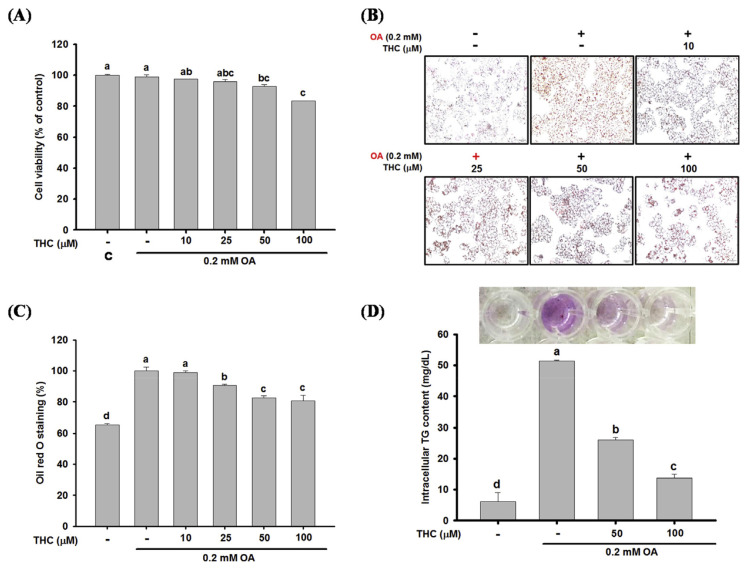
首先用油酸(OA)刺激 HepG2 细胞以诱导脂肪变性,然后用 THC 处理以检测其对脂肪变性的治疗效果。通过台盼蓝测定法测定THC对OA处理的HepG2细胞的细胞毒性作用。将HepG2细胞与OA共孵育12小时,然后用不同浓度的THC(10-100 μM)处理24小时。如图1A所示,10 μM和25 μM浓度的THC对细胞活力无显著影响。然而,100 μM THC使细胞活力降低17%,但在显微镜检查下细胞的形态特征没有明显变化。接下来,通过油红O染色检测THC对OA诱导的细胞脂肪变性的影响。与未处理的对照细胞相比,用OA孵育HepG2细胞诱导了脂肪变性,其标志是细胞内脂滴显著积聚(图1B-1C)。THC处理显著减轻了这些HepG2细胞的脂肪变性,表现为脂滴积聚和细胞内甘油三酯含量的明显减少(图1B-1D)。这证实了THC抑制OA诱导的细胞脂肪变性的效力。
图1. THC对OA诱导的HepG2细胞脂质蓄积的影响。
2 .THC对油酸诱导的脂肪变性中脂肪生成因子表达和AMPK信号通路的影响
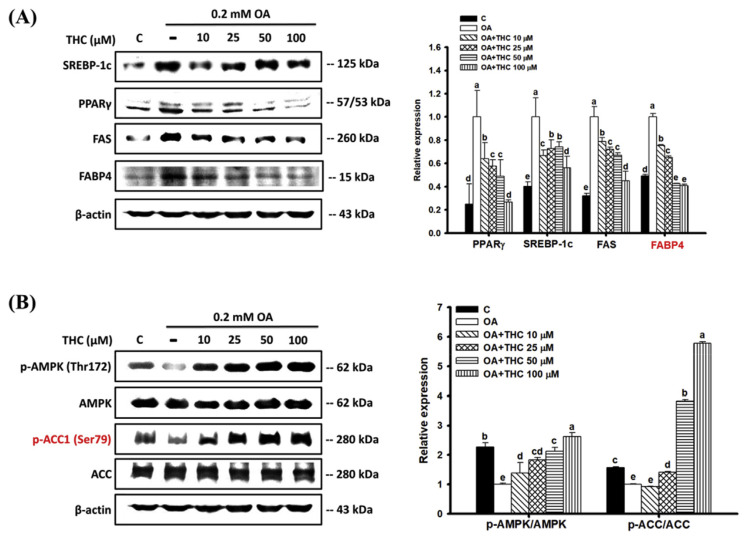
为探究THC是否通过下调脂肪生成因子来减轻OA诱导的细胞脂肪变性,我们采用蛋白质印迹法检测了SREBP -1c、过氧化物酶体增殖物激活受体γ(PPARγ)及其下游靶点FAS和脂肪酸结合蛋白4(FABP4)的表达。图2A显示,与未处理的对照细胞相比,OA处理的细胞中SREBP-1c、PPARγ、FAS和FABP4的蛋白质水平显着升高。然而,这些蛋白水平经THC处理后显著降低。OA诱导的脂肪变性减弱了HepG2细胞中AMPK的磷酸化,导致ACC在Ser79位点的磷酸化降低,从而使其活化增加(图2B)。经THC处理后,AMPK的磷酸化显著增加,从而AMPK介导的ACC失活。这些观察结果表明,THC可能通过下调HepG2细胞中的脂肪生成和上调AMPK信号通路来减轻脂肪变性。
图2.THC对OA处理的HepG2细胞中脂肪生成因子蛋白表达和AMPK 信号传导的影响。
3. THC通过AMPK依赖性途径减轻油酸诱导的脂肪变性
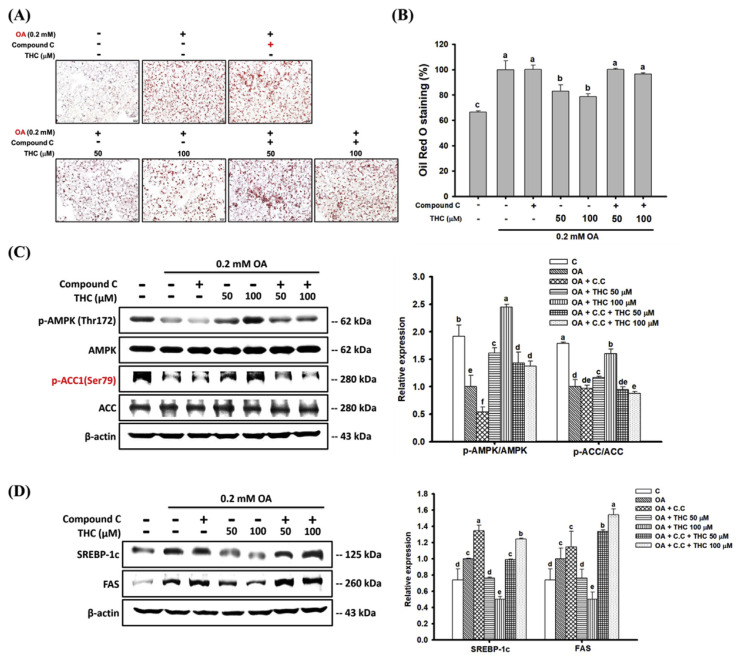
为验证THC对OA诱导脂肪变性的减轻作用是否依赖于AMPK,我们用AMPK抑制剂compound C预处理细胞,并测量了细胞内脂质积聚情况。与之前的观察结果一致,油红O染色显示OA诱导了HepG2细胞中的脂质积聚,而THC显著抑制了脂质积聚。然而,用compound C预处理逆转了THC诱导的脂肪变性减轻(图3A,B)。此外,在compound C存在的情况下,THC诱导的AMPK和ACC磷酸化减弱(图3C)。这些结果支持了THC诱导的AMPK激活对其抑制脂肪变性中脂质积聚的作用这一因果关系的假设。此外,THC显著降低了OA处理细胞中脂肪生成因子SREBP-1c和FAS的蛋白表达,而该效应可被compound C预孵育所逆转(图3D)。因此,THC通过AMPK依赖性机制减轻了HepG2细胞中OA诱导的脂肪变性。
图3.compound C对THC的影响:减弱了OA处理的HepG2细胞中的脂肪生成和AMPK信号传导。
4.THC促进油酸处理的HepG2细胞中的脂肪分解和脂肪酸氧化
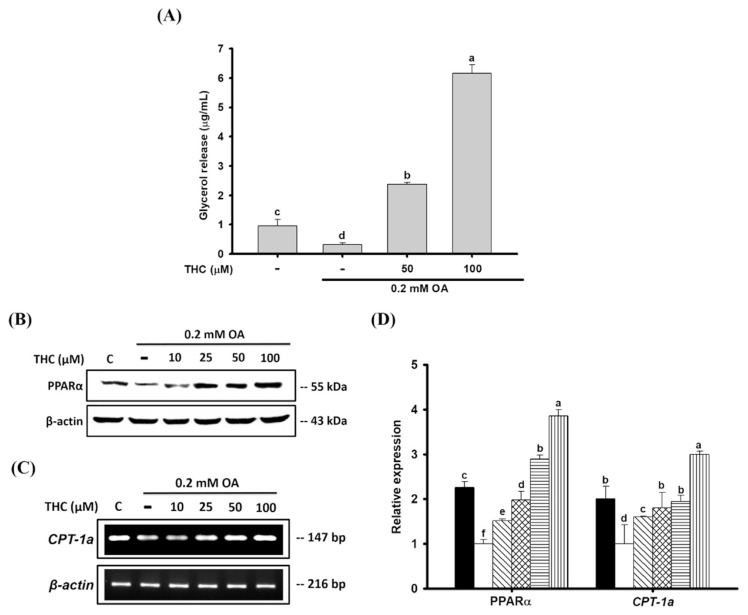
我们通过测定细胞培养基中释放的甘油代谢物浓度,研究了THC对OA诱导脂肪变性的减轻作用是否与脂肪分解相关。与未处理的对照组细胞相比,OA孵育的细胞中脂解作用降低(图4A)。另一方面,THC以剂量依赖性方式刺激甘油释放到培养基中。此外,PPARα(线粒体脂肪酸β-氧化的关键调节因子)的蛋白表达被OA处理降低,但被THC以剂量依赖性方式显著上调(图4B)。关于肉碱棕榈酰转移酶1(CPT1)的表达也观察到了类似结果,CPT1是PPARα的已知靶标,参与长链脂肪酸的线粒体转运[30]。CPT-1a表达在OA处理的细胞中下调,而THC处理显著升高CPT-1a表达(图4C)。这些发现表明,THC刺激HepG2细胞中的脂肪分解和脂肪酸氧化,从而导致OA诱导的脂质堆积减少。
图4.THC对OA 处理的 HepG2 细胞中脂肪分解和脂肪酸氧化的影响。
5.THC增加油酸处理的HepG2细胞中的葡萄糖摄取
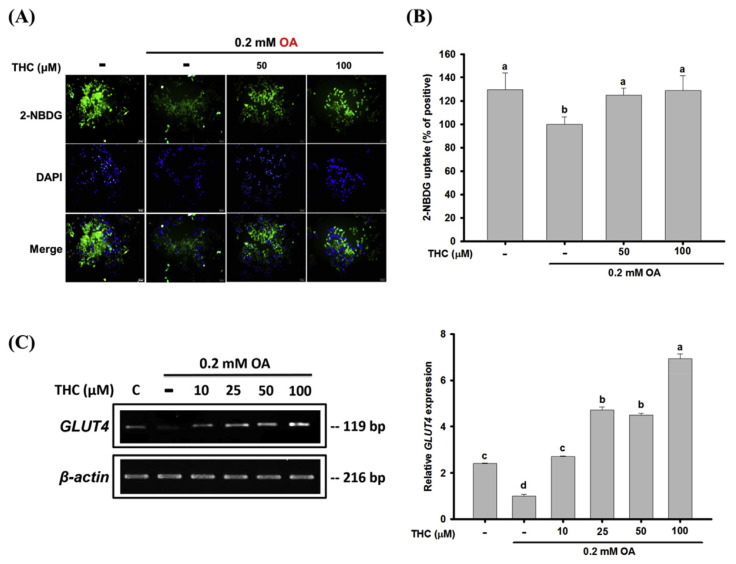
游离脂肪酸(FFA)流入增加已被证明会损害肝脏中的胰岛素信号传导和葡萄糖代谢[3]。为确定THC对脂肪变性中葡萄糖摄取的影响,在OA处理的HepG2细胞中进行了2-NBDG葡萄糖摄取测定。2-NBDG是一种荧光葡萄糖类似物,结果显示,与未处理的对照组细胞相比,OA处理后荧光标记葡萄糖的水平显著降低(图5A)。流式细胞术分析验证了这一结果(图5B)。与仅接受OA处理的细胞相比,用THC处理细胞的2-NBDG摄取量显著更高。此外,GLUT4表达在OA处理细胞中降低,但在THC处理后显著增加(图5C)。这些结果表明,OA诱导的细胞脂肪变性中观察到的葡萄糖消耗失调可被THC逆转。
图5.THC对OA处理的HepG2细胞葡萄糖摄取的影响。
6.THC改善油酸处理的HepG2细胞中的胰岛素信号传导
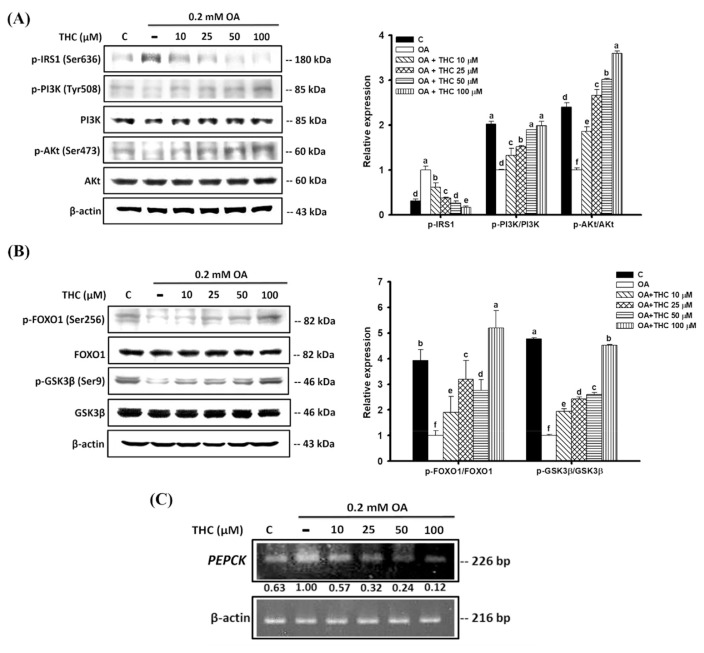
OA已被证明会损害肝细胞中的胰岛素信号传导[31]。为阐明THC对OA处理的HepG2细胞中葡萄糖代谢调节的机制作用,我们检测了胰岛素信号传导。图6A显示,与未处理的对照组细胞相比,用OA孵育HepG2细胞显着增加了胰岛素受体底物1(IRS-1)在Ser636位点的磷酸化,表明胰岛素信号传导受到抑制。这伴随着下游磷酸肌醇3-激酶(PI3K)和Akt信号传导的下调。然而,THC减弱了IRS-1在Ser636位点磷酸化的增加,并随后激活了PI3K/Akt信号通路。PI3K/Akt 信号传导的上调可能是由THC响应引起的葡萄糖摄取增加所致(图5)。Akt 胰岛素介导的叉头框蛋白O1 (FOXO1) Ser256位点磷酸化对于抑制FOXO1依赖性糖异生基因的转录至关重要[ 32 , 33 ]。在此我们发现,OA降低了FOXO1的磷酸化,这与其下游靶点PEPCK的基因表达升高相关(图6B和C)。此外,OA减弱了Akt对糖原合酶激酶3β(GSK3β)在Ser9位点的磷酸化,该磷酸化参与糖原合酶的刺激。然而,THC处理恢复了这些磷酸化水平,表明THC可能逆转脂肪变性中的胰岛素抵抗(图6B)。
图6. THC减轻油酸诱导的HepG2细胞胰岛素抵抗的作用
讨论
在本研究中,我们首次证明THC通过多个靶点减轻了油酸诱导的HepG2细胞脂肪变性。首先,THC显著减轻OA刺激的HepG2细胞中的脂质堆积,表明其对肝脂肪变性具有潜在的治疗益处。其次,THC显著提高了与OA孵育的HepG2细胞中的脂肪分解。最后,THC同时增加OA处理的HepG2细胞中的葡萄糖摄取并激活胰岛素信号传导。
在肥胖人群中,游离脂肪酸水平升高被认为是包括非酒精性脂肪肝病(NAFLD)和糖尿病在内的代谢性疾病的关键致病因素[2,3,34]。本研究中,我们使用不饱和脂肪酸——油酸(oleic acid)来诱导HepG2细胞产生脂肪变性,旨在探究四氢姜黄素(THC)的治疗效益并阐明其作用机制。我们观察到,尽管在最高浓度(100 μM)下THC对OA处理的HepG2细胞具有细胞毒性,但它能有效减少细胞内脂质蓄积。我们的数据表明,这种脂质蓄积的减少可能通过多种机制协同改善肝脏脂肪变性,包括抑制脂肪生成、促进脂肪分解和β-氧化。
THC通过降低SREBP-1及其下游靶点FAS的蛋白表达来减轻脂质积累。SREBP-1是一种在调控脂肪生成基因中的关键转录因子[35],而FAS作为脂肪酸合成中的关键酶[36],其表达下调抑制了脂质生成。PPARγ作为脂肪合成的核心转录因子,除其靶点FABP4外,其表达也因OA而上调。FABP4是脂肪组织中FABP家族的成员,研究表明肝脏PPARγ水平升高与肝细胞中FABP4表达增加相关[37,38]。此外,ACC酶通过Ser79位点直接磷酸化失活可抑制其酶活性,从而阻断脂肪酸生物合成中乙酰辅酶A向丙二酰辅酶A的转化[39,40]。肝脏中存在ACC1和ACC2两种亚型,各自具有不同代谢功能:ACC1定位于细胞质,是肝脏新生脂肪生成的重要调控因子;ACC2则定位于线粒体,参与脂肪酸氧化[41]。THC处理可诱导OA处理的HepG2细胞中ACC1失活,进而可能减少脂肪酸合成。THC抑制脂肪生成的分子机制很可能通过激活细胞代谢核心调节因子AMPK实现。AMPK通过快速磷酸化直接影响酶活性,并调控负责脂质合成的转录因子(如SREBP-1)来调节脂质代谢[5]。Li等研究表明,肝脏AMPK的激活可通过抑制SREBP-1c依赖性脂肪生成来减轻饮食诱导的脂肪变性[42]。本研究中,THC处理激活了AMPK信号通路。此外,我们的结果表明,在AMPK抑制剂Compound C存在的情况下,THC无法抑制OA处理的HepG2细胞中的脂质蓄积,且AMPK的抑制进一步导致ACC1、SREBP-1c和FAS的激活增加。这些结果凸显了AMPK在THC治疗脂肪变性中的重要性。事实上,既往研究曾报道,姜黄素(THC的母体化合物)可通过上调AMPK来抑制脂肪变性[43,44]。尽管仍需进一步研究,但本研究首次明确证实了THC能够激活AMPK信号通路。
THC减轻OA处理的HepG2细胞脂肪变性的另一潜在机制在于促进脂肪分解和β-氧化。我们的研究结果显示,THC处理增加了HepG2细胞培养基中释放的甘油水平,这表明脂解作用被激活。此外,THC处理上调了脂肪酸氧化的关键转录因子PPARα及其下游靶点CPT1的蛋白表达水平[45]。尽管本研究未直接检测β-氧化,但根据现有数据我们推测THC可能刺激了脂肪酸氧化,不过这一结论仍需进一步研究确证。此外,已有研究报道AMPK可通过上调PPARα和CPT1来正向调控脂肪酸氧化[46]。我们已证实THC可诱导AMPK激活,因此,这可能促进了THC处理引起的PPARα上调。然而,仍需进一步研究以全面阐明该机制。综上所述,这些结果表明THC对脂肪变性中的脂肪分解和脂肪酸氧化具有积极作用,这可能为肥胖性肝脂肪变性的治疗提供新的潜在策略。
肝脏游离脂肪酸(FFA)通量的增加与肝脏胰岛素抵抗相关,而肝脏胰岛素抵抗与非酒精性脂肪性肝病(NAFLD)的发生发展密切相关[47]。胰岛素与胰岛素受体(一种酪氨酸激酶受体)结合并激活该受体,随后激活一系列复杂的下游信号级联反应,这些通路参与葡萄糖代谢的调控,如IRS-1/PI3K/Akt信号通路[48]。游离脂肪酸和细胞内脂质代谢产物通过阻断肝脏胰岛素作用,导致肝脏中葡萄糖代谢异常,引起胰岛素信号传导缺陷,进而无法刺激葡萄糖摄取、激活糖原合成以及抑制糖异生[49]。在本研究中,我们观察到OA诱导的HepG2细胞中葡萄糖摄取能力下降和GLUT4表达减少,这表明葡萄糖代谢存在缺陷[49]。经THC处理后,葡萄糖摄取得到有效恢复,GLUT4表达增加。此外,THC处理逆转了OA诱导的IRS-1抑制和PI3K/Akt信号下调。游离脂肪酸升高诱导的肝脏胰岛素信号缺陷与糖异生增加[50-52]及糖原合成减少[53]相关。据报道,Akt通常通过调节肝脏葡萄糖产生来参与肝脏胰岛素信号传导。Akt直接磷酸化FOXO1,并介导其核排斥与下调,从而降低糖异生基因(如PEPCK)的转录[32]。此外,Akt磷酸化可使GSK3β失活,从而激活糖原合酶并促进糖原蓄积[54]。在我们的研究中,OA导致的Akt信号损伤与HepG2细胞中FOXO1磷酸化水平降低及PEPCK基因表达升高相关。THC处理逆转了OA对Akt信号的抑制作用,还恢复FOXO1磷酸化并抑制PEPCK表达。此外,我们证实THC逆转了OA处理的脂肪变性中GSK3b磷酸化水平的降低,提示THC可能激活了糖原合酶,但本研究未对此进行深入探讨。总体而言,我们的数据表明,THC可恢复OA处理的HepG2细胞中受损的胰岛素信号传导,这揭示了其在改善脂肪变性葡萄糖代谢方面具有治疗益处。
综上所述,我们的研究结果表明,四氢姜黄素(THC)对肝脂肪变性具有潜在治疗作用,我们认为其作用机制可能涉及抑制脂肪生成、促进脂肪分解以及激活胰岛素信号通路。此外,我们证实THC可激活AMPK信号通路,这可能是其抗脂肪生成作用的关键机制。尽管还需要进一步研究来验证THC对抗肝脏脂肪变性的具体作用和机制,但现有数据已充分表明THC是治疗NAFLD的有前景的候选药物。
免责声明:
以上部分内容来源于外网我们重在信息分享,版权归属原作者或原刊发平台所有,如有侵权、信息有误或其他异议,请联系处理,我们将在24小时内删除或整改。
复合免疫 健康活力





























