LPS泛菌糖脂质と炎症,抗炎营养新视角,营养消炎的预防潜力,一起来看看!
消炎与LPS泛菌糖脂质
LPS(脂多糖)泛菌糖脂质与炎症的关系较为复杂,既有促炎潜力,也在一定条件下表现出免疫调节作用,而营养抗炎则是通过膳食成分直接调控炎症反应。
LPS泛菌糖脂质的双重角色:
促炎机制:
LPS是革兰氏阴性菌细胞壁成分,通过激活免疫细胞(如巨噬细胞)表面的TLR4受体,触发NF-κB等炎症通路,导致TNF-α、IL-6等促炎因子释放。这种反应在急性感染中起防御作用,但慢性暴露可能导致炎症性疾病(如肠漏、代谢综合征)。
可能的抗炎/免疫调节作用:
少量LPS或特定结构的糖脂质(如泛菌来源的短链LPS)可能诱导免疫耐受,通过调节性T细胞(Treg)或抗炎因子(IL-10)减轻过度炎症。但这一效应高度依赖剂量和机体状态,研究尚不充分。
营养抗炎的关键作用
当我们人体有炎症的时候,往往选择消炎药,消炎药(抗炎药)是广泛用于缓解疼痛和炎症的药物,但不同类别的消炎药具有不同的副作用,长期或不当使用可能对健康造成负面影响。常用的消炎药就是阿司匹林,布洛芬以及萘普生等,这些药物只是缓解症状,减少疼痛和炎症的。 这类非甾体抗炎药的作用机理就是阻断体内环氧化酶COX2的作用,达到抗炎效果,同样的,我们用营养素或者食物可以阻断这个酶的反应达到抗炎效果,而且这些食物没有副作用。药物是降低免疫达到抗炎效果,营养素可以抑制炎症,平衡免疫系统。慢性炎症是多种疾病的共同病理基础(如糖尿病、心血管病),而膳食成分可直接干预炎症通路。
LPS泛菌糖脂质本身并非抗炎剂,但通过营养策略(如优化肠道微生态、摄入抗炎食物)可间接调控其作用。对于慢性炎症管理,综合饮食干预比依赖单一成分更可靠。若存在自身免疫病或严重炎症,建议在专业指导下制定个性化方案。
- 以下为文献详情内容 -
在C8-B4小胶质细胞中,通过重复低剂量LPS转化具有促炎和抗炎表型独特的双重特征
摘要
虽然泛菌糖脂质(LPS)被认为是炎症的诱导剂,但以前的研究表明,重复低剂量LPS通过免疫调节小胶质细胞(脑内常驻的巨噬细胞)具有神经保护作用。然而,通过重复低剂量LPS刺激转化的小胶质细胞(排斥小胶质细胞)还没有被很好地表证,而通过重复高剂量LPS转化的小胶质细胞被很好地研究为内毒素耐受模型,其中促炎分子的诱导被抑制。在本研究中,为了表证排斥小胶质细胞,用鼠C8-B4小胶质细胞细胞系分析了排斥小胶质细胞的基因表达和吞噬活性。排斥小胶质细胞的特征在于促炎分子的高表达(Nos2, Ccl1IL-12B和CD86)、抗炎分子(IL-10,Arg1, Il13ra2和Mrc1),以及神经保护分子(Ntf5, Ccl7,以及Gipr).此外,排斥小胶质细胞的吞噬活性与单一低剂量LPS转化的小胶质细胞的吞噬活性一样高。这些结果表明排斥小胶质细胞具有炎症调节、神经保护和吞噬清除的潜力。此外,本研究显示排斥小胶质细胞的基因表达与重复高剂量LPS处理转化的小胶质细胞的基因表达不同,表明不同剂量LPS转化小胶质细胞的多样性。
介绍
泛菌糖脂质(LPS)是一种表达于革兰氏阴性菌外膜的糖脂。因为当实验性地静脉内或腹膜内给药时,LPS是强有力的全身性炎症的诱导剂,所以LPS自从被发现以来就被认为是一种内毒素。相比之下,我们已经证明了口服LPS对改善各种发病模型中的病理状况的有益作用1–3。我们的研究结果表明,适当浓度、频率和暴露途径的LPS经粘膜给药不会加重炎症,反而有助于维持体内平衡。
最近,我们报道了通过在小鼠中口服LPS(1mg/kg/天)改善了阿尔茨海默病相关的认知障碍,并且通过口服LPS诱导了促炎细胞因子白细胞介素(IL)-6的抑制和抗炎细胞因子IL-10的促进4。此外,以前的报告表明,小胶质细胞,即大脑中的常驻巨噬细胞(mφ),通过促进吞噬作用来清除淀粉样β5,6。这些结果表明,小胶质细胞通过口服LPS治疗而转化,并获得高吞噬活性和炎症调节的神经保护特性。在这方面,其他小组已经报道了通过腹膜内施用重复的低剂量LPS改善了神经病理学7–10。与腹腔注射单次高剂量LPS的有害作用相反,腹腔注射LPS会加剧Aβ积聚、神经元损伤和认知障碍7,11,12他们表明,LPS对神经病的相反作用(即,单次LPS治疗的恶化作用和重复LPS治疗的愈合作用)与不同的小胶质细胞特性有关。考虑到这些结果,可以合理地假设,通过LPS诱导神经保护作用的要求之一是重复和低剂量给药,并且在这种LPS条件下转化的小胶质细胞在维持脑稳态中起关键作用。因此,表征小胶质细胞转化的刺激低剂量LPS(排斥小胶质细胞)为我们阐明口服LPS维持体内平衡的不清楚机制提供了重要的突破性线索。
然而,我们对排斥小胶质细胞的详细情况知之甚少,因为大多数关于LPS刺激的小胶质细胞特征的研究都是在高剂量LPS诱导的严重炎症模型中进行的。本研究的目的是描述小鼠排斥小胶质细胞的特性。首先,我们通过吞噬活性及其促炎分子、抗炎分子和神经保护分子的表达来表征排斥小胶质细胞。然后,为了验证低剂量LPS处理所特有的排斥小胶质细胞的特征,将排斥小胶质细胞与通过重复高剂量LPS转化的小胶质细胞进行比较。结果表明,排斥小胶质细胞的特征在于高吞噬活性和促炎、抗炎和神经保护分子的高表达,这是低剂量LPS治疗所特有的。
结果
促炎分子Nos2, Ccl1、IL-12B和CD86在排斥小胶质细胞中高度表达
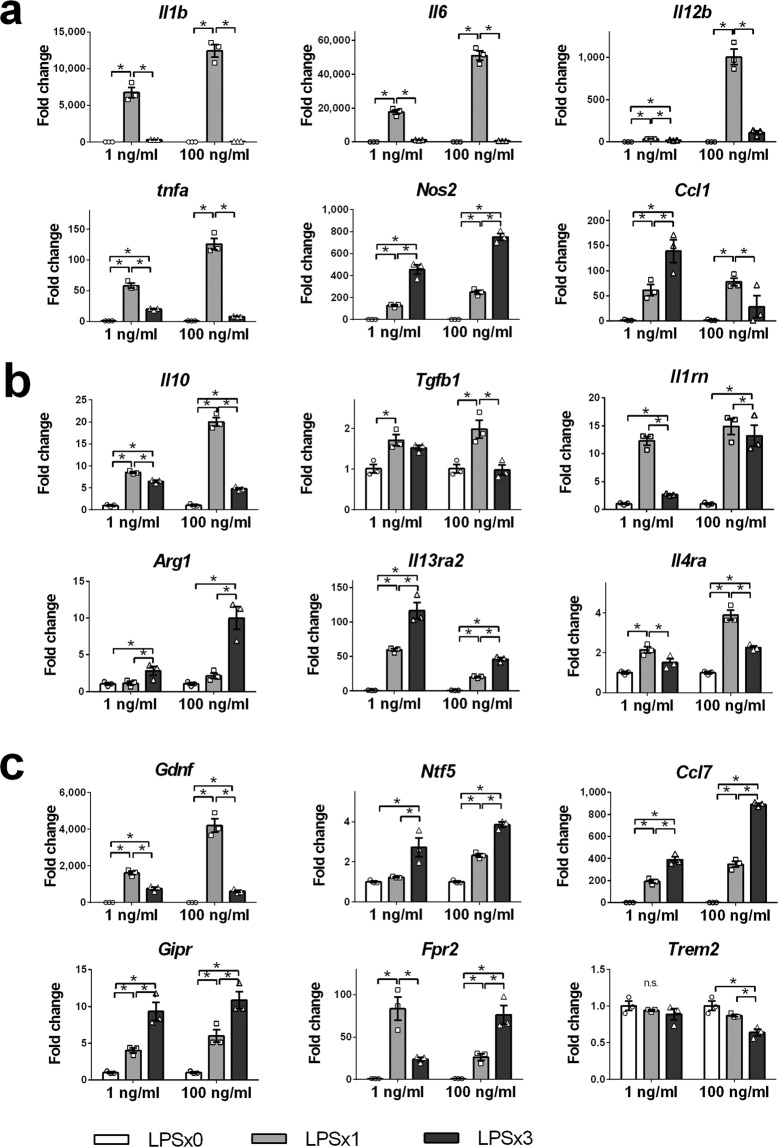
补充表中列出了本研究中用于表征排斥小胶质细胞的基因和分子的缩写1。C8-B4小胶质细胞是最广泛使用的啮齿类小胶质细胞细胞系,并且已经报道了C8-B4细胞系和原代小胶质细胞之间特征的相似性13–15。为了表征排斥小胶质细胞,用低剂量LPS (1 ng/mL)处理C8-B4小胶质细胞一次或三次(n = 3,一式三份)(图。1a),并且将排斥小胶质细胞中促炎分子的表达与通过刺激转化的小胶质细胞中的促炎分子的表达进行比较。定量RT-PCR显示,单个小胶质细胞上调促炎基因的表达,如细胞因子(Il1b, Il6, Il12b, Tnfa,以及Ccl1),精氨酸代谢酶Nos2(图。1b)、细胞表面受体(Fcgr1和Cd36)(图。1c),以及转录调节因子(Stat1和Irf5)(图。1d).排斥小胶质细胞中的大多数促炎基因表达与单一小胶质细胞中的不可比。然而,例外地,精氨酸代谢酶表达Nos2和趋化因子Ccl1在排斥小胶质细胞中比在单一小胶质细胞中明显上调。接下来,测量培养上清液中代表性细胞因子的蛋白质水平(图。1e).与这些组的mRNA表达一致,IL-6和TNF-α的分泌在单一小胶质细胞中被促进,在排斥小胶质细胞中被抑制。然而,IL-12B的分泌在排斥小胶质细胞中以与单一小胶质细胞相同的强度被促进。此外,排斥小胶质细胞表面CD86的蛋白表达高于未治疗的对照组和单一小胶质细胞(图。1f).这些结果表明排斥小胶质细胞的特征是高表达Nos2, Ccl1、IL-12B和CD86。
图一
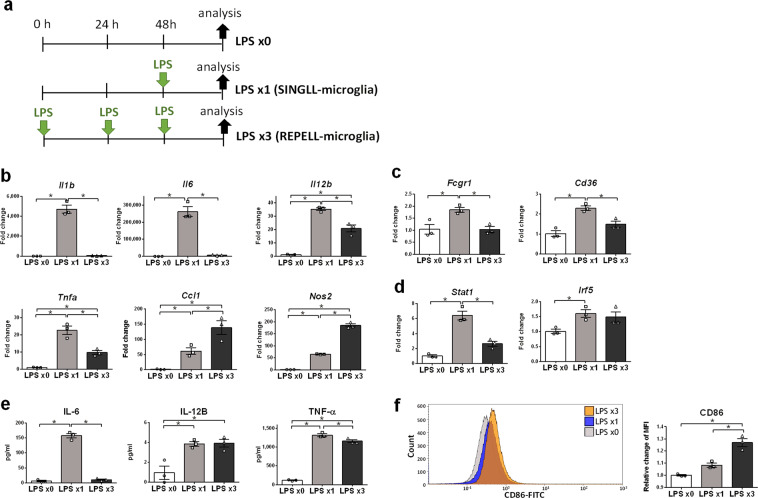
抗炎分子IL-10,Arg1, Il13ra2和Mrc1在排斥小胶质细胞中高度表达
分析排斥小胶质细胞中抗炎分子的表达。定量RT-PCR显示Il10,Arg1,以及Il13ra2在排斥小胶质细胞中高度表达(图。2a–c).抗炎细胞因子的基因表达Il10在排斥小胶质细胞中未被抑制,并保持与在单一小胶质细胞中发现的相同水平的促进作用(图。2a).精氨酸代谢酶的表达Arg1和细胞表面受体Il13ra2在排斥小胶质细胞中的表达明显高于单一小胶质细胞(图。2a,b).相比之下,排斥小胶质细胞不上调其他抗炎分子的表达,例如抗炎细胞因子(Tgfb, 胰岛素f1, Il1rn,以及Chil3)(图。2a)、细胞表面受体(Il4ra和Cd163)(图。2b),以及转录调节因子(Stat3, Stat6, Irf4, Socs3,以及Pparg)(图。2c).此外,排斥小胶质细胞促进IL-10的分泌(图。2d)加入培养基中。Mrc1的蛋白表达(图。2e)高于未处理的对照组,与单一小胶质细胞相当。总之,这些结果表明排斥小胶质细胞高度表达IL-10,Arg1, Il13ra2和Mrc1。
图二
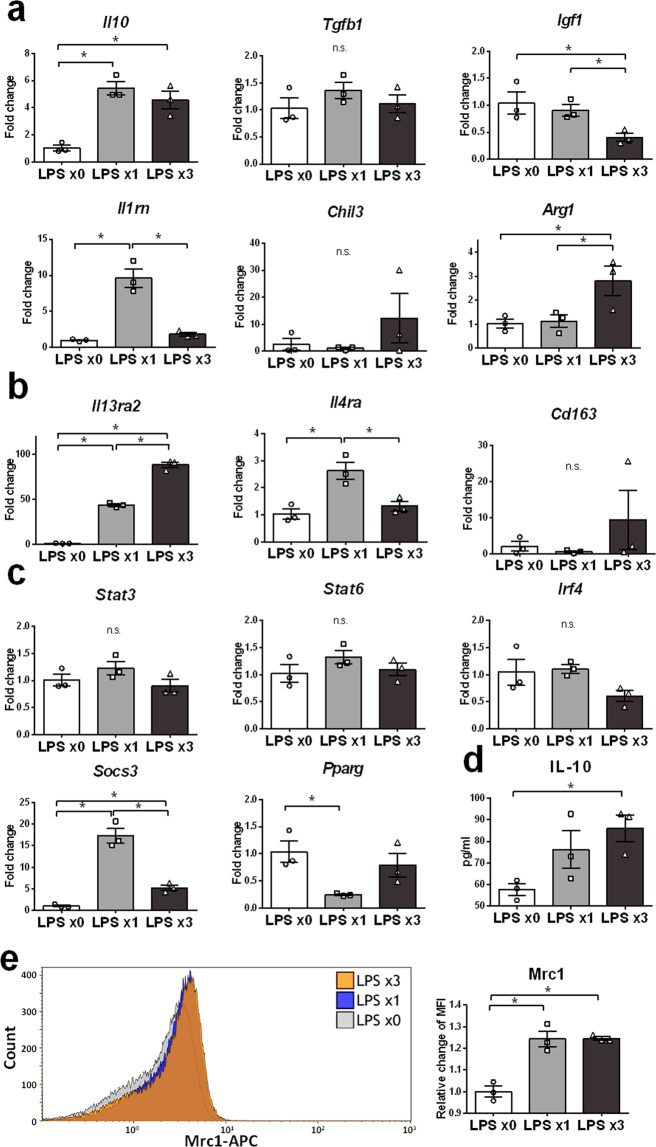
神经保护分子Ntf5, Gipr,以及Ccl7在排斥小胶质细胞中高度表达
为了进一步表征排斥小胶质细胞,我们分析了神经保护基因的表达,例如神经营养分子(Gdnf,Bdnf,以及Ntf5)(图。3a),肠促胰岛素受体(Gipr和Glp1r)(图。3b),以及与神经保护相关的细胞表面受体(Ccl7,Fpr2,以及Trem2)(图。3c).神经营养蛋白5的表达(Ntf5)和C-C基序趋化因子配体7(Ccl7)在排斥小胶质细胞中表达上调。(图3a-c).胃抑制多肽受体的表达(Gipr)在排斥小胶质细胞中上调至与单一小胶质细胞相同的高水平(图。3b).本研究中研究的其他神经保护基因的表达在排斥小胶质细胞中被抑制或没有改变。这是第一个已知的鉴定Ntf5,Gipr,以及Ccl7在排斥小胶质细胞中高度表达。
图3
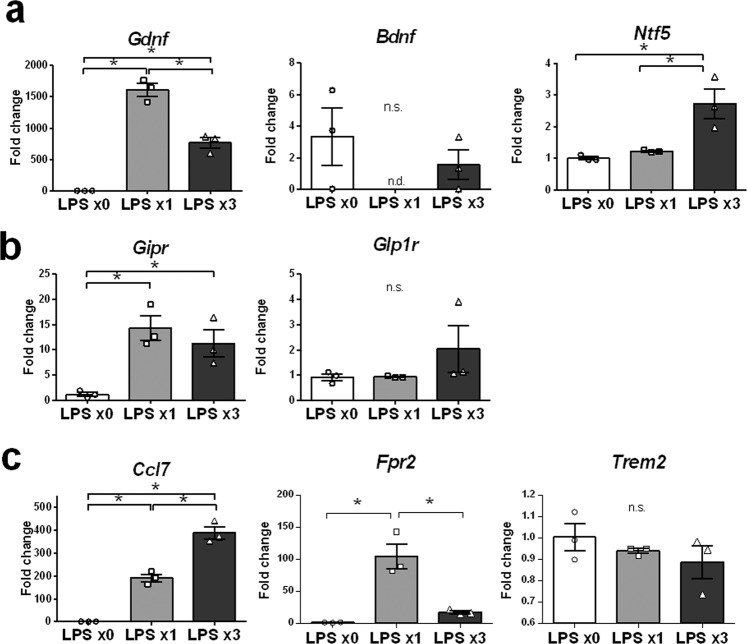
神经保护分子,例如Ntf5, Gipr,以及Ccl7在排斥小胶质细胞中高度表达。
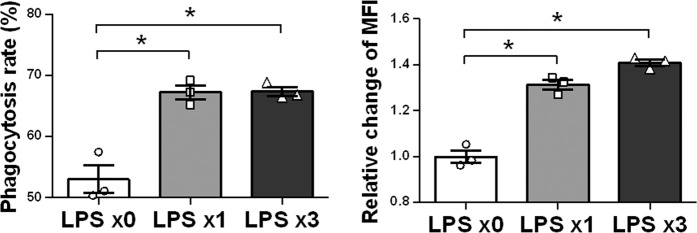
持续促进排斥小胶质细胞的吞噬活性
吞噬作用是小胶质细胞清除外来物质和废物,维持脑内环境稳定的关键功能之一。为了评估吞噬活性,排斥小胶质细胞与荧光乳胶珠一起孵育,并测量细胞中吞噬珠的吞噬率和平均荧光强度(MFI )(图。4).与对照组(53.0%±1.9%)相比,排斥小胶质细胞的吞噬率(67.4%±0.9%)提高到单一小胶质细胞的吞噬率(67.2%±0.6%)。细胞中吞噬珠的MFI也表现出相同的趋势。排斥小胶质细胞的MFI是未治疗对照组的1.4倍,与单一小胶质细胞的MFI相当。因此,这些结果表明排斥小胶质细胞对外来物质具有高吞噬活性。
图4
持续促进排斥小胶质细胞的吞噬活性。
排斥小胶质细胞的基因表达模式在低剂量LPS条件下是独特的
为了测试排斥小胶质细胞的上述特征是否是低剂量LPS治疗所特有的,将排斥小胶质细胞(1 ng/mL LPS)的mRNA表达与重复高剂量LPS (100 ng/mL LPS)转化的小胶质细胞的mRNA表达进行了比较(图。5).基因表达模式Ccl1, Il1rn, Fpr2,以及Trem2两组之间有所不同。的水平Ccl1在排斥小胶质细胞中上调,但在重复高剂量LPS治疗中受到抑制(图。5a).的水平Il1rn与单一小胶质细胞相比,排斥小胶质细胞中的这种活性受到抑制,而重复高剂量LPS组的这种活性与单一高剂量LPS组一样高(图。5b).的水平Fpr2与单一小胶质细胞相比,在排斥小胶质细胞中受到抑制,与反复高剂量脂多糖上调相反。Trem2排斥小胶质细胞的水平没有变化,但重复高剂量LPS下调了水平(图。5c).其他基因的表达在低剂量和高剂量LPS处理之间表现出相同的趋势。因此,由重复LPS诱导的基因表达依赖于LPS浓度而不同,表明排斥小胶质细胞的基因表达模式对其低剂量LPS治疗是独特的。
图5
低剂量和高剂量LPS诱导的不同基因表达的特征是Ccl1, Il1rn, Fpr2,以及Trem2在小胶质细胞中表达。
讨论
先前的研究表明,重复低剂量LPS给药通过诱导具有神经保护表型的小胶质细胞来促进神经保护7–10,16。然而,很少有研究关注排斥小胶质细胞的特征。在目前的研究中,我们通过促炎分子(Nos2, Ccl1、IL-12B和CD86。1)、抗炎分子(IL-10、Arg1, Il13ra2和Mrc1:图。2),以及神经保护分子(Ntf5, Ccl7,以及Gipr:图。3).对于这些代表性分子如IL-6、TNF-α、IL-12B和IL-10,蛋白质表达水平(IL-6、TNF-α、IL-12B:图。1e和IL-10:图。2d)与mRNA表达几乎相关(Il6, Tnfa, Il12b:图。1b,以及Il10:图。2a).众所周知,单一的LPS处理诱导促炎分子,而重复的LPS处理抑制促炎分子的诱导,这种现象称为“LPS耐受”。事实上,据报道,反复高剂量LPS治疗可抑制小胶质细胞中的促炎分子,如IL-1β、IL-6和TNF-α17–22。尽管IL-1β、IL-6和TNF-α在排斥小胶质细胞中受到抑制,与过去高剂量LPS模型报告的数据相似,但排斥小胶质细胞并没有显示促炎分子的整体下调,而是显示出高水平的表达。Nos2, Ccl1、IL-12B和CD86(图1).IL-12B的mRNA表达在排斥小胶质细胞中被轻微抑制,而其蛋白水平与单一小胶质细胞一样高,这可能与转录后水平的蛋白稳定机制有关23–25。抗炎分子的排斥小胶质细胞表达与先前报道的重复高剂量LPS上调IL-10、Arg1和Mrc1部分一致8,26,27。促炎和抗炎分子的共表达是排斥小胶质细胞的独特特征之一。因为据报道,表达IL-12和IL-10的自体灭活肿瘤细胞的组合通过控制局部炎症诱导协同肿瘤缓解28表明表达IL-12和IL-10的排斥小胶质细胞具有调节炎症的潜力。此外,排斥小胶质细胞高度表达神经保护分子Ntf5, Gipr,以及Ccl7(图。3).NTF529还有GIPR30–32通过其在脑炎期间的抗氧化和抗凋亡特性具有神经保护作用,CCL7与神经元分化相关33,表明排斥小胶质细胞通过这些因素具有神经保护潜力。据报道,小胶质细胞“记忆”重复的LPS刺激并转化为神经保护细胞7,这项研究中确定的神经保护分子可能参与了这一机制。同时,微小RNA (miRNA)是抑制mRNA合成蛋白质的机制之一。据报道,miRNA-146a、miRNA-155、miRNA-221、miRNA-125b、miRNA-132、miRNA-579和miRNA-21参与LPS耐受34–36。在这种情况下,miRNA数据库(microRNA.org)证实在排斥小胶质细胞中具有高mRNA表达的分子如Nos2,Ccl1(图。1b), Arg1,Il13ra2(图。2a,b), Ntf5、Ccl7,以及Gipr(图。3a–c)不是上述LPS耐受期间诱导的miRNAs的靶标。因此,可以推测,在我们研究的条件下,至少通过这种miRNA机制,Nos2、Ccl1、Arg1、Il13ra2、Ntf5、Ccl7和Gipr的mRNA翻译转化成蛋白质的过程不太可能受到抑制。
排斥小胶质细胞还表现出高吞噬活性(图。4).据报道,小胶质细胞通过促进Aβ的吞噬作用来改善阿尔茨海默病相关的病理7,表明具有高吞噬活性的排斥小胶质细胞有助于清除引起神经病变的脑异生物质。TREM2是参与促进吞噬作用和抑制小胶质细胞中促炎分子如TNF-α和NOS2的分子之一37,38。然而,在排斥小胶质细胞中Trem2没有改变,然而Nos2表达和吞噬作用得到促进。因此,提示排斥小胶质细胞的吞噬作用是通过不依赖于TREM2的机制来促进的。事实上,吞噬作用是一个非常复杂的过程,涉及各种吞噬受体和肌动蛋白重塑39。因为IL-12B和TNF-α促进NOS2诱导40,41,并且NOS2不仅在细胞内杀伤中而且在吞噬活性中具有关键作用42这表明这些分子与排斥小胶质细胞的高吞噬活性有关。
综上所述,本研究首次证明排斥小胶质细胞具有高吞噬活性和高表达促炎、抗炎和神经保护分子的特征。有趣的是,排斥小胶质细胞的独特特征被认为有助于维持大脑稳态,就好像它们在名义上和实际上都是“击退疾病”。此外,据报道,轻度氧-葡萄糖剥夺诱导小胶质细胞表现出抗炎和保护表型在试管内43,这是一种类似于我们研究中排斥小胶质细胞的现象。因此,这些数据表明,无论是脂多糖还是氧糖剥夺,小胶质细胞保护性表型都可以通过“温和”刺激来诱导。
重要的是,排斥小胶质细胞的特征与在阿尔茨海默病小鼠模型中口服LPS诱导的小胶质细胞的特征一致在活生物体内16在高吞噬活性和高IL-10表达方面。在这种情况下,另一项研究报道了通过腹膜内重复施用低剂量LPS转化的小胶质细胞也表现出增强的Aβ吞噬作用和高IL-10表达的特征,这也与排斥小胶质细胞的特征一致7。因此,上述排斥小胶质细胞的特征可能部分反映了通过口服LPS转化的小胶质细胞的特征在活生物体内。因为据报道腹膜内施用IL-10可以诱导小胶质细胞表达高水平的IL-10,就像腹膜内施用重复的低剂量LPS的情况一样7,IL-10也可能是两种排斥小胶质细胞诱导机制共同的关键介质在试管内和通过口服LPS转化的小胶质细胞在活生物体内.
此外,目前的研究表明排斥小胶质细胞不仅仅是重复高剂量LPS转化的小胶质细胞的缩小版10但是表现出基本上不同的特征(图。5).结果提示,低剂量LPS条件是诱导转化为排斥性小胶质细胞的重要分子。小胶质细胞通过适应各种微环境条件不同转化,在维持体内平衡的先天免疫中发挥重要作用44–46最近有报道称,小胶质细胞的多样性可以通过不同的配体、疾病和时间进程来转化45–49。然而,很少认识到不同剂量LPS转化小胶质细胞的多样性,低剂量LPS转化的小胶质细胞的表型通常被认为是高剂量LPS的简化版本10。因此,本研究为不同剂量LPS诱导小胶质细胞转化的多样性提供了新的视角。最近的一份报告也支持了这一观点,即低剂量LPS (1 fg/mL)预处理可使小胶质细胞在随后PI3Kγ介导的高剂量LPS (100 ng/mL)刺激下产生促炎细胞因子50。此外,其他报告显示,在巨噬细胞中,低剂量LPS (5 pg/mL)的预刺激诱导RelB降解,与高剂量LPS (100 ng/mL)的预刺激期间发生的RelB诱导相反51,表明在低剂量和高剂量LPS刺激的小胶质细胞中不同的细胞内信号转导起作用。
总之,目前的研究表明排斥小胶质细胞的独特特征是高吞噬活性和促炎、抗炎和神经保护分子的高表达(图。6),表明排斥小胶质细胞具有“排斥疾病”和促进维持脑稳态的潜力。此外,本研究揭示了低剂量LPS是诱导排斥性小胶质细胞的关键因素,表明了不同剂量LPS对小胶质细胞转化的多样性。通过引发小胶质细胞的目的转化,适当的低剂量LPS治疗有望成为排斥各种神经障碍的新的治疗或预防靶点。
图6。
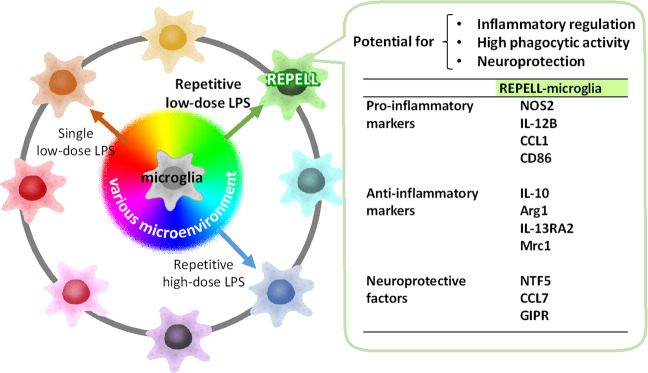
C8-B4小胶质细胞中通过重复低剂量脂多糖转化的具有促炎和抗炎表型的独特杂交特征模型。
免责声明
以上部分内容来源于外网我们重在信息分享,版权归属原作者或原刊发平台所有,如有侵权、信息有误或其他异议,请联系我们,我们将在24小时内删除或整改。
复合免疫 健康活力