
脂肪组织巨噬细胞中胰岛素和LPS介导的信号通过Akt-mTOR激活调节餐后血糖
LPS调节血糖稳态的作用机制
注:
本文为中、日、英三种语言,下方附有中文翻译,供您查阅!
私たちが食事をすると、一過性に血糖値があがります。これを元に戻しているのがインスリンです。すい臓の膵ランゲルハンス島に存在する膵β細胞から分泌されます。
インスリンの役割は、筋肉細胞や脂肪細胞に作用して、それらの細胞が糖を取り込むようにすることです。つまりインスリンは、食事によって摂取され、一旦血液の中に入った糖を、細胞に取り込ませ、エネルギーとして使わせる、ことを促すホルモンです。またインスリンは肝細胞での糖新生を抑制し、逆に糖をグリコーゲンとして保存することを促進することで、血糖値が高くなり過ぎないように調節します。こうして、食後しばらくすると、血糖値は通常レベルに戻るのです。
しかし、すい臓からのインスリンの出が悪くなったり、インスリンの作用を受ける細胞側でインスリン受容体の感受性が落ちたりすると、糖が細胞に移行せず、血糖値がずっと高いままになります。血糖値が高いと、色々なたんぱく質に糖が結びついて変性・劣化します。これが糖尿病で、糖尿病がさらに様々な病気につながっていくことが知られています。従って血糖値の調節が、私たちの健康にとても重要であることがわかります。
さて、近年、血糖値を制御しているのはインスリンだけではないことがわかってきました(*1)。食事によって糖が腸内に送り込まれると、腸内細菌の分布が変わります。具体的には、小腸内で腸内細菌科のグラム陰性細菌が一過性に増加します。その結果、生理的な現象としてグラム陰性細菌由来のLPSが、微量に腸管から出て門脈(消化管等から肝臓につながる静脈)に入ります。こうして体内に入るLPSは炎症を起こすと言われてきましたが、実は門脈の免疫細胞や、脂肪組織マクロファージから炎症を抑制するIL-10を誘導します。そしてこのIL-10はインスリンと協働して、肝細胞での糖新生を抑制します。このように、腸内細菌由来のLPSが血糖値(糖の代謝)を正常に保つ事に深く関わっているのです。
(*1)Insulin- and Lipopolysaccharide-Mediated Signaling in Adipose Tissue Macrophages Regulates Postprandial Glycemia through Akt-mTOR Activation.Molecular Cell 79: 1–11 (2020)
中文翻译:
当我们进食时,血糖值会暂时上升。胰岛素的作用就是将血糖值恢复到正常水平。胰岛素是由胰腺的朗格汉斯岛中的β细胞分泌的。
胰岛素的作用是作用于肌肉细胞和脂肪细胞,促使这些细胞吸收糖分。也就是说,胰岛素是促进因饮食而摄取的糖分被细胞吸收,并作为能量使用。此外,胰岛素还抑制肝细胞中的糖异生,并促进糖转化为糖原储存,从而调节血糖值,防止其过高。这样,在饭后不久,血糖值就会恢复到正常水平。
然而,如果胰腺分泌的胰岛素减少,或者接受胰岛素作用的细胞对胰岛素受体的敏感性下降,糖分就不会转移到细胞中,血糖值将一直保持在较高水平。高血糖会导致各种蛋白质与糖结合发生变性和劣化。这就是糖尿病,而糖尿病又会进一步导致多种疾病。因此,调节血糖值对我们的健康非常重要。
近年来,已经明确血糖值的控制不仅仅依赖于胰岛素(*1)。当食物中的糖分进入肠道时,肠道菌群的分布会发生变化。具体来说,在小肠中,肠道菌群科的革兰氏阴性细菌会暂时增加。结果,作为生理现象,革兰氏阴性细菌来源的LPS会微量从肠道排出进入门静脉(连接消化道等至肝脏的静脉)。尽管LPS进入体内一直被认为会引起炎症,但实际上,门静脉的免疫细胞或脂肪组织巨噬细胞会诱导产生抑制炎症的IL-10。而这种IL-10会与胰岛素协同作用,抑制肝细胞中的糖异生。这样,肠道菌群来源的LPS在维持正常血糖值(糖代谢)方面发挥着重要作用。
(*1)Insulin- and Lipopolysaccharide-Mediated Signaling in Adipose Tissue Macrophages Regulates Postprandial Glycemia through Akt-mTOR Activation.
Molecular Cell 79: 1–11 (2020)
脂肪组织巨噬细胞中胰岛素和LPS介导的信号通过Akt-mTOR激活调节餐后血糖
摘要
免疫细胞在调节餐后葡萄糖代谢中的生理作用尚未完全阐明。我们发现,脂肪组织巨噬细胞在进食时产生白细胞介素-10 (IL-10 ),它与胰岛素协同抑制肝葡萄糖的产生。通过Akt/哺乳动物雷帕霉素靶蛋白(mTOR)途径产生IL-10需要胰岛素和肠道微生物来源的LPS升高。事实上,胰岛素受体的骨髓特异性敲除或突变TLR4骨髓细胞的骨髓移植会导致糖异生基因表达增加和糖耐量受损。此外,骨髓特异性Akt1和Akt2敲除导致相似的表型,这种表型可以通过额外敲除TSC2(一种mTOR抑制剂)来挽救。在肥胖症中,由于巨噬细胞中的胰岛素抵抗,导致IL-10的产生受到损害,而腺病毒介导的IL-10的表达改善了餐后高血糖。因此,内源性激素和肠道环境对进食的协调反应是餐后血糖的关键调节因素。
引言
胰岛素抵抗和胰岛素分泌缺陷在不同程度上促进了2型糖尿病的发病机制。据报道,细胞应激和由此产生的炎症是导致这些病理状态的重要过程(Wellen和Hotamisligil,2005)。肝脏对进食的适应是维持代谢稳态中最重要的生理反应之一。据报道,禁食过程中糖异生基因的表达是由通过叉头盒O1(FoxO1)来调节的,并且在进食后通过其胰岛素信号介导的核输出来抑制[Dong et al., 2008]。然而,有趣的是,即使肝脏中胰岛素信号级联的关键成分不足,也能观察到进食后糖异生基因表达的抑制(Lu et al.,2012),这表明除了肝脏胰岛素信号级联之外的其他途径可能具有调节作用。
肠道菌群已被证明是肥胖发病机制中的重要参与者,它们中有许多细菌产生LPS,这种物质能通过Toll样受体4(TLR4)强烈诱导多种细胞类型中的基因表达。产生LPS的细菌或LPS被认为会加剧肥胖诱导的代谢紊乱的发展(Cani et al.,2007年;Kim et al.,2012年)。另一方面,据报道,LPS的生理浓度会增加上皮细胞的通透性(Guo et al.,2013),这突出了LPS的潜在生理作用。实际上,有报道指出,在非肥胖状态下,进食后血液中的LPS水平会升高(Dror et al.,2017),然而,这种升高的含义尚不清楚。
通过免疫细胞如巨噬细胞引起的慢性炎症已被证明是代谢稳态失调的一个重要因素(Donath 和 Shoelson, 2011; Kamei et al., 2006; Kobayashi et al., 2011; Nishimura et al., 2009; Toda et al., 2014; Ueki et al., 2004),然而,巨噬细胞也被报道通过Th2细胞因子的作用来维持代谢稳态(Lee et al., 2015; Qiu et al., 2014)。在慢性炎症和代谢的背景下,已经对髓系细胞(包括巨噬细胞)的胰岛素信号级联中的激酶进行了分子水平的研究(Jiang et al., 2014; Kawano et al., 2012; Mauer et al., 2010),但巨噬细胞在对进食的急性反应中的作用尚未有报道。
在这项研究中,我们调查了肠道菌群、脂肪组织巨噬细胞(ATMs)和胰岛对进食的协调反应及其对控制餐后血糖的影响。在这项工作的过程中,我们发现由胰岛素和LPS诱导的巨噬细胞衍生的白细胞介素-10(IL-10)与胰岛素合作抑制肝脏的葡萄糖生成,并且这一过程的损害有助于肥胖中胰岛素抵抗的发展。
在这项研究中,我们研究了肠道微生物群、脂肪组织巨噬细胞(ATMs)和胰岛对喂养的协调反应及其对餐后血糖控制的影响。在这项工作的过程中,我们发现巨噬细胞来源的白细胞介素-10(IL-10),由胰岛素和LPS诱导,与胰岛素合作抑制肝葡萄糖的产生,这一过程的损害有助于肥胖中胰岛素抵抗的发展。
结果
ATMs中餐后IL-10的产生调节肝脏糖异生基因的表达
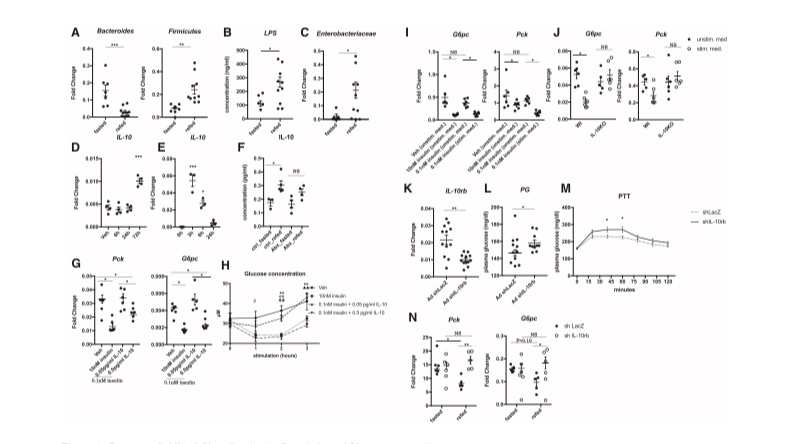
在进食过程中血清LPS浓度已被证明会升高,我们研究了LPS在进食中的潜在生理作用。进食后,小鼠小肠总质量显著增加(图S1A),主要拟杆菌门和厚壁菌门的相对丰度发生显著变化,拟杆菌减少,厚壁菌门增加(图1A)。虽然拟杆菌家族含有产生LPS的成员,但根据以往的报道,重新进食后血清LPS浓度升高(图1B),肠杆菌科的丰度也增加(图1C)。这些结果通过16S核糖体测序得到证实,发现大肠杆菌的丰度显著增加,大肠杆菌是一种产生具有强大基因诱导特性的LPS的物种(Vatanen et al.,2016)(图S1B)。为了评估进食后小肠内因素的影响,我们尝试尽可能地向十二指肠口服禁食和进食后的小肠内容物,并在30分钟后进行分析。虽然进食后小肠的内容物与胃的内容物相比没有提高血糖水平(图S1C),但在肝脏中可以检测到门静脉胰岛素和LPS的增加,以及抑制糖异生基因G6pc的表达水平(图S1D-S1F),这表明小肠内容物的调节作用。由于已知LPS可以刺激免疫细胞,我们决定探索在生理和病理生理条件下,LPS的增加在葡萄糖稳态调节中的作用。
首先,我们评估了LPS刺激的巨噬细胞的基因表达谱。虽然如先前报道的那样,LPS刺激巨噬细胞在数小时内诱导了炎症细胞因子的基因表达(图S1G)(Xaus et al.,2000),但在骨髓源性巨噬细胞中,Th2细胞因子IL-10仅在第3天被诱导(BMDMs;图1D)。然而,当LPS和胰岛素刺激巨噬细胞时,IL-10的诱导时间缩短至3小时内,这两种细胞在餐后血清中均升高(图1E和S1H)。单独的胰岛素并不能诱导IL-10的产生(图S1I)。根据这些数据,在再喂食1小时后,门静脉中IL-10的浓度升高(图1F),这增加了IL-10可能有助于喂食后的肝脏反应的可能性。在接受口服抗生素治疗的小鼠中,这种餐后反应减弱了,这表明了一个依赖于源自肠道微生物群的LPS的过程(图1F)。
由于在瘦小鼠附睾白色脂肪组织(WAT)中的脂肪组织巨噬细胞(ATMs)可以检测到IL-10表达的升高(图S1J),其中常驻巨噬细胞在正常饮食条件下每个脂肪垫约为1-3 x 10^5个,因此对进食的IL-10分泌很可能来自内脏脂肪组织(图S1K)。据报道,胰岛素在10 nM的浓度下可以抑制原代肝细胞中的糖异生基因表达,尽管这样的浓度比进食后在门静脉中可检测到的水平高100倍(约0.1 nM;Haluzik et al., 2004)。尽管分别用0.5 pg/mL的IL-10或0.1 nM的胰岛素刺激,这些分子在进食后门静脉中的生理浓度,并未改变糖异生基因磷酸烯醇丙酮酸羧激酶(Pck)和葡萄糖-6-磷酸酶催化亚基(G6pc)的表达(图S1L),但同时受到这两种因子刺激的肝细胞表现出糖异生基因表达的抑制,这在用与禁食状态下门静脉中浓度相对应的低10倍的IL-10浓度刺激后并未观察到(图1G)。与这种基因表达谱一致,用餐后水平的IL-10和胰岛素刺激的肝细胞培养物中葡萄糖浓度的增加被抑制到与用10 nM胰岛素刺激的肝细胞相似的水平,而在仅用餐后水平的胰岛素刺激的肝细胞中未观察到显著的抑制(图1H)。
为了探究源自巨噬细胞的因素是否真的能够抑制肝细胞中的糖异生基因表达,我们在含有生理水平胰岛素的BMDM(骨髓来源的巨噬细胞)培养基中培养肝细胞。尽管未刺激的巨噬细胞培养基未能抑制肝细胞中的糖异生基因表达,但预先用LPS和胰岛素处理的巨噬细胞培养基显著抑制了这些基因(图1I)。此外,来自IL-10基因敲除小鼠的巨噬细胞培养基未能抑制糖异生基因表达(图1J),这表明是一个依赖于IL-10的过程。在用来自IL-10基因敲除小鼠的巨噬细胞培养基刺激的肝细胞中,Stat3磷酸化被抑制,这支持了IL-10通过Stat3磷酸化传递信号的观点(图S1M)(Shen et al., 2000)。这些数据共同表明,在生理条件下,维持餐后血糖稳态的过程中,多种刺激因素发挥作用,其中与胰岛素协同作用的IL-10似乎很重要。
为了进一步阐明IL-10在进食反应中的潜在作用,我们尝试使用腺病毒介导的方法对IL-10受体β(IL-10rb)亚基进行基因下调,该受体的组成性表达信号亚基(Shouval et al., 2014)。我们生成了一个携带针对IL-10rb的短发夹RNA(shRNA)的腺病毒载体。与感染对照载体的小鼠相比,注射这种腺病毒的小鼠肝脏中IL-10rb基因的表达被抑制了一半(图1K)。基因下调也导致自由进食的小鼠血糖水平升高(图1L),以及在禁食后重新再进食时血糖水平的加剧升高(图S1N)。在这种抑制模型中,当自由进食时,通过腹腔注射丙酮酸后血糖水平升高,显示出体内餐后肝脏葡萄糖产生增加(图1M)。在IL-10rb基因下调模型中的血浆胰岛素浓度也更高(图S1O),这共同表明餐后胰岛素活性受损。在IL-10rb缺乏小鼠的肝脏中,Stat3磷酸化被抑制,在这些小鼠中通过IL-10受体支持的IL-10信号传导存在缺陷(图S1P)。这些小鼠肝脏中G6pc和Pck表达的抑制也明显减弱,表明IL-10信号通路与胰岛素合作,介导了进食后糖异生基因的抑制(图1N)。在其他据报道影响餐后反应的基因中(Rhee et al., 2003),PGC-1a在IL-10rb抑制模型和对照组中均显著受到抑制,而HNF4a在这个短时间内未显示抑制(图S1Q),表明这些基因在该模型中未受影响。
从微生物群中提取的LPS通过TLR4在髓系细胞中抑制餐后糖异生基因
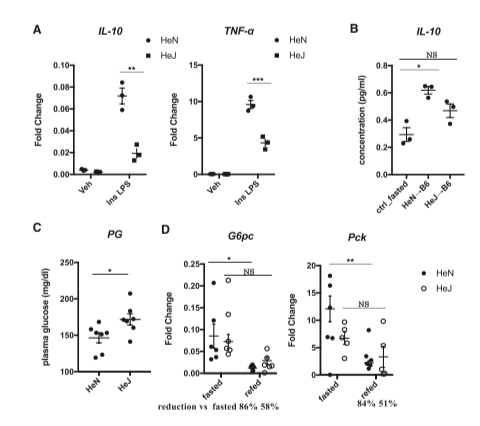
为了探索微生物群中LPS在调节肝脏糖异生基因表达中的潜在作用,我们使用TLR4突变的C3H/HeJ小鼠的BMDMs(骨髓来源的巨噬细胞)研究了在胰岛素和LPS共同刺激下IL-10的诱导情况,结果发现与对照小鼠的细胞相比,IL-10的诱导显著受到抑制(图2A)。接下来,我们对C3H/HeJ小鼠向野生型小鼠进行了骨髓移植实验。与HeN移植小鼠相比,C3H/HeJ骨髓移植小鼠门静脉IL-10浓度的升高较弱(图2B)。移植小鼠在自由进食时血糖水平较高,并且进食后糖异生基因的抑制减弱(图2C和2D);这些结果支持了LPS信号在髓样细胞中对餐后糖异生抑制的重要作用的观点。值得注意的是,与胰岛素抵抗发病机制有关的细胞因子肿瘤坏死因子-α(TNF-α)在C3H/HeJ小鼠的BMDMs中的诱导受到抑制。由于体内糖代谢失调,我们的研究结果共同支持了餐后信号诱导的其他因素如IL-10在正常瘦小鼠餐后血糖调节中的作用。
髓系特异性敲除IR破坏了对喂养的反应
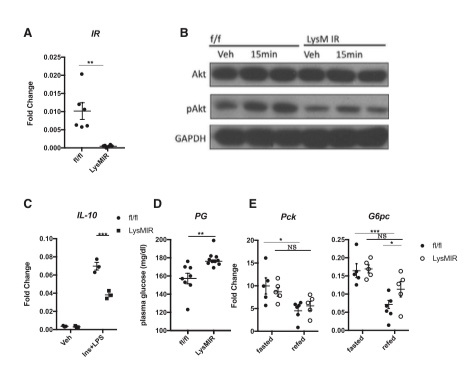
为了测试胰岛素信号在瘦小鼠巨噬细胞对食物摄入的生理反应中的作用,我们利用了LysM-Cre:胰岛素受体-条件性敲除(LysMIR)小鼠作为髓系特异性胰岛素受体(IR)敲除模型。来自LysMIR小鼠的BMDMs显示出IR表达的显著抑制(图3A),对胰岛素刺激的Akt磷酸化反应也减少(图3B)。这些细胞在胰岛素和LPS刺激下IL-10的诱导也受到抑制(图3C)。在肥胖高胰岛素血症小鼠中,髓系特异性IR缺乏已被报道可以改善胰岛素抵抗(Kubota et al., 2018; Mauer et al., 2010)。当喂食正常饮食时,LysMIR小鼠表现出更高的血糖值(图3D),并且在重新进食后这些小鼠的糖异生基因表达并未受到抑制(图3E)。这些数据表明,在瘦小鼠中,巨噬细胞中的胰岛素信号通过抑制糖异生基因表达来防止进食后血糖水平的上升。在LysMIR小鼠中未检测到体重差异,并且这些小鼠在胰岛素和糖耐量测试中的血糖浓度差异微妙(图S2A–S2C),但在糖耐量测试中的胰岛素浓度较高,支持巨噬细胞胰岛素信号在维持瘦小鼠胰岛素敏感性中的作用(图S2D)。
餐后信号以akt-mtor依赖的方式诱导巨噬细胞中产生的IL-10
如上所述,通过胰岛素和LPS共同刺激,巨噬细胞能够迅速诱导IL-10的产生。为了探究这种诱导的分子机制,我们使用一种磷脂酰肌醇-3-激酶(PI3K)抑制剂处理了BMDMs,并发现这种处理有效抑制了IL-10的诱导,但对TNF-a没有影响(图 S3A)。这些结果促使我们研究Akt信号在通过诱导IL-10维持餐后血糖中可能的作用。因此,我们生成了髓系细胞特异性Akt1/Akt2双敲除(LysMCre:Akt1/Akt2-floxed [LysMDKO])小鼠。在LysMDKO小鼠的BMDM细胞中Akt表达降低了70%–80%(图4A),并且在对LPS和胰岛素刺激的反应中,检测到两种Akt异构体和哺乳动物雷帕霉素靶蛋白(mTOR)磷酸化缺陷(图4B和4C)。在LysMDKO小鼠的BMDMs中,胰岛素和LPS共同刺激诱导的IL-10明显受到抑制,这再次表明了akt介导的过程(图4D)。在细胞上清液中也观察到IL-10的产生受到抑制(图S3B)以及在LPS刺激下F4/80和IL-10的免疫荧光(图S3C),表明IL-10的产生依赖于Akt。
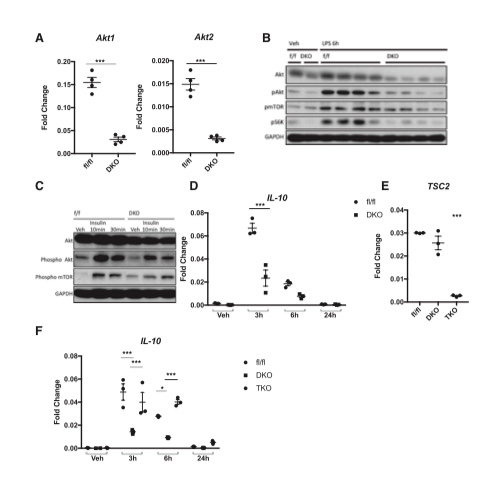
在Akt下游的信号通路中,我们首先检测了FoxO1在IL-10诱导中的作用。在胰岛素和LPS共刺激下,除了双敲除Akt1和Akt2外,还未能诱导IL-10的表达(图S3D和S3E)。然后,我们通过组织特异性敲除结节性硬化复合体2(TSC2;Inoki等人,2002),研究了mTOR信号,Akt下游通路对餐后IL-10产生的影响并抑制mTORC1的活性。我们测试了其敲除与Akt1和Akt2破坏同时进行的效果,使用LysM-Cre:Akt1/Akt2/TSC2-floxed(LysMTKO)小鼠。LysMTKO小鼠中Akt表达被抑制到与LysMDKO小鼠巨噬细胞中相似的水平(图 S3F),并且LysMTKO BMDMs中TSC2表达也被抑制(图4E)。LysMTKO BMDMs中mTOR的磷酸化与对照小鼠相似,证实了这一信号的恢复(图 S3G)。LysMTKO小鼠中胰岛素和LPS共同刺激诱导的IL-10与对照动物相似,显示Akt-mTOR依赖的IL-10诱导(图4F)。
在小鼠中,髓系特异性敲除Akt1和Akt2表现出在餐后对糖异生基因的抑制不足
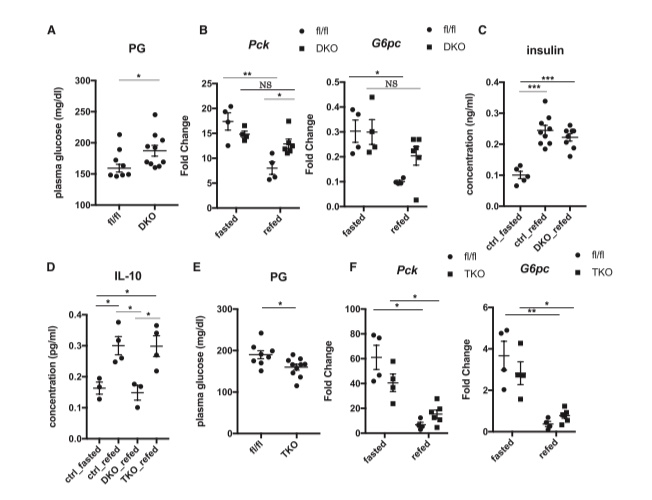
接下来,我们评估了巨噬细胞Akt信号通路在体内的作用。LysMDKO小鼠在自由进食条件下的血糖值比对照小鼠高(图5A)。通过禁食后重新进食,对照小鼠中糖异生基因的表达在数小时内被抑制,而在LysMDKO小鼠中则没有被抑制(图5B)。尽管LysMDKO小鼠和对照小鼠在餐后门静脉胰岛素浓度没有差异(图5C),但LysMDKO小鼠门静脉中IL-10浓度的餐后升高是不足的。在LysMTKO小鼠中IL-10的产生得到了恢复(图5D),进一步指出Akt/mTOR驱动的IL-10诱导在肝脏餐后稳态调节中的潜在作用。为了进一步评估巨噬细胞Akt-mTOR信号在维持餐后血糖中的作用,我们评估了LysMTKO小鼠的代谢特征。在自由进食条件下血糖值较低(图5E),并且在禁食后重新进食时糖异生基因表达被抑制(图5F)。结合体内外IL-10诱导的恢复,这支持了巨噬细胞产生的IL-10在进食后抑制糖异生基因表达中的作用,尽管Akt-mTOR途径诱导的其他因素也可能发挥作用的可能性仍然存在。此外,在LysMTKO小鼠中,胰岛素和葡萄糖耐量测试中观察到适度降低的葡萄糖值,而体重没有差异。在葡萄糖耐量测试中胰岛素浓度较低,表明这些小鼠具有显著的胰岛素敏感性(图S4A-S4D)。这一发现,加上LysMIR小鼠的胰岛素抵抗,表明这一过程有助于维持全身胰岛素敏感性。
肥胖小鼠ATMs中IL-10的表达降低,补充IL-10可提高胰岛素敏感性,同时抑制肝脏中的糖异生基因
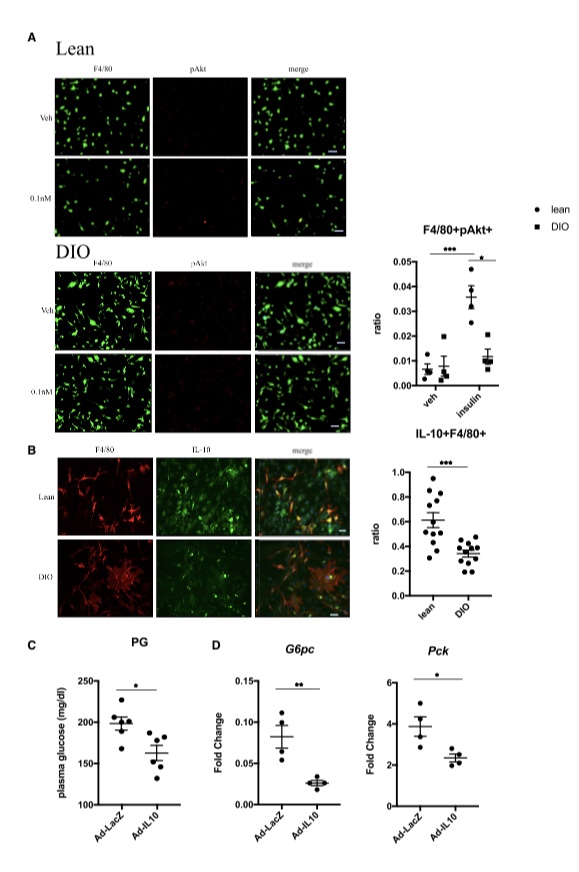
接下来,我们评估了IL-10在胰岛素耐药状态下的治疗潜力。当饮食诱导的肥胖(DIO)小鼠附睾(WAT)中的基质血管组分(SVF)细胞受到胰岛素刺激时,与瘦小鼠的SVF细胞相比,F4/80阳性脂肪组织巨噬细胞(ATMs)中磷酸化Akt阳性细胞的比例降低(图6A)。这些数据与过去在DIO小鼠中观察到的巨噬细胞胰岛素信号传导存在缺陷的报道一致(Kawano et al.,2012),并表明在病态肥胖状态的下巨噬细胞中,胰岛素信号的生理作用被破坏。值得注意的是,LysMDKO小鼠在高脂饮食(HFD)下的代谢特征与DIO小鼠没有不同(图S5A-S5D),这可能是因为DIO小鼠以及肥胖的LysMDKO小鼠中巨噬细胞的Akt信号受损。
因此,我们尝试评估IL-10对DIO(饮食诱导的肥胖)小鼠糖异生基因表达的影响。首先,我们检测了瘦小鼠和DIO状态下巨噬细胞中的IL-10产生。在DIO小鼠附睾WAT中的ATMs(脂肪组织巨噬细胞)中,IL-10阳性细胞的比例显著降低(图6B),这表明IL-10的产生存在缺陷。向DIO小鼠注射表达人IL-10的腺病毒载体(Ad-IL-10)后,与注射对照腺病毒的小鼠相比,几天内进食状态下的血糖水平降低(图6C),并抑制糖异生基因表达(图6D)。总体而言,我们的数据为IL-10在巨噬细胞中对进食诱导的协调变化(包括来自肠道的LPS和来自胰腺的胰岛素)产生的潜在治疗作用提供了证据,这一过程在巨噬细胞胰岛素抵抗的发展中受到损害。
讨论
在本研究中,我们提出了一种机制,即进食后免疫过程和胰岛素作用的结合维持葡萄糖稳态。进食后,肠道菌群的组成发生改变,导致肠杆菌科和血清LPS浓度增加。尽管产生LPS的Bacteroides门在进食后减少,但该门的LPS被报道具有相对较弱的基因诱导潜力(Vatanen et al., 2016),因此我们的整体结果与餐后LPS信号通路显著增加一致。结合在抗生素处理小鼠中观察到的餐后IL-10诱导的中断以及用TLR4突变骨髓移植的致死性照射小鼠中餐后糖异生基因抑制的缺陷一致,这些数据表明LPS可以通过巨噬细胞产生的因子调节葡萄糖稳态。通过基因敲除和体外共培养研究,我们已经证实了Th2细胞因子IL-10的重要作用,该因子在胰岛素与LPS信号通路协同快速诱导的。然而,还需要进一步的研究,以精确阐明肠道微生物群如何对食物产生反应,以及这些食物敏感因子是否直接作用于巨噬细胞或与其他髓样细胞类型合作。从分子角度来看,我们的体外实验结果表明,巨噬细胞中的PI3K通路有可能通过诱导IL-10驱动餐后反应。采用条件性敲除模型的研究表明,胰岛素与LPS协同激活巨噬细胞中的Akt-mTOR通路对于维持餐后葡萄糖稳态的重要性。实际上,我们已经证明,胰岛素和TLR4介导的信号对于巨噬细胞中IL-10的诱导和餐后糖异生基因的抑制都是必要的。
尽管IL-10的代谢作用仍存在争议(Cintra et al., 2008; Kowalski et al., 2011),但已被证明肝脏中的STAT3激活可以抑制PGC-1a介导的糖异生基因表达(Inoue et al., 2006)。在本研究中,我们发现IL-10信号对于正常抑制糖异生基因表达是必要的,并且生理浓度的IL-10和胰岛素可以在原代肝细胞中抑制葡萄糖产生。我们的数据表明,由胰岛素和肠道信号共同诱导的巨噬细胞中的IL-10在餐后血糖调节中发挥关键作用,尽管最近在IL-10基因敲除小鼠中报道了通过诱导米色脂肪生成而增加能量消耗(Rajbhandari et al., 2018)。这份报告和我们的研究共同表明,基线时的IL-10对于维持体重是必需的,而餐后门静脉中的增加会抑制糖异生。因此,需要进一步的研究来探索IL-10对肥胖相关疾病的治疗价值。
先前的研究表明,在DIO(饮食诱导的肥胖)模型中,小鼠巨噬细胞中IR(胰岛素受体)基因的破坏可以防止胰岛素抵抗的发展(Mauer et al., 2010)。最近有人提出,在肥胖高胰岛素血症小鼠中,IR破坏上调的Irs2可以通过Foxo1的核输出增加IL-4/Irs2介导的抗炎基因表达,有趣的是,IL-10的表达并未改变(Kubota et al., 2018)。相反,在本研究中,瘦小鼠中髓系特异性IR敲除小鼠的血糖值升高,并且进食后糖异生基因表达的抑制存在缺陷。这与IR缺乏的巨噬细胞中IL-10诱导不足一起,表明胰岛素信号在进食过程中起着重要作用。此外,由于在我们的髓系胰岛素信号中断模型中可以检测到胰岛素抵抗,并且在增加mTOR信号的LysMTKO模型中得到缓解,Akt/mTOR介导的巨噬细胞在胰岛素和LPS刺激下的IL-10产生可能反过来在维持全身胰岛素敏感性方面发挥作用,尽管本研究使用条件敲除模型表明,我们不能完全排除由Akt/mTOR信号通路和其他机制增加的其他因素的潜在作用。未来的研究可能会进一步阐明调节餐后抑制糖异生的因素。
在肥胖小鼠中观察到Akt激活以及ATMs(脂肪组织巨噬细胞)产生IL-10的不足,这可能与巨噬细胞中的胰岛素抵抗有关,也可能受到菌群失调的影响。这些小鼠肝脏中IL-10的表达改善了葡萄糖代谢,说明了IL-10信号在肝脏中缓解肥胖引起的肝脏胰岛素抵抗的潜力。因此,对食物反应发生变化的肠道因素,以及被它们刺激的巨噬细胞内的细胞内信号通路,是可以用来缓解餐后血糖控制受损的胰岛素抵抗状态的潜在工具。
根据本报告中提供的数据,我们提出了一种动态调节葡萄糖稳态的机制,其中巨噬细胞对餐后胰岛素分泌和肠道菌群的变化作出反应,随后通过Akt/mTOR信号通路表达IL-10,并抑制肝脏中的糖异生基因表达。这一机制有可能为基于免疫细胞的治疗肥胖引起的糖尿病的治疗策略的发展奠定基础。
免责声明
以上部分内容来源于外网我们重在信息分享,版权归属原作者或原刊发平台所有,如有侵权、信息有误或其他异议,请联系我们,我们将在24小时内删除或整改。
复合免疫 健康活力





























