
LPS通过TNF-α/TNFR1途径降低氧化应激来保护对乙酰氨基酚诱导的肝毒性。
LPS可缓解肝损伤
摘要:
大量有力的证据表明肠源性的LPS在各种肝损伤疾病中起着重要作用;然而,肠源性LPS的作用对APAP过量导致的急性肝损伤的作用尚不清楚。本研究旨在探讨肠源性LPS对APAP诱导的肝损伤的影响。我们的研究结果显示,使用多种抗生素减少肠源性LPS可显著加重APAP诱导的肝损伤,并增加小鼠的死亡率。相比之下,外源性LPS预处理可以逆转APAP诱导的小鼠和大鼠肝毒性。我们观察到经过LPS预处理后,肝脏中TNF-α的分泌显著增加。此外,TNF-α或TNFR1的缺失可以抑制LPS对APAP诱导的肝毒性的保护作用,这表明TNF-α/TNFR1途径是保护免受APAP诱导的肝损伤所必需的。从机理上讲,LPS通过上调肝脏GSH的表达,降低肝组织中MDA的水平,并上调APAP注射后几种抗氧化基因的表达来降低氧化应激。然而,在缺乏TNF-a或TNFR1的大鼠的肝组织中,肝脏GSH的产生并没有增强,且在LPS和APAP共同处理后,MDA水平并没有降低。上述结果表明,以上结果表明,LPS通过TNF-a/TNFR1途径缓解了APAP诱导的氧化应激。
引言
APAP是一种常用的解热镇痛药。然而,据报道,APAP引起的肝损伤是各国最常见的药物肝毒性[1,2]。从机理上讲,APAP可以被肝细胞色素P450代谢产生N-乙酰基p苯醌亚胺(NAPQI)。之后,NAPQI通过与谷胱甘肽(GSH)反应来解毒[3,4]。然而,当肝脏GSH耗尽时,过量的NAPQI与细胞蛋白共价结合,最终导致线粒体通透性转变和细胞死亡[5,6]。
肝脏通过门静脉接收来自肠道的静脉血,因此是第一个能够防御肠道来源的微生物群产物的肠外器官[7]。越来越多的证据表明,肠道微生物群产物与人类肝病之间存在明显的关联[8-10]。LPS是肠道菌群的主要成分。肠源性LPS已被证实在各种肝损伤疾病的发展中起着至关重要的作用,包括酒精性肝病、病毒性肝炎、肝硬化和肝癌[11-13]。然而,到目前为止,肠源性LPS在APAP诱导的急性肝损伤中的影响尚不清楚。
LPS作为一种细菌成分,影响抗炎和促炎细胞因子的产生,特别是肿瘤坏死因子-α (TNF-α),它是参与LPS和革兰氏阴性细菌感染发病机制的最关键的介质之一。发现LPS以剂量依赖的方式刺激TNF-α的分泌[14,15]。然而,LPS是否通过TNF-α影响APAP诱导的肝损伤仍有待确定。在本研究中,我们旨在研究LPS和TNF-α对APAP诱导的肝毒性的影响。
结果
1、肠源性LPS的减少加重了APAP诱导的肝损伤
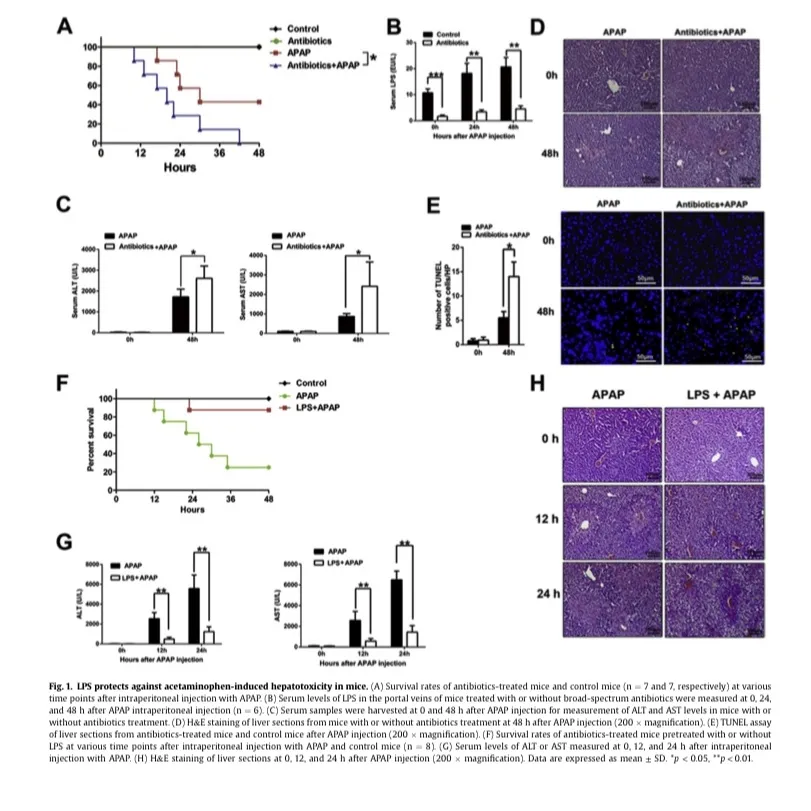
为了研究肠源性LPS在APAP诱导的急性肝损伤中的作用,我们评估了腹腔注射APAP (600 mg/kg)后LPS对APAP诱导的死亡率的影响。发现用广谱抗生素治疗降低了肠源性LPS的水平。用APAP与抗生素联合治疗的小鼠的死亡率高于用APAP单独治疗的小鼠的死亡率(图1A)。为了进一步验证肠源性LPS对APAP诱导的肝毒性的影响,抗生素组和对照组均腹腔注射300 mg/kg APAP(图1B)。结果显示,与对照组相比,给予抗生素的小鼠血清中ALT和AST水平高于对照组(图1C)。肝切片的组织学分析也显示,使用抗生素治疗的小鼠的肝组织坏死比对照组小鼠更明显(图1D)。TUNEL染色结果显示,与对照组相比,注射APAP后,经抗生素处理的小鼠的DNA片段更为明显(图1E)。上述发现表明肠源性LPS的减少加重了APAP诱导的小鼠肝损伤和死亡率。
2、LPS预处理可保护小鼠和大鼠免受APAP肝毒性的影响
为了进一步验证LPS在APAP诱导的肝损伤中的作用,我们接下来探讨了外源性LPS预处理是否可以保护抗生素处理的小鼠免受APAP诱导的肝损伤。抗生素组小鼠经外源性LPS预处理,腹腔注射(250 mg/kg),每日1次,连续2天。结果显示,外源性LPS预处理降低了APAP诱导的抗生素处理小鼠的死亡率(图1F),这得到了血清ALT和AST水平较低,以及外源性LPS预处理小鼠肝坏死显著减少的支持(图1g和H)。以上结果表明,外源性LPS显著保护了抗生素治疗的小鼠免受APAP诱导的肝损伤。
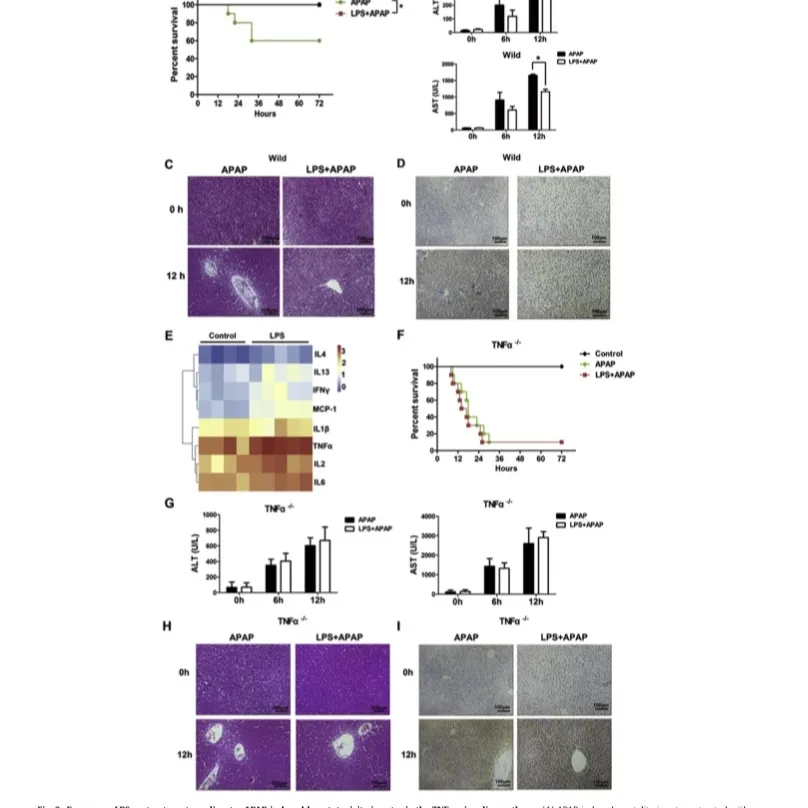
LPS预处理可改善APAP诱导的大鼠急性肝损伤。lps预处理的大鼠在APAP给药后死亡率较低(图2A),这是由血清ALT和AST水平降低和肝坏死明显减少所支持的(图2b和C)。活化的caspase-3是测定细胞凋亡率的可靠指标。我们的结果表明,与单独使用APAP的大鼠相比,同时使用LPS和APAP的大鼠肝脏中caspase-3阳性细胞的数量显著减少(图2D)。
3、TNF-a/TNFR1通路对LPS预处理诱导的肝保护至关重要
结果显示,注射LPS后,肝脏中TNF-a水平表达上调(图2E)。为了进一步证实TNF-a参与LPS预处理诱导的肝保护,TNFa/大鼠与APAP或单独APAP联合处理。我们发现,LPS预处理并没有提高TNF-a/大鼠的存活率(图2F)。此外,LPS处理的TNF-AS/大鼠的ALT和AST水平没有明显变化(图2G),肝坏死也没有减轻(图2h和I)。以上结果表明,LPS对TNF-a/大鼠的保护作用已被消除。
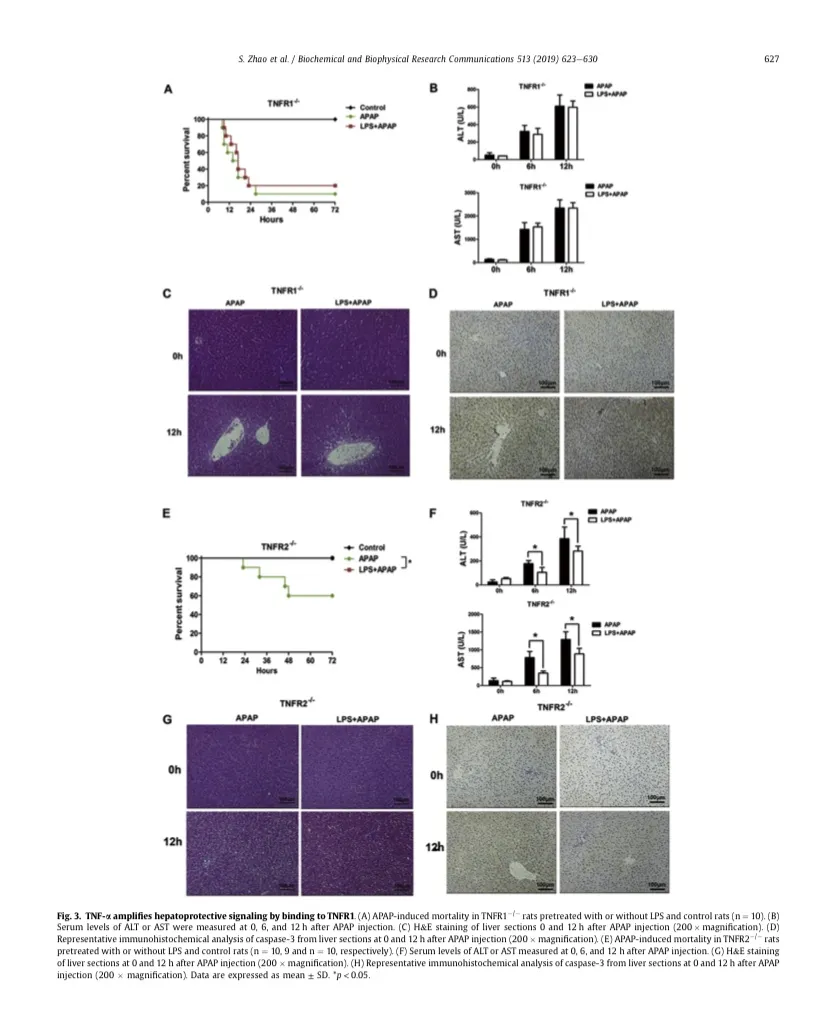
TNF-a通过两个已知的跨膜受体TNFR1和TNFR2 [16]发挥广泛的生物学效应。结果表明,LPS预处理并没有增加APAP处理的TNFR1/大鼠的存活率(图3A),也没有导致APAP诱导的TNFR1/大鼠肝损伤的显著变化(图3b、C和3D)。然而,LPS预处理可改善APAP诱导的TNFR2/大鼠急性肝衰竭,显示为较低的死亡率(图3E),降低ALT和AST水平,并减少肝坏死(图3f、G和3H)。以上结果表明,TNF-a通过与TNFR1而不是TNFR2结合而发挥肝保护作用。
4、LPS可减轻APAP诱导的肝脏氧化应激
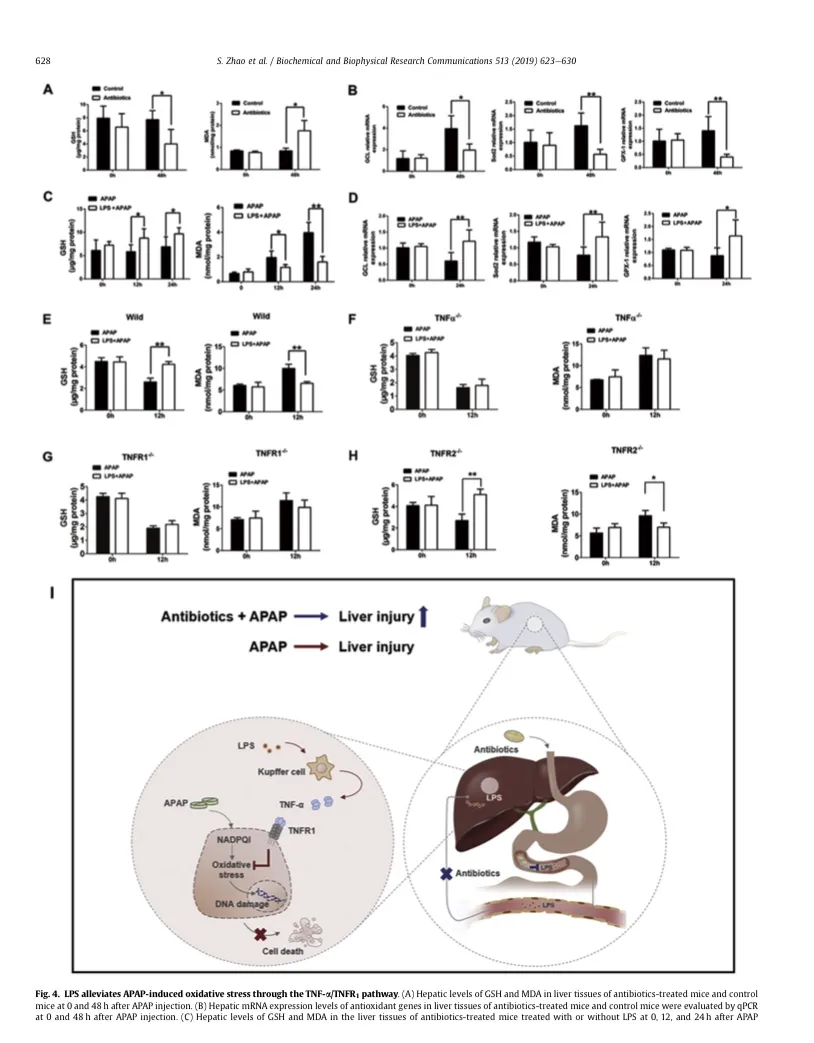
为了研究LPS是否能影响APAP的代谢,我们评估了肝组织中GSH和MDA的水平。我们的研究结果显示,已知的肝脏GSH的水平在对乙酰氨基酚代谢物NAPQI的解毒过程中具有重要作用,抗生素治疗小鼠低于对照组;另一方面,与对照组相比,抗生素治疗小鼠的MDA水平增加(图4A)。考虑到氧化应激与ROS清除系统相关,我们接下来进行了qPCR分析,以评估经抗生素处理的小鼠和对照组中一些关键基因的肝脏表达水平。结果表明,与对照组相比,抗生素处理小鼠的抗氧化基因如Gpx-1、Sod2和GCL的mRNA水平被下调(图4B)。此外,LPS预处理通过上调肝脏GSH的表达,降低肝组织中MDA的水平(图4c和E),并上调几种抗氧化基因的表达(图4D)来缓解氧化应激。以上结果表明,外源性LPS预处理通过恢复肝脏抗氧化系统功能来防止APAP诱导的肝毒性。
5、LPS通过TNF-a/ TNFR1途径缓解APAP诱导的氧化应激
我们的结果显示,TNF-a/大鼠的肝组织中肝脏GSH的表达没有增强,而经LPS预处理后,APAP处理后MDA水平没有降低(图4F)。在TNFR1/大鼠中也观察到同样的现象(图4G)。然而,外源性LPS预处理通过上调TNFR2/大鼠肝脏GSH的表达和降低MDA的水平来降低氧化应激(图4H)。以上结果表明,LPS通过TNF-a/TNFR1信号通路缓解APAP诱导的氧化应激。
讨论
越来越多的研究表明,维持肠道菌群和肝脏之间的稳态对人类健康起着重要作用[7,8]。作为肠道菌群衍生细菌产物的主要成分之一,肠道源性LPS在各种肝损伤疾病中发挥着重要作用[17]、[18]、[19]。在本研究中,我们发现肠源性LPS对减轻APAP诱导的肝损伤至关重要。抗生素治疗降低小鼠肠道源性LPS水平,加重了APAP诱导的肝损伤,增加了死亡率。以上研究结果提示,长期使用多种抗生素可减少LPS的形成,并增加APAP诱导的肝损伤的严重程度。
TNF-a主要由库普弗细胞响应LPS [20,21]而产生。几十年的研究已经证实,TNF-a是复杂的细胞因子网络中起着核心作用,不仅调节促炎反应,还涉及包括细胞间通讯在内的多种过程[22]。在哺乳动物中,TNF与TNFR1的结合可以通过TAK1和IkB激酶(IKK)依赖的NF-kB [23]的激活来触发促生存信号通路。同时,我们的研究结果证实了TNF-a的分泌对于LPS预处理诱导的APAP诱导的肝损伤保护至关重要。损伤后,TNF-a在血管舒张后迅速迁移到损伤组织中,抑制进一步的细胞死亡,激活干细胞,促进上皮细胞增殖[24]。此外,我们的研究结果证明,LPS诱导的肝保护是由TNF-a通过TNFR1信号引起的,而不是TNFR2。
肝氧化应激和线粒体功能障碍被认为是APAP诱导的急性肝脏的中心介质损坏[25]。氧化应激导致线粒体过氧亚硝酸盐的产生,导致线粒体蛋白的硝化和线粒体DNA损伤,最终导致线粒体通透性转变和细胞死亡[26]。此外,APAP代谢物NAPQI通过与谷胱甘肽(GSH)反应而立即解毒,形成无毒的代谢物半胱氨酸[27]。与上述研究结果一致,我们目前的研究结果表明,LPS对APAP诱导的活损伤的保护作用主要是由于其减轻肝氧化应激的能力。特别是,LPS的消耗会加剧APAP诱导的肝组织中ROS的积累、脂质过氧化和GSH的消耗,而外源性LPS的补充则逆转了这些变化。LPS介导的肝脏氧化应激的降低也与一组抗氧化基因的表达上调有关。TNF-a已被证明可以调节活性氧(ROS)和活性氮(RNS)的生成。此外,TNF诱导的NF-kB信号通路不仅能导致抗凋亡基因的转录,而且还能导致降低细胞内ROS水平[28]的基因的转录。我们的研究结果显示,野生型和TNFR2/大鼠经LPS预处理后,氧化应激有所减轻,但在TNF-a/和TNFR1/大鼠中,这种作用并没有降低。以上研究结果表明,LPS通过TNF-a/TNFR1通路降低氧化应激,对ROS介导的肝损伤具有保护作用。
总结来说,我们的研究结果表明,通过抗生素治疗减少肠源性LPS加重了APAP诱导的肝损伤。LPS预处理可通过抑制氧化应激,显著减轻APAP诱导的肝损伤。此外,研究结果证明,LPS预处理显著增加了肝脏中TNF-a的分泌,并且需要TNF-a/ TNFR1通路来建立对APAP诱导的肝损伤的肝保护,以减少APAP诱导的氧化应激(图4I)是必需的。
免责声明
以上部分内容来源于外网我们重在信息分享,版权归属原作者或原刊发平台所有,如有侵权、信息有误或其他异议,请联系我们,我们将在24小时内删除或整改。
复合免疫 健康活力





























