
口服LPS通过改善高脂血症、促炎介质和氧化反应,预防高脂饮食喂养的apoe缺陷小鼠动脉粥样硬化的发展
口服LP可以改善动脉粥样硬化的发展
注:本文为中、日、英三种语言,下方附有中文翻译,供您查阅!
動脈硬化とLPS
LPSは、動脈硬化の予防に効果を持つことが示唆されています。
一般に「動脈硬化」といえばアテローム性動脈硬化を指すことが多いです。アテローム性というのは、「お粥状の」とでもいうような意味で、アテローム性動脈硬化(Atherosclerosis)とは、動脈に粥状の隆起(プラーク)が発生する状態のことです。
血管に傷ができると、コレステロールを運ぶLDLが血管内膜にひっかかり、そこで酸化され不要物となります。不要物である酸化LDLは、通常、マクロファージが食べて処理します。食べた後に残るコレステロールはHDLに引き渡されてリサイクルされます。しかし処理しきれない大量の酸化LDLがあると、マクロファージは酸化LDLをため込んだまま死んでしまい、あとには、お粥状のコレステロールの塊が残ります。これがプラークです。プラークが大きくなると、血管が狭められたり、プラークの破裂によって血栓ができたりします。
マクロファージは血管内を綺麗にする
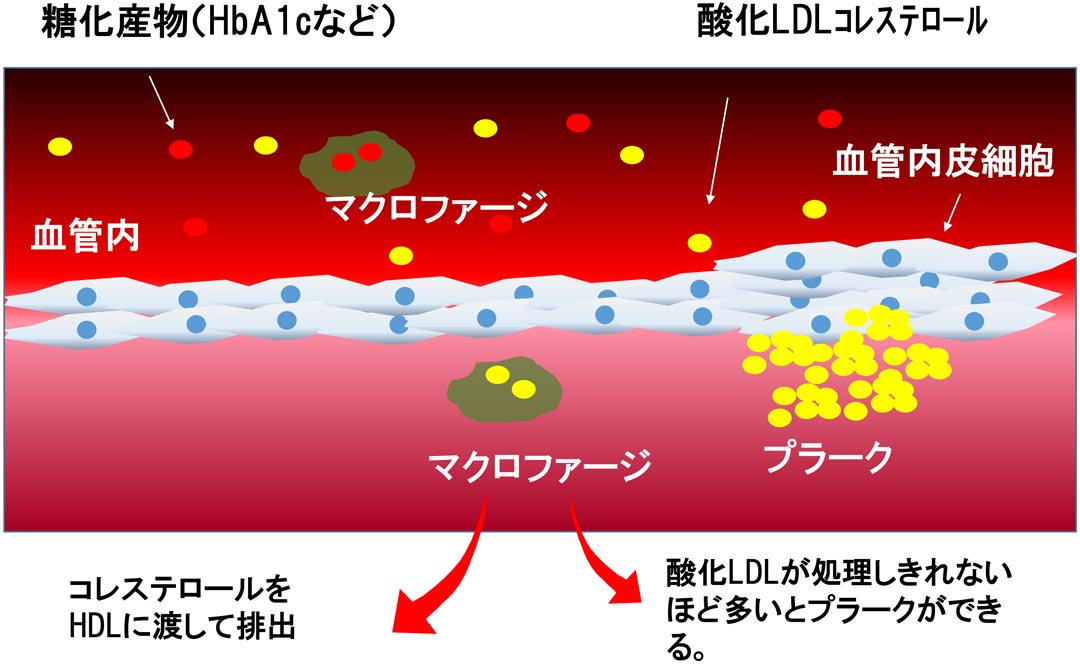
この話を聞くと、マクロファージを活性化すると、動脈硬化を促進するのではないかと思うヒトがいますが、それは大変な間違いです。処理しきれない量の酸化LDLがあると動脈硬化のリスクが高まるのであって、あくまでもマクロファージが活発に機能する事で血液が綺麗に保たれています。このことから、マクロファージを活性化するLPSが動脈硬化の予防にも効果があると考えられます。
実際に、動脈硬化モデルマウスに高脂肪食を食べさせる実験で、マクロファージを活性化するLPSを与えると、与えないマウスに比べて体重増加が抑制され、大動脈血管プラークの発生が少ないことがわかっています(*1)。
LPSは高脂肪食の影響を抑制する
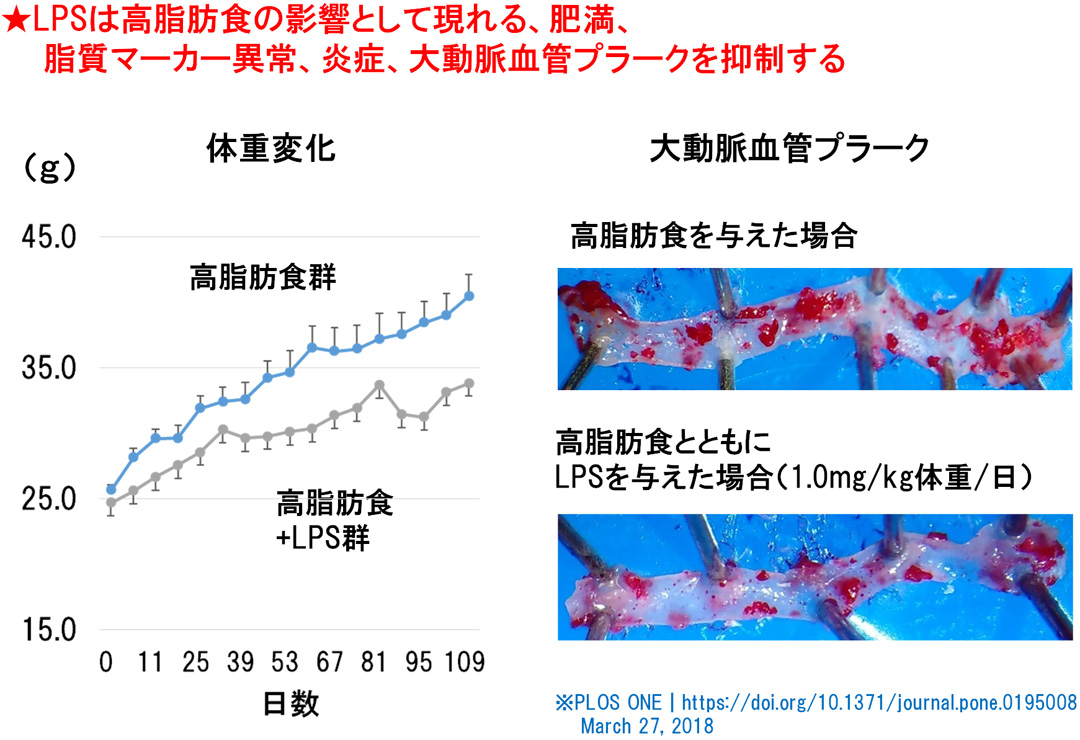
(*1)Oral administration of Pantoea agglomeransderived lipopolysaccharide prevents development of atherosclerosis in high-fat diet-fed apoE-deficient mice via ameliorating hyperlipidemia, pro-inflammatory mediators and oxidative responses, PLOS ONE | https://doi.org/10.1371/journal.pone.0195008 March 27, 2018
中文翻译:
LPS(脂多糖)已被暗示对预防动脉粥样硬化具有效果。 通常提到“动脉硬化”,大多数情况下是指动脉粥样硬化。所谓的动脉粥样硬化(Atherosclerosis),是指动脉内出现类似粥状的隆起(斑块)的状态。 当血管受伤时,携带胆固醇的LDL(低密度脂蛋白)会附着在血管内膜上,并在那里氧化变成有害物质。这些氧化的LDL通常会被巨噬细胞吞噬并处理掉。吞噬后剩余的胆固醇会被HDL(高密度脂蛋白)带走并进行回收。然而,如果存在大量无法处理的氧化LDL,巨噬细胞就会在充满氧化LDL的情况下死亡,留下类似粥状的胆固醇块。这就是斑块。斑块变大后,可能会导致血管变窄,或者因斑块破裂而形成血栓。
巨噬细胞清洁血管内部
听到这个,可能有人会认为激活巨噬细胞会促进动脉粥样硬化,这是一个非常大的误解。动脉粥样硬化的风险增加是因为存在大量无法处理的氧化LDL,而巨噬细胞的活跃功能正是保持血液清洁的关键。因此,可以认为激活巨噬细胞的LPS对预防动脉粥样硬化也有效果。
实际上,在一项让动脉粥样硬化模型小鼠食用高脂肪食物的实验中,给予激活巨噬细胞的LPS的小鼠与未给予的小鼠相比,体重增加受到抑制,大动脉血管斑块的发生也较少(*1)。
LPS可以抑制高脂肪饮食的影响
- 以下为文献详情内容 -
口服LPS通过改善高脂血症、促炎介质和氧化反应,预防高脂饮食喂养的apoe缺陷小鼠动脉粥样硬化的发展
摘要
成团泛菌 (P. 成团的)是一种与各种可食用植物共生的革兰氏阴性细菌,口服或舌下给予来自P. 成团的(LPSp)已被认为有助于预防免疫相关疾病。我们之前的研究表明,口服LPSp在高脂血症志愿者中显示出降低LDL的效果;然而,LPSp对动脉粥样硬化的预防作用尚不清楚。本研究试图评估LPS在高脂饮食(HFD)诱导的动脉粥样硬化小鼠模型中的抗动脉粥样硬化效果。在16周的时间里,apoE缺陷小鼠被喂食HFD,并接受含有LPSp (0.3或1 mg/kg体重/天)的饮用水。结果表明,口服LPSp可减轻体重。即使使用较低剂量的LPSp,也观察到了动脉粥样硬化斑块沉积的显著减少。生化分析表明,LPSp显著改善葡萄糖耐量,降低血浆LDL和氧化LDL水平。此外,LPSp显著减少了包括MCP-1(在血浆中)、TNF-α和IL-6(在结肠中)在内的促炎介质的产生,并降低了外周血样中的氧化爆发活性。综上所述,这些结果表明口服LPSp可以有效改善HFD诱导的高脂血症和炎症/氧化反应,从而预防动脉粥样硬化和相关的代谢紊乱。
引言
众所周知,泛菌糖脂质(LPS)是革兰氏阴性菌外膜的主要成分,是人和动物的强免疫刺激剂。然而,最近的研究表明,在预防各种疾病方面有一些有益的作用。许多流行病学研究证实,在生命早期环境暴露,如农场生活,可降低儿童[1]过敏敏感、哮喘和花粉热的风险。此外,通过静脉注射低剂量LPS预处理可以增强小鼠模型对金黄色葡萄球菌感染的抵抗力,可能通过LPS介导的toll样受体(TLR)4信号通路[2]的表观遗传变化来激活(启动)巨噬细胞。
我们的研究小组一直在研究从可食用植物中获得的巨噬细胞(或免疫细胞)激活化合物和相关的副产物[3–5]的生理效应。我们之前发现,小麦粉水提取物在小鼠体内表现出启动活性,其活性化合物被确定为来源于小麦[6]上的成团泛菌 (P. 成团的)的LPS。P. 成团是一种革兰氏阴性细菌,与各种可食用植物共生生长,如小麦和水稻[7],并且一些菌株已经被用作生物控制剂来预防仁果类水果上的细菌性疾病[8]。体内研究报道,口服或舌下给予纯化自P. 成团的(LPSp)L与一些重要的健康益处相关,包括预防胃溃疡[9]、特应性皮炎[10]和糖尿病[11],以及提高黏膜疫苗对抗流感病毒[12]的效力。LPSp经口服或经皮途径给药时的安全性已通过常见的体内安全性试验和皮肤贴片试验[13]得到证实。
动脉粥样硬化仍然是世界范围内发病率和死亡的主要原因之一,高脂血症被认为是动脉粥样硬化[14]发展的主要危险因素。在动脉粥样硬化的早期,氧化LDL(ox-LDL)的产生和动脉粥样硬化斑块的形成主要是由活化的血管免疫细胞引起的,病原体识别受体(包括TLRs)引起的过度炎症反应;然而,TLR介导的动脉粥样硬化保护作用的发现也已经出现[15]。例如,当口服给予apoE缺陷小鼠时,发现作为TLR4激动剂的热休克蛋白显示出对高脂血症和动脉粥样硬化的预防作用[16]。在我们之前的临床研究中,口服含LPSp的茶可显著降低高脂血症志愿者的空腹血糖和低密度脂蛋白(LDL)胆固醇水平,且无不良反应[17]。此外,口服LPSp在高脂血症兔[18]模型中有效降低血清LDL水平,但尚未有报道描述口服LPSp的抗动脉粥样硬化作用。
因此,本研究的目的是确定口服LPSp是否能预防apoE缺陷小鼠高脂饮食(HFD)诱导的动脉粥样硬化模型中动脉粥样硬化的发展。口服LPSp16周显著减少了胸主动脉中的动脉粥样硬化斑块沉积。此外,LPSp显著改善葡萄糖耐量,降低血浆LDL、氧化LDL水平、促炎介质和外周血样中的氧化爆发活性。我们的研究结果首次证明,当口服给予HFD喂养的apoE缺陷小鼠时,LPSp可以有效地改善高脂血症和炎症/氧化反应,以防止动脉粥样硬化的进展。
结果
一般观察
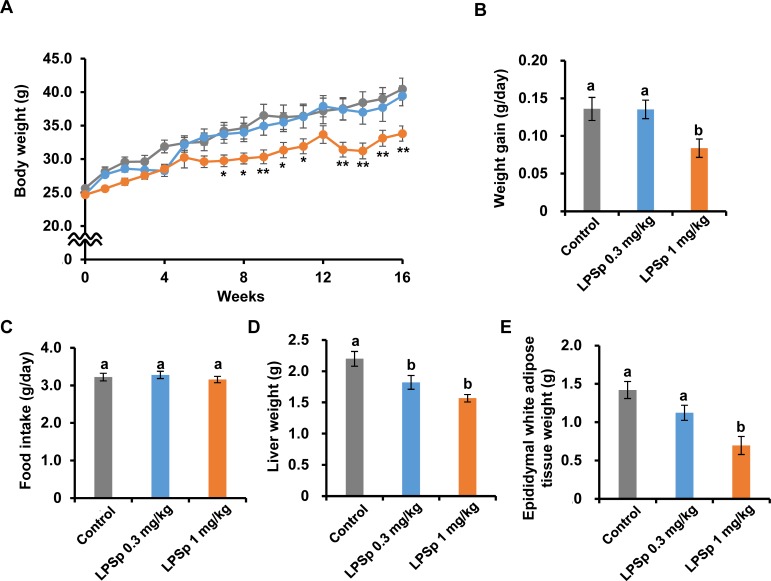
为了研究LPSp对动脉粥样硬化的影响,给apoe缺陷小鼠喂食HFD以诱导动脉粥样硬化的发展,并接受添加纯化LPSp的饮用水16周。根据体重和饮水量,小鼠接受剂量为0.3或1mg/kg BW/天的LPSp。如图1A所示,随着时间的推移,所有小鼠的体重逐渐增加。口服LPSp (1mg/kg BW/天)显著减轻了HFD诱导的体重增加(p < 0.05), 除了第12周 (p= 0.12)。同样,与对照组相比(p < 0.05),lp<处理组(1mg/kgBW/天)的每日体重增加也有所减少(图1B)。在实验期间,实验期间各组间的食物摄取量(图1C和图S3)和初始BW(对照组25.6 ± 0.4 g;LPSp 0.3 mg/kg BW/天24.7 ± 0.3 g;LPSp 1 mg/kgBW/天24.7 ± 0.4 g,n = 8)均无显著差异。与对照组相比,LPSp处理组的肝脏重量较低(LPSp 0.3 mg/kg BW/天:p < 0.05;LPSp 1 mg/kgBW/天:p<0.01)(图1D),而LPSp(1 mg/kgBW/天)处理组的附睾白色脂肪组织明显较低(p<0.05)(图1E)。在实验过程中,没有小鼠死亡,也没有出现,如直肠出血、腹泻或异常行为等不良现象。
图1. 口服LPSp对体重变化、每日体重增加、食物摄入以及肝脏和附睾白色脂肪组织重量的影响。
口服葡萄糖耐量试验、空腹胰岛素和糖化血红蛋白
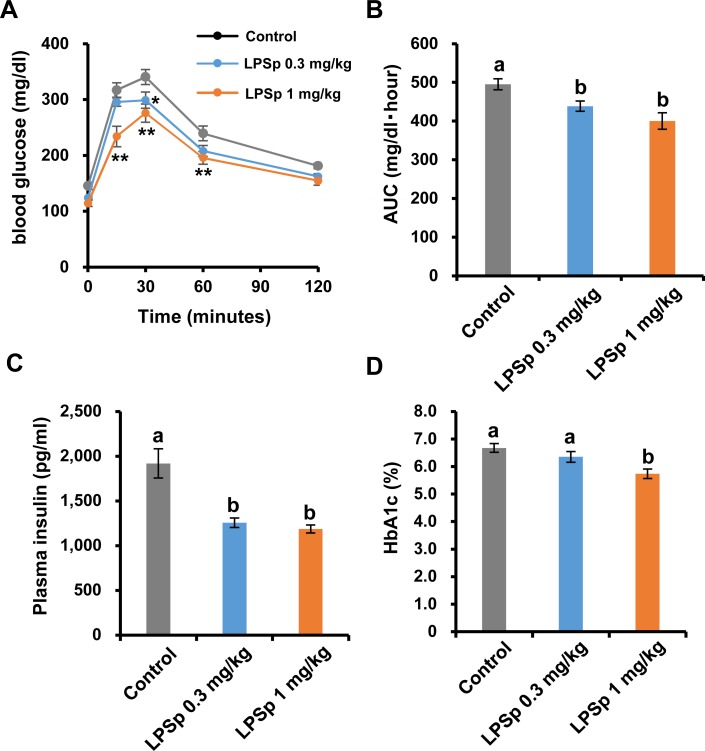
动脉粥样硬化的发展与糖耐量、脂质和脂肪因子谱以及炎症生物标志物[28]的恶化有关。为了评估LPSp对葡萄糖耐量的影响,我们在第16周进行了OGTT检查。如图2A所示,与对照组相比,口服LPSp(1 mg/kg体重/d)在15、30和60 min时对葡萄糖负荷的血糖反应显著降低(p < 0.01)。较低剂量的LPSp(0.3mg/kgBW/d)可导致30 min时血糖显著下降(p < 0.05)。AUC分析显示,与对照组相比,LPSp处理组的血糖均显著降低(LpSp0.3mg/kgBW/天: p < 0.05;LpSp1mg/kgBW/天:p<0.01)(图2B)。治疗后,与对照组相比,LPSp治疗组的空腹血浆胰岛素水平均较低(p<0.01)(图2C),而LPSp(1mg/kgBW/天)治疗组的HbA1c水平也较低(p<0.01)(图2D)。
图2. 口服LPSp对OGTT反应、血浆胰岛素和HbA1c的影响。
胸主动脉动脉粥样硬化病变的定量分析
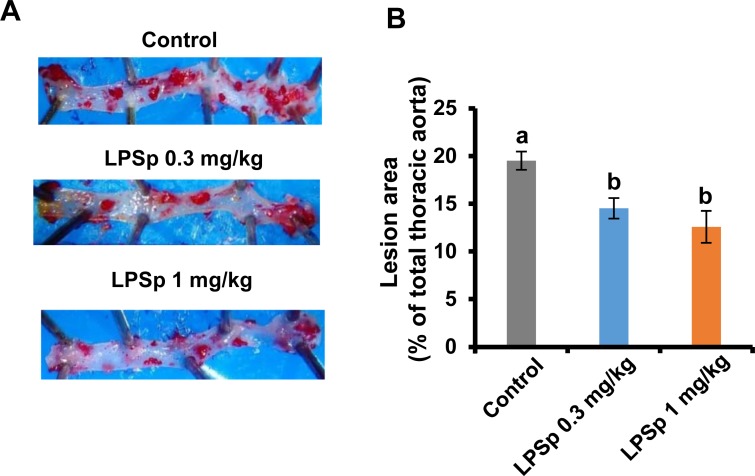
口服LPSp16周后,对胸主动脉的定量分析显示,与对照组相比,LPSp治疗组的油红色O-阳性动脉粥样硬化病变较少(LPSp0.3mg/kgBW/天: p < 0.05;LPSp1mg/kgBW/天:p<0.01)(图3A和3B)。在两组LPSp治疗组之间,斑块面积没有显著的剂量依赖性减少。
图3. 口服LPSp对胸主动脉粥样硬化病变区域的影响。
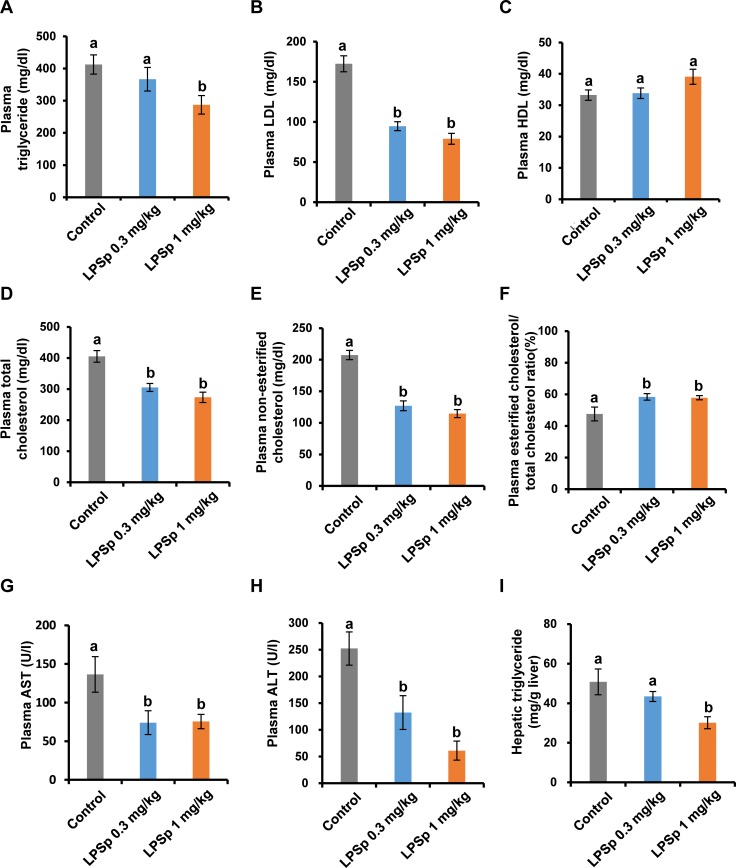
生化参数
如图4所示,用LPSp (1mg/kgBW/天)治疗的小鼠的血浆甘油三酯水平显著降低(p < 0.05,与对照组)(图4A),低密度脂蛋白(p<0.01)(图4B),总胆固醇(p<0.01)(图4D)和非酯化胆固醇(p<0.01)(图4E)和更高水平的酯化/总胆固醇比(p<0.05)(图4F)。与对照组(33.2 ± 1.6 pg/ml)相比,LPSp处理组的血浆HDL水平趋向更高(18%;39.1 ± 2.4 pg/ml),但这一差异没有统计学意义(p=0.10)(图4C)。肝脏在维持正常的脂质代谢和葡萄糖耐量[29]中起着重要作用。HFD诱导的小鼠肝功能损害的特征是血浆AST和ALT活性升高和肝脂质积累[30]。正如预期的那样,血浆AST(图4G)和ALT(图4H)和肝脏甘油三酯显著降低积累量(图4I)(p < 0.01)。在低剂量LPSp组中,LDL(p < 0.01,与对照组相比)、总胆固醇(p < 0.01)、非酯化胆固醇(p < 0.01)、酯化/总胆固醇比值(p < 0.05)、AST(p < 0.05)和ALT(p < 0.05)均有显著差异。综上所述,这些发现表明,口服LPSp可以防止HFD诱导的体重增加和动脉粥样硬化斑块的发展,并改善了糖耐量、血脂谱和肝功能。因此,我们接下来研究了口服LPSp是否能有效调节HFD诱导的炎症反应。
图4. 口服LPSp对血脂谱、AST活性、ALT活性和肝脏甘油三酯积累的影响。
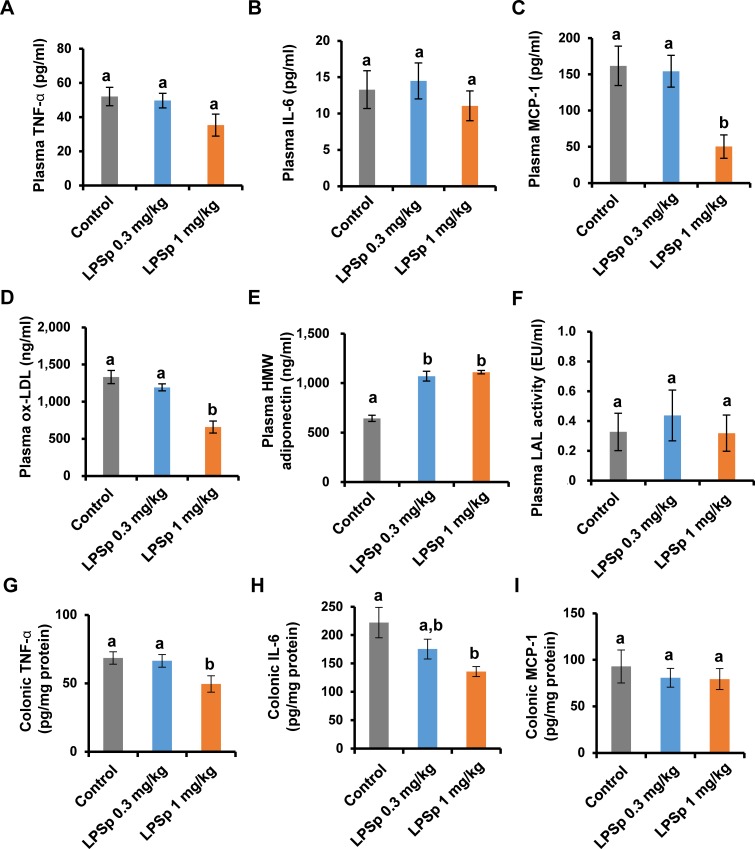
与对照组(52.0 ± 5.4 pg/ml)相比,LPSp治疗组血浆促炎细胞因子TNF-α的表达趋于降低(35.3±6.4 pg/ml),但这种差异不显著(p = 0.11,图5A)。此外,血浆IL-6水平无显著性差异(图5B)。口服LPSp(1mg/kgBW/天)可有效降低血浆水平(p < 0.01),可降低MCP-1水平,MCP-1是单核细胞相关炎症[31]的生物标志物(图5C)。有趣的是,口服LPSp(1mg/kgBW/d)可显著降低了血浆ox-LDL水平(p<0.01)(图5D)。此外,与对照组相比,LPSp处理组的血浆HMW-脂联素水平与糖耐量和炎症[32]呈负相关(p < 0.01)显著相关(图5E)。采用LAL凝血法测定血浆LPS总量。标准曲线采用标准LPS法测定,显示相关系数较高(r2 = 0.986)(S4图和S1 Table)。两组间无显著性差异(图5F)。结肠细胞因子表达分析显示,LPSp处理(1mg/kgBW/天)可有效降低TNF-α和IL-6的表达(p <比对照组为0.05)(图5G和5H)。结肠MCP-1无明显变化(图5I)。
图5. 口服LPSp对炎症细胞因子、趋化因子、ox-LDL、HMW-脂联素和LAL凝血活性的影响。
测定外周血样中超氧阴离子的产生、髓过氧化物酶的活性和吞噬作用
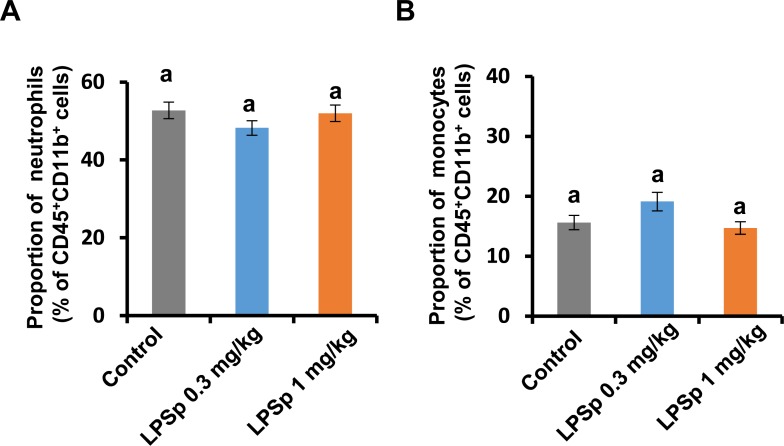
据报道,在apoe缺陷小鼠[33]中,高胆固醇血症或肝功能障碍导致循环白细胞过度氧化活性引发血管炎症的上调。白细胞的细胞氧化反应主要受氧化爆发的调节,包括活性氧(ROS)的产生和MPO介导的氧化反应[34]。为了评估从外周血样本中获得的白细胞部分的氧化爆发活性,采用了由Hamamatsu Photonics K.K.开发的化学发光/荧光实时双监测装置。在这里应用了[23,24]。该装置用于监测PMA后超氧阴离子(O2●-)产生的化学发光强度的变化和MPO反应的荧光强度的变化,每隔0.5秒刺激一次。具有代表性的分析结果如图6A所示。如图6B所示,PMA刺激下的两个LPSp处理组的O2●-产量均较低,与对照组比较(p < 0.01)。同样,pma诱导的MPO活性在LPSp(1mg/kgBW/天)处理组中较低(p<0.05)(图6C)。低剂量LPSp(0.3mg/kgBW/d)有MPO活性降低的趋势(p = 0.12)。此外,氧化爆发活性与吞噬活性密切相关,吞噬活性维持对异种生物[35]的免疫稳态。使用大肠杆菌生物颗粒测定吞噬活性,与对照组相比,LPSp处理组的吞噬活性均显著降低(p<0.05)(图6D)。此外,中性粒细胞(定义为CD45+ CD11b+ Ly-6G+)和单核细胞(CD45+ CD11b+ Ly-6G-Ly-6C+)的比例各组间无显著差异(图7)。
图6. 口服LPSp对外周血样中超氧阴离子产生、MPO活性和吞噬作用的影响。
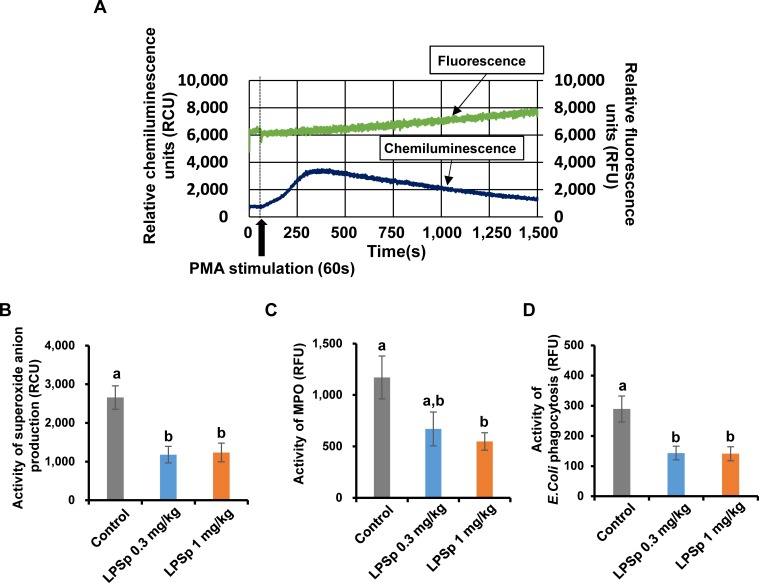
图7. 外周血样本中嗜中性粒细胞和单核细胞的数量。
肠道微生物群谱的分析
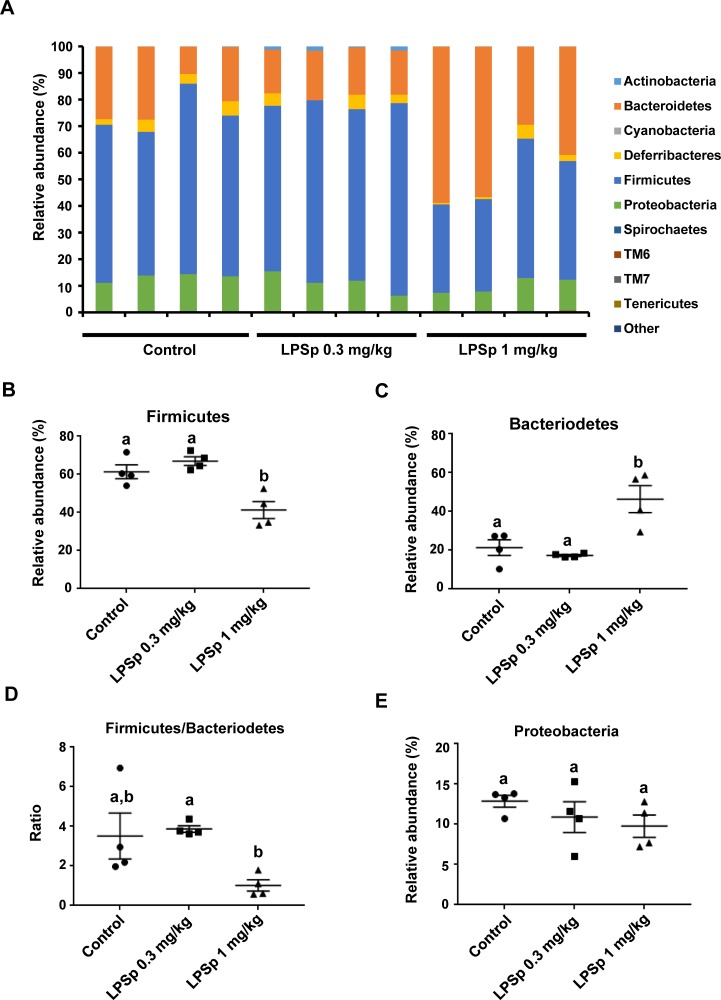
从粪便样本中提取微生物DNA,来分析肠道微生物群组成,然后对其进行Miseq 16S rRNA基因测序。如图8A所示,在门水平上计算了细菌的相对丰度。与对照组相比,口服LPSp(1mg/kgBW/d)可导致厚壁菌门的数量显著减少。(p<0.01)(图8B)和拟杆菌门的增加。(p<0.05)(图8C),并呈现出厚壁菌门与拟杆菌门的丰度比有下降的趋势(p=0.08)(图8D)。在两个LPSp处理组中,高剂量的LPSp(1 mg/kg BW/天)对减少厚壁菌门更有效。(p<0.01vs.LPS0.3mg/kg体重/天组),增加拟杆菌门。(p < 0.05),降低厚壁菌门与拟杆菌门的比率(p < 0.05)。变形菌门的相对丰度在各组间无显著性差异(图8E)。
图8. 口服LPSp对肠道菌群组成的影响。
讨论
补充资料:
S1图
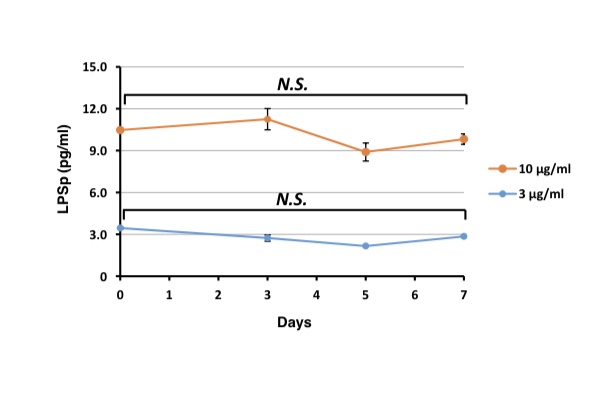
LPSp在饮用水中的稳定性
S2图
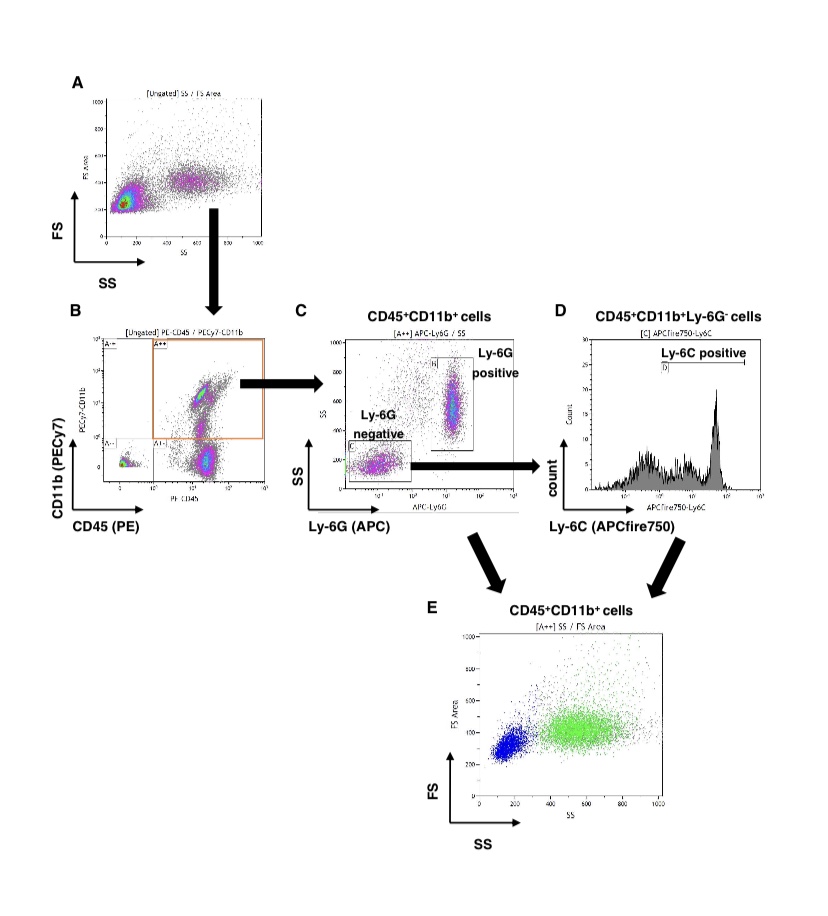
中性粒细胞和单核细胞的门控策略
S3图
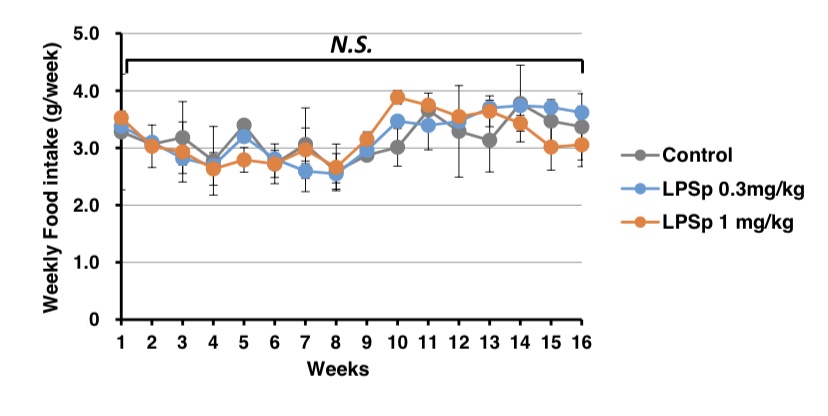
实验期间每周的食物摄入量
S4图
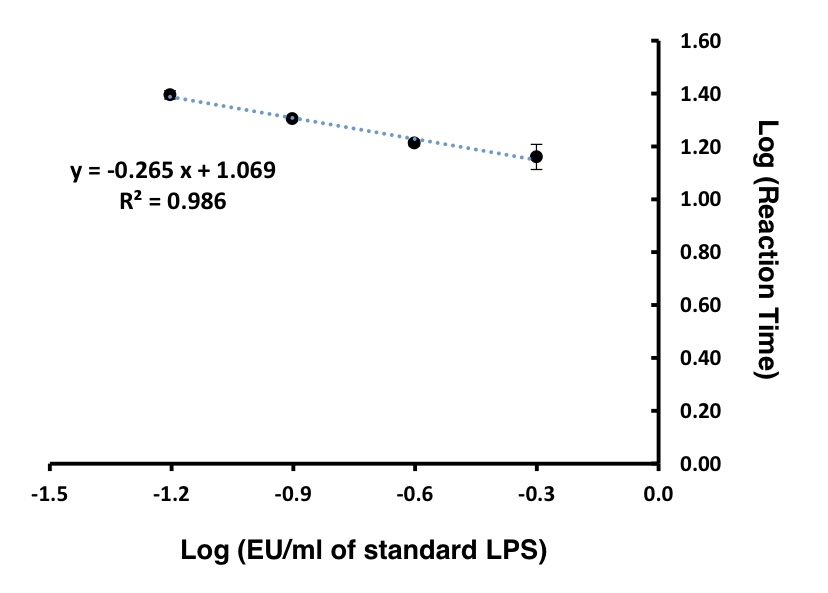
本研究的LAL测定法的标准曲线
S1表
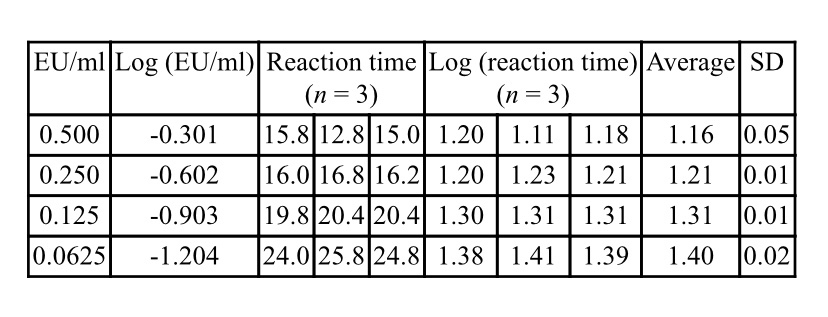
目前的LAL检测方法的标准数据
S2表
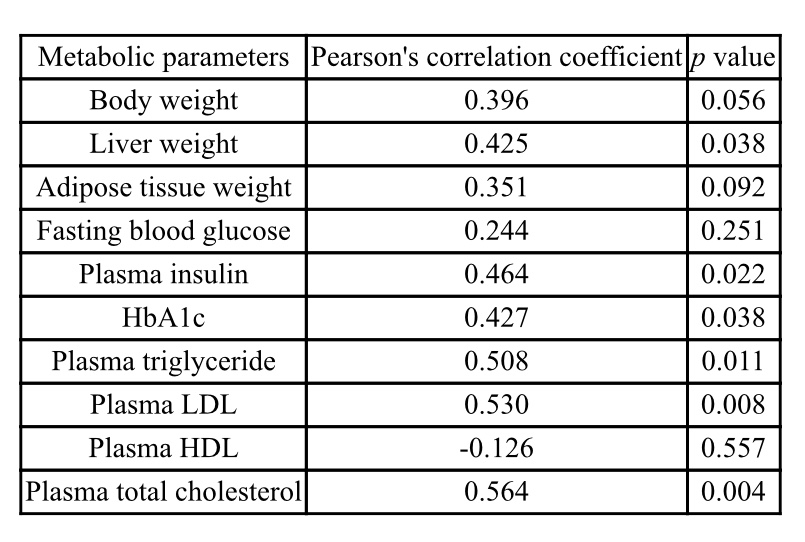
动脉粥样硬化斑块病变与主要代谢参数的比值之间的皮尔逊相关系数
免责声明:
以上部分内容来源于外网我们重在信息分享,版权归属原作者或原刊发平台所有,如有侵权、信息有误或其他异议,请联系我们,我们将在24小时内删除或整改。
复合免疫 健康活力





























