
Vancomycin 耐药肠球菌利用抗生物質诱导的先天免疫缺陷
LPS可以改善与消除共生肠道菌群相关的先天免疫缺陷
注:
本文为中、日、英三种语言,下方附有中文翻译,供您查阅!
抗生物質とLPS
LPSは抗生物質の副作用を低減することが報告されています(*1)。
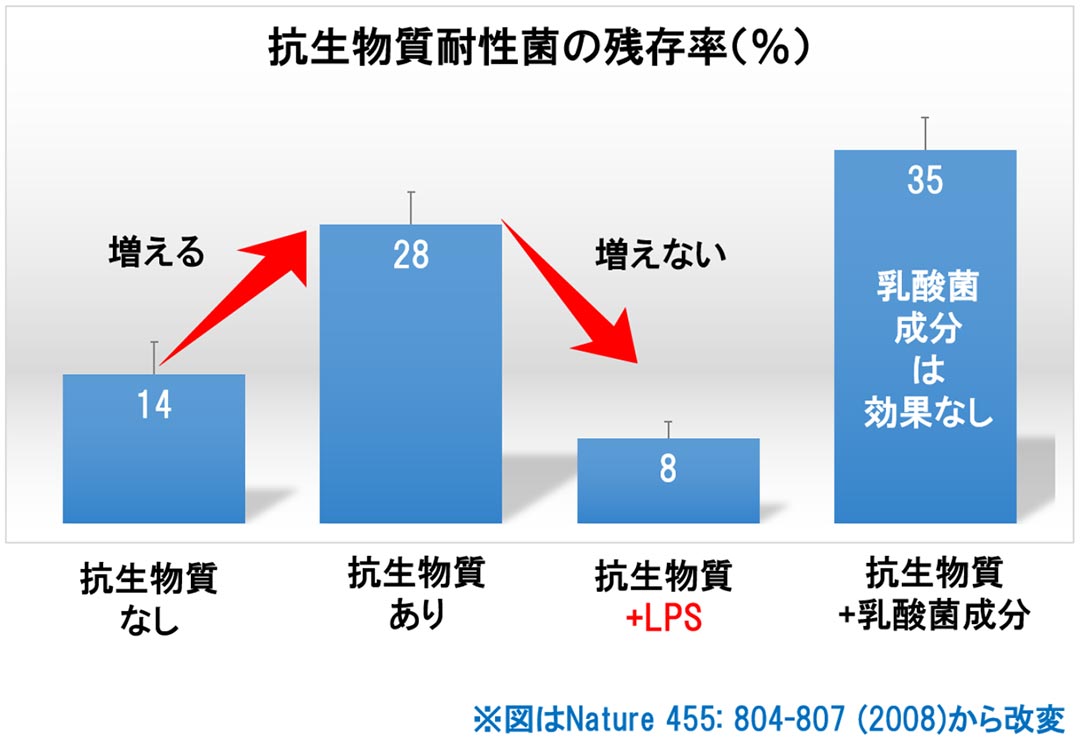
抗生物質は細菌感染症の治療に非常に有用ですが、腸内細菌も殺してしまうというデメリットがあります。抗生物質を飲むと腸の調子がおかしくなる方もあるでしょう。腸内細菌は、色々な面で重要ですが、そのひとつとして生体内抗菌物質を誘導する役割があります。この生体内抗菌物質は抗生物質が効かない耐性菌にも効果がありますが、腸内細菌が死ぬと生体内抗菌物質も少なくなり、抗生物質耐性菌を押さえられなくなるので、耐性菌が増えてきます。ややこしいですが、抗生物質を飲むと、抗生物質に耐性な菌はどんどん増えて、やっかいなことになるのです。ところで、LPSは腸内細菌に代わって、生体内抗菌物質を誘導できます(*1)。興味深いことに、この効果は乳酸菌の成分では得られません。つまりヨーグルトを食べても生体内抗菌物質は誘導できないのです。ですから、抗生物質を飲む際には、どうぞLPSも一緒に摂取してください。
抗生物質を飲むと抗生物質耐性菌が体内で増えるがLPSはそれを抑制する
(*1) vancomycin-resistant entero cocci exploit antibiotic-induced innate immune deficits,Nature 455: 804-807 (2008)
中文翻译:
抗生物質和LPS泛菌糖脂质
据报道,LPS可以降低抗生物質的副作用(*1)。
抗生物質在治疗细菌感染方面非常有效,但缺点是它也会杀死肠道内的有益细菌。有些人在服用抗生物質后可能会出现肠道不适。肠道细菌在很多方面都很重要,其中一个作用就是帮助身体产生内在的抗菌物質。这些内在的抗菌物質对那些抗生物質无法对抗的耐药菌也有效。然而,如果肠道细菌被杀死,内在的抗菌物質的产生会减少,导致无法抑制耐药菌的生长,从而使得耐药菌数量增加。这是一个复杂的问题,因为抗生物質的使用会导致耐药菌的不断增加,从而引发更多的问题。值得注意的是,LPS可以替代肠道细菌,帮助身体产生内在的抗菌物質(*1)。有趣的是,这种效果是乳酸菌成分所不能提供的。也就是说,即使喝酸奶也无法诱导身体产生内在的抗菌物質。因此,在服用抗生物質时,请同时摄取LPS。
服用抗生物質会导致抗生物質耐药菌在体内增加,但LPS会抑制这种情况
- 以下为文献详情内容 -
摘要
感染抗生物質耐药细菌,如Vancomycin耐药肠球菌(VRE),是广谱抗生物質治疗的危险且昂贵的并发症。抗生物質介导的共生菌消除如何促进抗生物質耐药细菌的感染,这是一个充满猜测但机制尚不明确的领域。在这里,我们证明了对小鼠的抗生物質治疗显著下调了肠道RegIIIγ(也称为Reg3g)的表达,这是一种分泌的C型凝集素,能够杀死包括VRE在内的革兰氏阳性细菌。RegIIIγ的下调显著降低了抗生物質治疗小鼠肠道内VRE的体内杀伤作用。通过口服LPS刺激肠道Toll样受体4,可以再重新诱导RegIIIγ,从而增强抗生物質治疗小鼠对VRE的先天免疫抗性。由广谱抗生物質治疗引起的粘膜先天免疫防御受损,可以通过选择性刺激粘膜上皮Toll样受体来纠正,这为减少抗生物質耐药微生物的定植和感染提供了潜在的治疗途径。
由高耐药细菌引起的感染,如耐甲氧西林金黄色葡萄球菌(MRSA)和VRE,对住院患者构成了日益严重的威胁。严重VRE感染的治疗受到有效抗生物質缺乏的限制。VRE定植于胃肠道,系统性血流感染可能是由肠道传播的结果。人们普遍认为,抗生物質治疗通过消除共生菌群,打开肠道生态位并提供更多的营养,从而增强VRE的生存和增殖。然而,最近的研究表明,肠道中的共生微生物可以诱导表达限制细菌生存和生长的蛋白质。因此,尽管共生微生物可能直接限制VRE的增殖,但另一种假设是共生微生物通过激活粘膜先天免疫防御间接抑制VRE。
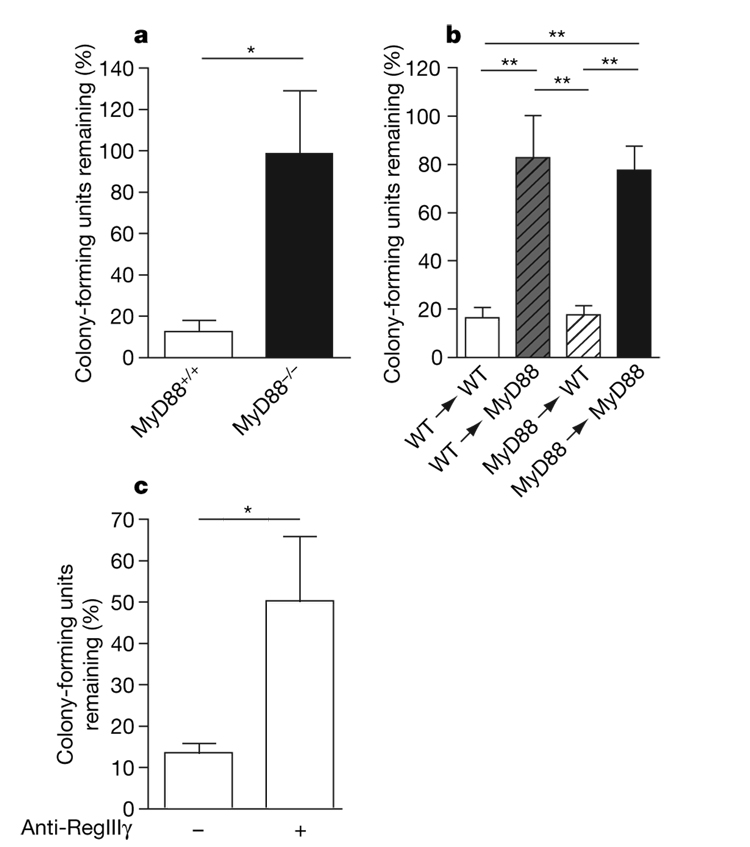
作为第一步,为了确定先天免疫信号通过Toll样受体(TLR)-MyD88途径是否限制了VRE在肠道内的定植,我们比较了野生型和MyD88缺陷型小鼠的回肠环中VRE的杀伤情况。图1a显示,在野生型小鼠的回肠环中,VRE的杀伤效果远比MyD88缺陷型小鼠更有效。在骨髓源性细胞中,VRE的肠道抑制不需要myd88介导的信号,而在非骨髓源性细胞中则需要,可能是上皮细胞(图1b)。RegIIIγ是一种分泌的凝集素,对肠上皮细胞和Paneth细胞表达的革兰氏阳性细菌具有较强的杀菌活性。RegIIIγ的表达依赖于肠上皮细胞中tlr-myd88介导的信号,并由共生微生物诱导。为了确定RegIIIγ是否介导了肠道内VRE的体内杀伤,我们在接种VRE之前,向野生型小鼠的回肠环中注射了针对RegIIIγ的阻断性多克隆抗血清。在用RegIIIγ特异性抗血清处理的肠道中,存活的VRE细菌数量增加了400%以上(图1c),表明RegIIIγ介导了体内VRE的杀伤。
对VRE具有抗性的广谱抗生物質组合的给药,显著增加了小肠、盲肠和结肠中VRE的定植(图2a和补充图1),这证实了先前发表的研究。然而,目前尚不清楚为什么消除小肠中相对稀少的微生物群会使得VRE的数量增加100-1000倍以上。由于VRE通过口服途径获得,并通过小肠在系统性传播之前,我们确定了抗生物質给药对野生型小鼠和用MNV处理1、3和7天的小鼠远端回肠中RegIIIγ信使RNA和蛋白水平的影响。RegIIIγ信使RNA水平在抗生物質给药后1天内下降,并在接下来的7天内持续下降,而RegIIIγ蛋白表达在抗生物質开始后的3天内显著减少(图2b,c)。另一种由恩诺沙星和克林霉素组成的抗生物質方案,与MNV一样,消除了革兰氏阳性、革兰氏阴性和厌氧共生细菌,同样减少了RegIIIγ mRNA和蛋白表达(图2d,e)。相比之下,其他抗菌防御介质——隐花蛋白和血管生成素-4并没有被抗生物質给药显著下调(补充图2)。
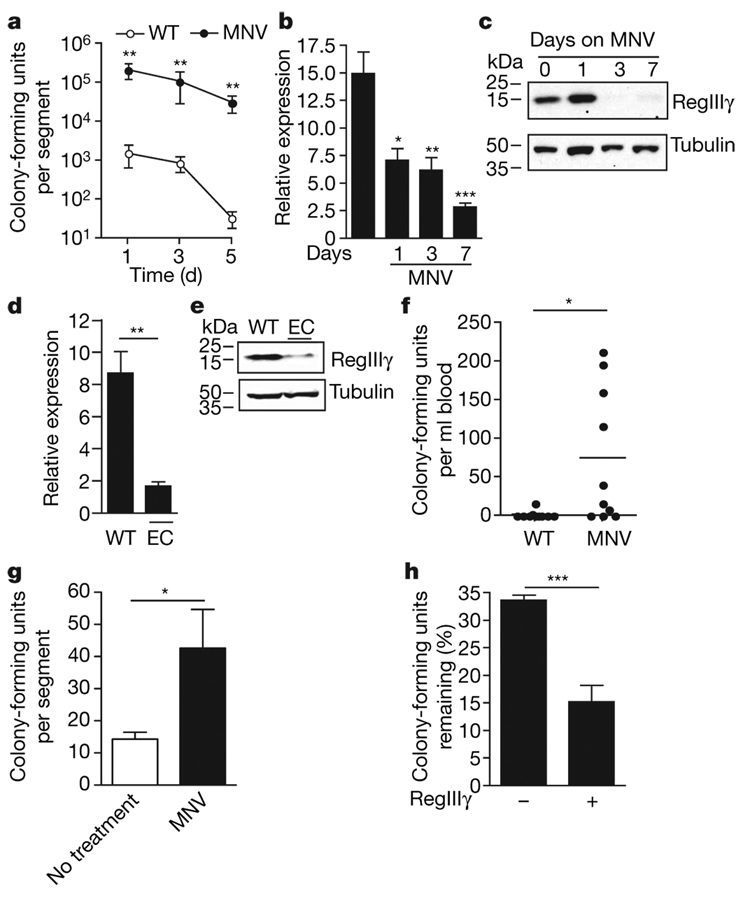
为了确定RegIIIγ水平的降低是否与对VRE的易感性增加相关,接受MNV的野生型小鼠被口服感染VRE,并在24小时后确定其在血液中的传播。在未处理的小鼠中,VRE菌血症不常见,但在大多数接受抗生物質治疗的小鼠血液中培养出了活的VRE(图2f)。此外,体内腔道杀伤实验显示,抗生物質治疗的小鼠在远端小肠中VRE的失活显著受损(图2g)。为了确定在抗生物質治疗的小鼠肠道中重建RegIIIγ是否能够纠正VRE杀伤的缺陷,我们在VRE接种前将重组RegIIIγ注入抗生物質治疗的小鼠的回肠环中,并测量了细菌杀伤情况。RegIIIγ的给药显著减少了抗生物質治疗的小鼠肠道中VRE的生存(图2h),证明了外源性RegIIIγ补充了广谱抗生物質治疗引起的先天免疫缺陷。
RegIIIγ在小鼠小肠中由革兰氏阴性共生细菌种类Bacteroides thetaiotaomicron诱导。相比之下,RegIIIγ的表达被革兰氏阳性的益生菌Bifidobacterium longum下调。为了确定与革兰氏阴性或革兰氏阳性细菌相关的TLR配体是否能在抗生物質治疗的小鼠中诱导RegIIIγ,我们在抗生物質治疗的小鼠的饮用水中添加了LPS或脂磷壁酸(LTA)。对远端回肠中RegIIIγ蛋白水平的定量分析显示,口服LPS治疗后显著上调(图3b和补充图3),对RegIIIγ mRNA的分析显示了一个类似的趋势,尽管这个趋势在统计学上并不显著(图3a)。相比之下,对MNV处理的小鼠进行口服LTA处理并没有增加RegIIIγ mRNA或蛋白的表达(图3a,b和补充图3)。
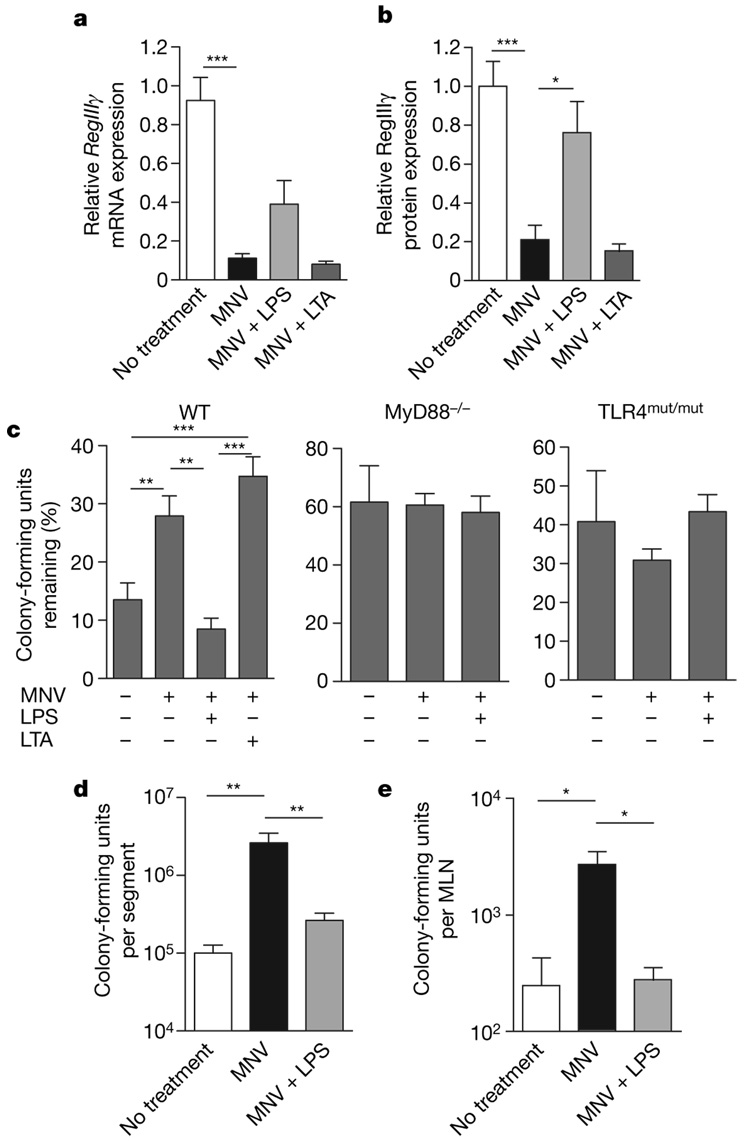
为了确定LPS诱导的RegIIIγ恢复是否纠正了抗生物質治疗小鼠肠道中的VRE清除缺陷,我们对接受MNV的小鼠、同时接受MNV和LPS或LTA的小鼠以及未接受治疗的小鼠进行了管腔杀伤试验。仅接受抗生物質的小鼠小肠VRE清除缺陷,而接受抗生物質和LPS的小鼠肠环清除VRE与野生型未治疗小鼠的回肠环一样有效(图3c)。相比之下,接受LTA的抗生物質治疗小鼠对VRE的管腔杀伤作用没有增强(图3c)。用MyD88-或tlr4突变小鼠研究了lps介导的拯救的特异性和tlr4-myd88依赖性。给myd88缺陷的小鼠使用抗生物質并没有增加VRE在回肠腔内的存活率,而使用LPS也没有增加VRE的杀伤率(图3c)。LPS给TLR4突变小鼠也没有增加肠腔内VRE的杀伤,说明野生型小鼠的LPS效应是tlr4介导的,LPS没有直接抑制VRE的存活(图3c和补充图4)。与未接受抗生物質治疗的小鼠相比,接受抗生物質治疗的小鼠在口服感染24小时后远端小肠和肠系膜淋巴结的VRE数量显著更高,而在tlr4突变小鼠中没有发现LPS的影响(补充图5a,b)。LPS治疗使小肠和肠系膜淋巴结(MLNs)中的VRE结肠形成单位降低到在野生型小鼠中观察到的水平(图3d,e),表明LPS介导的先天免疫防御增强降低了VRE的定植和传播。为了排除口服LPS治疗期间对全身LPS的影响,我们测定了使用抗生物質或抗生物質加LPS治疗7天的小鼠的血清肿瘤坏死因子(TNF)水平。两组小鼠均未检测到TNF,而腹腔注射LPS的小鼠血清TNF水平升高(补充图6)。为了确定经LPS处理的小鼠是否摄入了等量的抗生物質,我们测定了接受或不接受LPS处理的小鼠结肠中的万古霉素水平。两组间无显著性差异,说明使用LPS治疗并没有减少饮用水中抗生物質的摄入量(补充图7)。
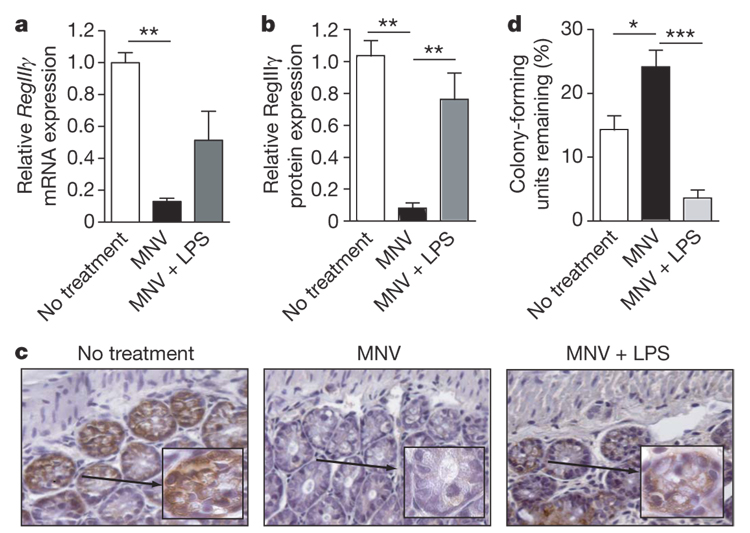
尽管之前的实验表明,在抗生物質治疗的同时使用LPS可以改善与消除共生肠道菌群相关的先天免疫缺陷,但在临床情况下,在已经使用抗生物質后,增强耐药性可能很重要。因此,接受抗生物質治疗4天的小鼠接受口服LPS治疗。在抗生物質治疗4天后,LPS治疗小鼠的RegIIIγ蛋白水平显著上调,RegIIIγ mRNA水平也显著升高,但没有达到统计学意义(图4b和补充图8)。免疫组化结果显示,野生型小鼠远端小肠的Paneth细胞和上皮细胞中RegIIIγ蛋白表达,而经抗生物質处理的小鼠中RegIIIγ蛋白缺失。相比之下,在免疫组化分析中,用LPS和抗生物質处理的小鼠易于表达大量的RegIIIγ(图4c)。根据这些数据,在接受LPS以挽救先天免疫防御的小鼠中,VRE的腔内杀伤也显著增强(图4d)。
我们的研究结果表明,广谱抗生物質通过消除共生微生物,损害肠道先天免疫防御,从而减少肠道黏膜中抗菌分子的表达。受损的肠道先天免疫防御增加了对抗生物質耐药微生物的敏感性,包括革兰氏阳性细菌病原体VRE。我们的实验表明,先天免疫效应分子RegIIIγ通过杀死小肠腔内的细菌,在宿主防御VRE中发挥了重要作用。然而,其他myd88诱导的因子可能也抑制了VRE的肠道定植,因为myd88缺陷小鼠的抑制效果较差,VRE生长比野生型小鼠用RegIIIγ抗血清处理。同样,给经抗生物質治疗的小鼠口服LPS,同时诱导RegIIIγ,也可能通过诱导其他抗菌因子来增加肠道对VRE定植的耐药性。
用广谱抗生物質改变肠道共生菌群的复杂性,为其他无害的微生物引起系统性疾病提供了机会。特异性的TLR信号可以替代共生微生物诱导的信号,恢复RegIIIγ,从而增强对VRE的防御。有趣的是,革兰氏阴性细菌外膜的主要成分LPS诱导RegIIIγ,RegIIIγ通过结合表面暴露的肽-聚糖,选择性地对抗革兰氏阳性细菌。相比之下,LTA,革兰氏阳性细菌的主要表面糖脂,不能诱导RegIIIγ,也不能增强VRE的清除。因此,我们的结果,支持先前的发现,表明一种共生的革兰氏阴性菌,而不是一种益生菌革兰氏阳性菌,诱导了RegIIIγ,这表明,属于不同类别的细菌可以通过在哺乳动物黏膜中诱导先天抗菌机制来相互对抗,从而选择性地使不同类别的细菌失活。
尽管经常考虑使用TLR(Toll样受体)配体进行治疗,但由于诱导炎症细胞因子的复杂性,这种治疗方式可能会带来极端情况下导致败血性休克和死亡的风险。这种严重后果是在全身性给予某些TLR配体后发生的,因此极大地限制了对这种治疗方式的热情。相比之下,胃肠道经常暴露于TLR配体。因此,尽管全身性TLR配体治疗存在困难,但在某些临床情况下,以增强先天免疫防御为目的,向粘膜表面给予TLR配体可能提供有益的效果。
尽管人们认为共生微生物的耗竭直接为病原体提供了空间和营养,但我们的发现表明,广谱抗生物質可能通过损害粘膜先天免疫防御,为病原体提供了更重要的间接优势。例如,通过口服LPS特异性诱导抗菌分子RegIIIγ,因此在接受了广谱抗生物質治疗的患者中可能具有潜在的治疗用途。
免责声明
以上部分内容来源于外网我们重在信息分享,版权归属原作者或原刊发平台所有,如有侵权、信息有误或其他异议,请联系我们,我们将在24小时内删除或整改。
复合免疫 健康活力





























