
细菌与LPS泛菌糖脂质的相关知识
革兰氏阴性菌与LPS泛菌糖脂质
注:本文为中日文双语,下方附有中文翻译,可供查阅!
1、グラム陰性細菌とLPS
LPSは、細菌成分ではありますが、細菌の病原性とは関係がありません。
すべての細菌は、グラム陰性菌とグラム陽性菌の2系統に分類されます。この2系統は、デンマークの学者であるハンス・グラム先生が開発した細菌の染色法で染まるか染まらないかによって区別するので、グラム陽性細菌、グラム陰性細菌と呼ばれています。グラム染色で染まるか染まらないかは細胞壁の構造によって違い、その構造の違いは2系統の菌の違いを明確に示すものなのです。
さて、LPSはグラム陰性細菌だけに存在しています。グラム陰性細菌の中には、有用な菌も病原性の菌も含まれます。グラム陰性細菌のうち、有用な菌としては酢酸発酵に使われる酢酸菌、テキーラの醗酵に使われているザイモモナス菌、食品増粘多糖であるキサンタンガムを産生するキサントモナス菌、食用植物に共生しカビの繁殖を抑えるパントエア菌などがあります。一方、病原菌としてはコレラ菌、サルモネラ菌などがそうです。冒頭に述べたように、病原性の有無はLPSとは関係ありません。例えばサルモネラ菌のLPSだけを取り出して食べたとしても、食中毒にはならないのです。
尚、グラム陽性細菌にも、有用な菌と病原性の菌がいます。有用な菌の代表株が乳酸菌。病原性の菌としては黄色ブドウ球菌、結核菌などがそうです。
中文翻译:
革兰氏阴性菌与LPS泛菌糖脂质
LPS虽然是细菌成分,但与细菌的致病性无关。
所有细菌分为革兰氏阴性菌和革兰氏阳性菌两大系统。这两个系统是根据丹麦学者汉斯·克医生开发的细菌染色法是否染色来区分的,所以被称为革兰氏阳性细菌、革兰氏阴性细菌。革兰氏染色是否染色根据细胞壁的结构而不同,该结构的不同明确地表明了两个系统的菌的不同。
细菌分类
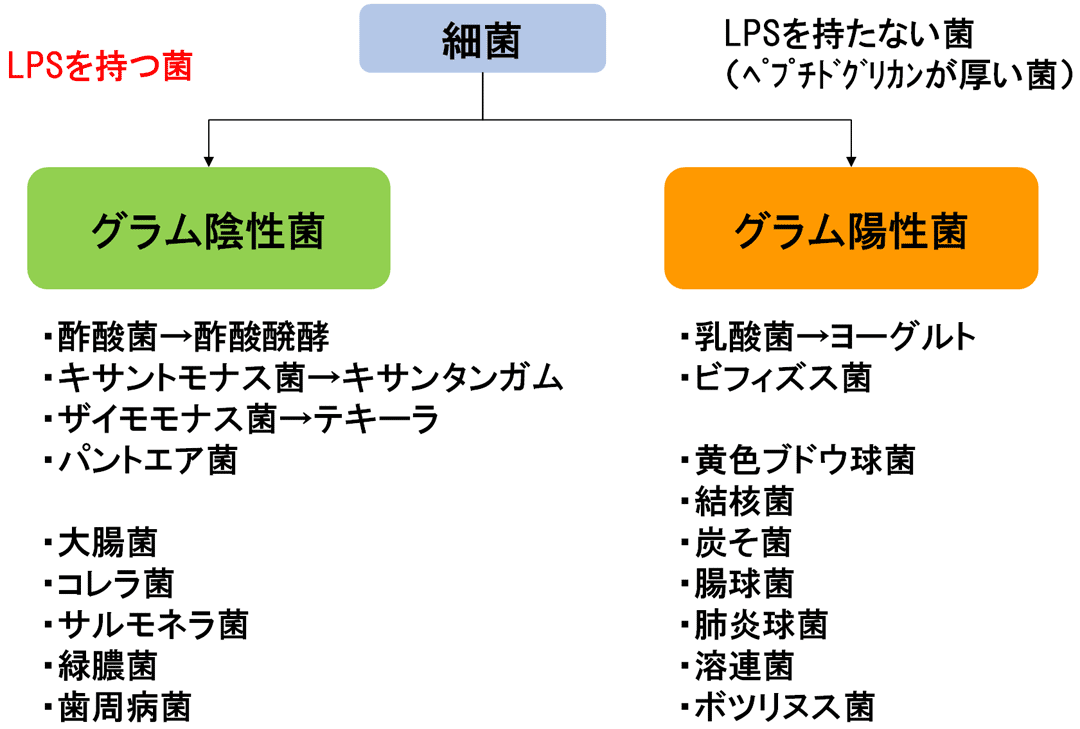
目前,LPS仅存在于革兰氏阴性菌中。革兰氏阴性菌包括有益菌和致病菌。在革兰氏阴性细菌中,有用的细菌包括用于醋酸发酵的醋杆菌属细菌、用于龙舌兰酒发酵的发酵单胞菌属细菌、产生黄原胶(一种食品增稠多糖)的黄单胞菌属细菌以及与食用植物共生的真菌以及泛菌属细菌。抑制繁殖。另一方面,致病菌包括霍乱弧菌和沙门氏菌。正如开头所说,致病性的有无与LPS无关。例如,即使取出沙门氏菌LPS并食用,也不会发生食物中毒。
此外,革兰氏阳性菌包括有益菌和致病菌。有用细菌的代表性菌株是乳酸菌。致病菌包括金黄色葡萄球菌和结核杆菌。
2、歯周病菌のLPS
ポルフィロモナス・ジンジバリス(Porphyromonas gingivalis)を代表とする歯周病菌は、グラム陰性細菌なので、細胞表面にLPSを持っています。よく、歯周病はLPSが原因で起こる、あるいは歯磨きでLPSを除去すれば歯周病が良くなるかのように言われることがありますが、これは間違いです。先に述べたように、LPSにはエンドトキシンのイメージが根強くあることと、歯周病菌がLPSを持つことが結び付けられて、このように言われるものと思います。しかし、歯周病菌のLPSは、ほかのグラム陰性細菌のLPSとは構造が異なっており、LPSのレセプターであるTLR4への結合力が非常に弱いので、サイトカインの誘導能もほとんどありません。歯周病菌で見られる炎症に係る生物活性は、夾雑しているリポタンパク質がTLR2に結合することで起こっていることも明らかになっています(*1,2)。歯周病の本質的な問題は、歯周病菌のLPSにあるのではなく、歯周病菌が排除されずに分裂増殖と溶菌を繰り返しつつ、生きて活動していることそのものにあります。
中文翻译:
牙周病菌与LPS泛菌糖脂质
以牙龈卟啉单胞菌为代表的牙周细菌是革兰氏阴性菌,因此其细胞表面含有脂多糖。人们常说牙周病是由脂多糖引起的,或者说通过刷牙去除脂多糖,牙周病就会好转,但这是不正确的。正如前面提到的,我认为这是因为LPS具有根深蒂固的内毒素形象,而且牙周病细菌也含有LPS。然而,牙周细菌的脂多糖与其他革兰氏阴性菌的结构不同,其与脂多糖受体TLR4的结合强度很弱,因此几乎没有诱导细胞因子的能力。研究还表明,牙周病细菌中与炎症相关的生物活性是由污染性脂蛋白与 TLR2 的结合引起的 (*1,2)。牙周病的本质问题不在于牙周病菌的脂多糖,而在于牙周病菌是活的、活跃的,反复分裂、增殖、溶菌而不被消灭。
牙周病细菌的LPS比较特殊
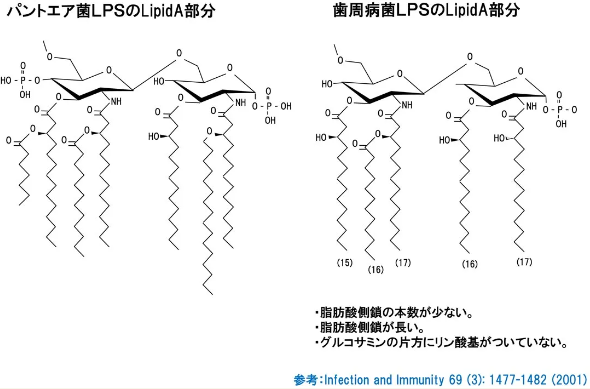
参考文献:
(*1)Signaling by toll-like receptor 2 and 4 agonists results in differential gene expression in murine macrophages, Infection and Immunity 69 (3): 1477-1482 (2001)
(*2)Bacteroides類縁菌LPSの化学構造と免疫生物学的活性━Porphyromonas gingivalis LPS研究を中心に━, 日本細菌学雑誌61 (4): 391-404 (2006)
3、インフルエンザウイルスとLPSの相互作用
LPSは、インフルエンザAウイルスに物理的に結合し、ウイルスを不活化することがわかっています。(*1)
共生細菌が宿主の免疫系と相互作用して、ウイルスを排除していることが以前から報告されていました(*2)。擬人的な表現になりますが、宿主の健康を脅かすウイルス感染は、宿主と生死を共にしている腸内細菌等にとって、有難くない侵入者なので、宿主と協力して戦うというわけです。しかし、共生細菌がウイルスに直接作用するかどうかはわかっていませんでした。
これについて、Bandoroらは、腸内細菌がインフルエンザAウイルスの安定性を大幅に低下させるということを報告しました。さらに、その効果は、生きた細菌でなくても、グラム陰性細菌由来のLPSで得られることがわかったのです(*1)。
LPSがインフルエンザウイルスを不活化する効果は、37℃以上で顕著になります。これは温度が高くなることによって、LPS結合部位が露出されるようにウイルスの構造が変わるからではないかと著者らは言っています。この論文では、LPSとインフルエンザH1N1 PR8ウイルスを37℃でインキュベートすると、ウイルスの形態が顕著に変わることが示されています。
著者らは、本知見が呼吸器系感染の予防や治療の開発につながるのではないかとし、また家禽や豚養殖で抗生物質を使いすぎることは、抗生物質耐性菌を増やすだけでなく、ウイルス感染のリスクをも上げると警鐘をならしています。
中文翻译:
流感病毒与LPS泛菌糖脂质的相互作用
LPS 已被证明可以与甲型流感病毒物理结合并使其失活。(*1)
此前已有报道称,共生细菌与宿主的免疫系统相互作用以消除病毒(*2)。这听起来可能很拟人化,但威胁宿主健康的病毒感染却是与宿主同生共死的肠道细菌不欢迎的入侵者,因此它们会与宿主合作对抗。然而,尚不清楚共生细菌是否直接与病毒相互作用。
对此,Bandoro 等人报道,肠道细菌显着降低了甲型流感病毒的稳定性。此外,还发现即使来自革兰氏阴性菌的LPS不是活菌,也能获得这种效果(*1)。
当温度高于 37°C 时,LPS 对流感病毒的灭活作用变得明显。作者说,这可能是因为较高的温度导致病毒改变其结构,暴露 LPS 结合位点。本文表明,在 37°C 下用 LPS 孵育 H1N1 PR8 流感病毒会显著改变病毒的形态。
LPS与病毒外膜结合使其变形
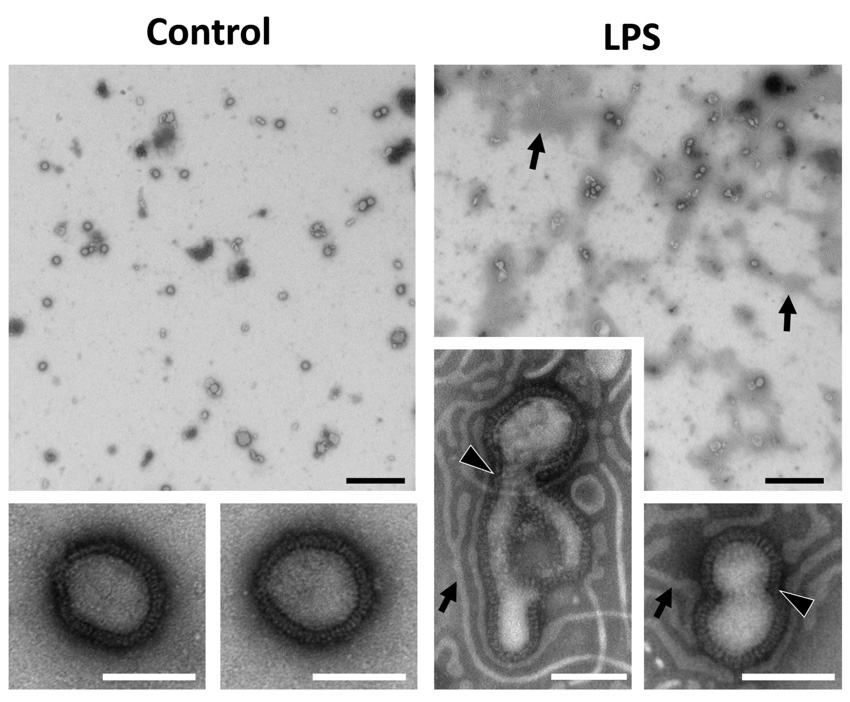
H1N1 PR8 与水(对照)或 LPS 在 37°C 下孵育 1 小时后的透射电子显微照片。以 4,800 和 49,000 放大倍率拍摄。黑色箭头表示LPS,白框包围的黑色箭头表示病毒外膜。黑条:1 mm,白条:100 nm。
作者们提到,这些知识可能与预防和开发呼吸系统感染的治疗方法有关,并且警告说,在家禽和猪的养殖中过度使用抗生素不仅会增加抗生素耐药性细菌,还会增加病毒感染的风险。
参考文献:
( *1) bacterial lipopolysaccharide de stabilizes influenza viruses American Society for Microbiology,September/October 2017 volume2issue 5e 00267-17 ( 2017 )
https://MSP here.ASM.org/content/2/5/e 00267-17
( *2) trans kingdom control of micro biota diurnal oscillations promotes metabolic homeostasis cell,159:514–529 ( 2014 )
4、傷口とLPS
LPSは口から入っても、皮膚に付いても毒性はありません。むしろ自然免疫の活性化に貢献しています。しかし、血液中に注射すると量によっては強い炎症がおこります。では胃腸や皮膚に傷口があった場合はどうでしょうか。傷口から血液中に入って、炎症が起こることがあるのでしょうか。
結論から言うと、遊離のLPSが傷口周辺にあるとして、炎症を誘導するほどの生物活性を保ったまま、傷口から血液中に移行することはとても難しいです。
「LPSの構造と機能」の項で述べたように、LPSはグラム陰性細菌の細胞壁に埋まっている成分で、糖と脂質でできています。体の中には、脂肪もあれば、脂質と結合するタンパク質(代表的な例としては、コレステロールを運ぶLDLなど)も存在します。LPSの活性中心でもある脂質部分は、脂肪やLDLにトラップされ、かつ不活性な状態になります。このことは、血液にLPSを混ぜた後、LPSの量を測定しようとしてもうまく検出できないことでもわかります(*1)。当然ながら強い生物活性もありません。
LPSが血液あるいは臓器に運ばれるためには、生きたグラム陰性細菌の介在が必要です。生きた菌が体内に侵入し、増えて、溶菌したときに、(脂質結合タンパク質では抑制できないぐらい)多量のLPSが、生物活性を保った状態で放出されます。生きた細菌がいない限り、例え傷口周辺にLPSが存在しても、それが炎症の原因になることはまずないといって良いでしょう。
中文翻译:
伤口与LPS泛菌糖脂质
LPS 口服或接触皮肤均无毒。相反,它有助于激活先天免疫。然而,如果注射到血液中,根据量的不同,可能会发生严重的炎症。但如果胃、肠或皮肤有伤口怎么办?它会通过伤口进入血液并引起炎症吗?
总之,即使伤口周围存在游离LPS泛菌糖脂质,它也很难从伤口迁移到血液中,同时保留足够的生物活性来诱发炎症。
正如“LPS的结构和功能”部分提到的,LPS是埋藏在革兰氏阴性菌细胞壁中的成分,由糖和脂质组成。体内既有脂肪,也有与脂肪结合的蛋白质(典型的例子是低密度脂蛋白,它携带胆固醇)。脂质部分也是LPS的活性中心,被脂肪和LDL困住而变得不活跃。这一点可以从以下事实看出:即使将 LPS 与血液混合后尝试测量其量,也无法正确检测(*1)。当然,它也没有很强的生物活性。
将 LPS 输送到血液或器官需要存在活的革兰氏阴性细菌。当活细菌侵入体内、繁殖并裂解时,会释放大量LPS(不能被脂质结合蛋白抑制),同时仍保留其生物活性。只要没有活细菌,即使伤口周围存在LPS,也不太可能引起炎症。
参考文献:
( *1) Endotoxemia—menace,marker,or mistake?J Leukoc Biol.100(4):687–698 ( 2016 )
复合免疫 健康活力





























