
肥胖与LPS泛菌糖脂质
注:本文为中日文双语,文中附有中文翻译,可供查阅!
1、<肥満とLPS>
LPSの経口摂取が肥満の原因になることはありません。OECD基準で行った、ラットを使ったLPSの90日間の継続経口摂取試験によると、1日に体重1kgあたり45mgまで与えても、対照動物と体重に違いはなく、また臓器内に異常がないことが確認されています(*1)。
2007年、「Metabolic endotoxemia initiates obesity and insulin resistance」という論文が発表されました(*2)。この論文を引用し、不用意に「LPSが肥満の原因になる」としている本もありますが、食品や環境や腸内に存在するLPSがそのまま肥満の原因になるかのような誤解を招くので、引用するのであれば、正しく丁寧に解説してほしいものです。この論文は、マウスに高脂肪食を与えると、血清中のLPS濃度がやや高くなること。またLPSを人為的に注射する(具体的には、LPSを継続的にポンプで送り出して注射する装置を皮内に埋め込んでおく)と、高脂肪食を食べたときと類似した体重増加傾向と炎症パターンがみられることを示した論文です。決して、食品や呼吸から自然摂取するLPSで肥満が起こるとした内容ではありません。この論文の結果は、2019年現在では、高脂肪食によるリーキーガット(「リーキーガットとLPS」参照)で説明がつきます。すなわち、高脂肪食を摂取する→腸内細菌バランスが崩れる→腸管バリア機能が破たんする→腸内の腸内細菌及びLPSが体内に移行する→体内で炎症が起こる、という現象です。本論文は、現在であれば、肥満の研究というよりは、リーキーガットの研究と言えるでしょう。
尚、2018年には、マウスに高脂肪食を与える実験系において、LPSの経口投与によって、動脈硬化やアミロイドβ蓄積抑制とともに、体重増加が抑制される論文が発表されています(*3, *4)。
以下、肥満に関する最近の知見について興味のある方はお読みください。
中文翻译:
肥胖与LPS泛菌糖脂质:
口服LPS泛菌糖脂质不会导致肥胖。根据OECD标准对大鼠进行的90天连续口服LPS泛菌糖脂质研究显示,即使每天每公斤体重摄入45毫克,与对照动物的体重没有差异,器官也没有异常。这已得到证实(*1)。
2007年,发表了题为“代谢性内毒素血症引发肥胖和胰岛素抵抗”的论文(*2)。
有些书无意中引用这篇论文,认为“LPS是肥胖的原因”,但食品、环境、肠内存在的LPS会直接导致肥胖,引起误解,如果要引用的话,希望能正确且仔细地解说。 这篇论文表明,当给小鼠喂食高脂肪饮食时,其血清中的 LPS 浓度略有增加。
此外,人工注射LPS泛菌糖脂质(具体来说,植入一个连续泵入LPS泛菌糖脂质并将其注射到皮肤中)会导致体重增加,类似于食用高脂肪饮食时出现的情况。 这篇论文表明,存在炎症。这并不是说通过食物或呼吸自然摄入的LPS泛菌糖脂质会导致肥胖。
截至2019年,这篇论文的结果可以用高脂肪饮食引起的肠漏来解释(参见“肠漏和LPS泛菌糖脂质”)。也就是说,其现象是摄入高脂肪饮食→肠道细菌的平衡被破坏→肠道屏障功能被破坏→肠道内的肠道细菌和LPS转移到体内→体内发生炎症。目前这篇论文可以说是肠漏的研究而不是肥胖的研究。
此外,2018年发表了一篇论文,其中在给小鼠喂食高脂肪饮食的实验系统中,口服LPS泛菌糖脂质可抑制动脉硬化和β-淀粉样蛋白积累以及体重增加(*3、*4)。
如果您对肥胖的最新发现感兴趣,请阅读以下内容。
2、<肥満の定義>
世界保健機構(World Health Organization:WHO)によれば、過体重および肥満は、健康を損なう可能性のある異常または過剰な脂肪蓄積として定義されます(*5)。指標としては以下のとおりです。
・過体重:BMIが25以上
・肥満:BMIが30以上
※BMI(Body Mass Index)は、成人の過体重と肥満を分類するために一般的に使用される身長に対する体重の関係から計算する単純な指標です。これは、キログラム単位の体重をメートル単位の身長の二乗(kg/m2)で割ったものとして定義されます。
中文翻译:
肥胖的定义:
根据世界卫生组织( World Health Organization:WHO ),超重和肥胖被定义为异常或过度的脂肪堆积,可能会损害健康( *5)。指标如下。
超重: BMI在25以上
肥胖: BMI在30以上
※BMI(Body Mass Index )是根据体重与身高的关系计算的简单指标,常用于对成人超重和肥胖进行分类。它的定义是您的体重(公斤)除以身高(米)的平方 (kg/m2)。
3、<肥満の原因>
これもまたWHOによれば、肥満と過体重の根本的な原因は、摂取カロリーと消費カロリーの間のエネルギーバランスの不均衡です(*5)。すなわちカロリーの過剰摂取と運動不足が原因になると言っています。
ただし、満腹感を促すホルモンや、代謝に係る因子が正常に動かないという遺伝的な要因でエネルギーバランスの不均衡が起こる場合もあります(*6)。また、最近の知見では、下記に述べるように、腸内細菌バランスが崩れることで肥満になりやすくなることがわかっています。
中文翻译:
肥胖的原因:
据世卫组织称,肥胖和超重的根本原因是摄取热量卡路里和消耗卡路里之间的能量平衡不均衡( *5)。也就是说,肥胖原因是卡路里的摄取过多和运动不足。
然而,由于遗传因素(例如促进饱腹感的激素或与新陈代谢功能不正常相关的因素)也可能会出现能量失衡(*6)。此外,最近的研究结果表明,肠道细菌失衡会导致肥胖,如下所述。
但是,也有可能因为促进饱腹感的激素和代谢相关的因子不能正常动作的遗传因素而引起能量平衡的不均衡( *6)。此外,最近的研究结果表明,肠道细菌失衡会导致肥胖,如下所述。
4、<肥満と腸内細菌>
これまでに肥満と腸内細菌の関係を示すいくつかの研究が報告されています。例えば、2013年には無菌のマウスの腸に、肥満とやせ形の双子の腸内細菌を移植すると、肥満の人の腸内細菌を移植したマウスは太り、痩せた人の腸内細菌を移植したマウスは痩せるという結果が報告されました(*7)。また、肥満の人と普通の人の腸内細菌バランスが異なることを示す研究も多数報告されています(*8)。増減する菌の種類については必ずしも結果の一致があるわけではなく、特定の細菌が良い悪いというよりも、腸内細菌の多様性が減じていることが肥満に関係する、と解釈されています。
では、なぜ腸内細菌が肥満と関係するのでしょうか。腸内細菌は、人間が分解できない食物繊維などを分解し、酢酸、酪酸、プロピオン酸などの短鎖脂肪酸をつくります。この短鎖脂肪酸は、人間のエネルギー源になるだけではなく、下記のように肥満抑制に関与する種々の作用を持っています(*9)。
①
交感神経を刺激して、体温上昇や酸素消費などのエネルギー消費を上昇させる
②
脂肪組織では、脂肪細胞への脂肪の蓄積を抑える
③
脂肪組織以外の組織では、脂質・糖代謝を促進する
④
腸管内分泌細胞に、食欲を抑制につながるホルモンを分泌させる
従って、短鎖脂肪酸を作る腸内細菌の割合は、肥満になりやすいかどうかに関係します。
中文翻译:
肥胖与肠道细菌:
迄今为止,已有一些研究表明肥胖与肠道细菌之间存在关系。
例如,2013年有报告称,研究人员将肥胖和体重不足双胞胎的肠道细菌移植到无菌小鼠的肠道中,据报道,接受这种治疗的小鼠体重减轻了(*7)。
此外,许多研究表明,肥胖者和正常人的肠道细菌平衡是不同的(*8)。对于增加或减少的细菌种类不一定有共识,有人解释肥胖与肠道细菌多样性减少有关,而不是与特定细菌的好坏有关。
那么,为什么肠道细菌与肥胖有关呢?肠道细菌会分解人类无法分解的膳食纤维,并产生短链脂肪酸,如乙酸、丁酸和丙酸。这些短链脂肪酸不仅作为人类的能量来源,还具有抑制肥胖的各种作用(*9)。
肠道细菌决定BMI?

01.刺激交感神经,增加体温、耗氧量等能量消耗
02.在脂肪组织中,抑制脂肪细胞内的脂肪堆积
03.在脂肪组织以外的组织中,促进脂质和糖代谢
04.使肠道内分泌细胞分泌抑制食欲的激素
因此,肠道细菌产生短链脂肪酸的比例与是否容易肥胖有关。
5、<肥満と炎症>
近年、肥満は炎症性疾患だと言われます。それは肥満になると脂肪組織で炎症が起きるからです。
カロリー過剰摂取によって脂肪細胞が肥大すると、脂肪細胞がマクロファージを呼び集める因子を分泌し始め、集まってきたマクロファージと脂肪細胞の両方が炎症性因子を出すことによって脂肪組織で炎症が起こります(*10)。ここで起こる炎症は、インスリン抵抗性(インスリンが出ていても、そのシグナルを受け取る細胞の感受性が低くなる状態)を与えます。インスリン抵抗性が起こると、作用を代償するためインスリン分泌は亢進することとなり、その結果、すい臓のβ細胞が疲弊したり死んだりし、真のインスリン不足となり2型糖尿病が発症します。
脂肪組織の変化
ところで、肥満になるならないとは関係なく、上述したように、カロリー過剰摂取によって、腸内細菌バランスがくずれます。腸内細菌の作る短鎖脂肪酸は、腸壁の粘液や抗炎症物質を増加させる役目も持っており、腸内細菌バランスのくずれによって短鎖脂肪酸が少なくなると、腸管のバリア機能が弱まりリーキーガットの原因になります(*11, *12)。こうしてリーキーガットになると、腸内細菌や腸内細菌由来のLPSが体の中に移行し炎症を起こします。肥満が炎症性疾患だと言われる所以として、このカロリー過剰摂取の結果として起こるリーキーガット経由の炎症も、合わせて考えられているようです。
腸内細菌叢の乱れからくるリーキーガット
中文翻译:
肥胖与炎症:
近年来,肥胖被描述为一种炎症性疾病。主要原因是肥胖会导致脂肪组织发炎。
当脂肪细胞因摄入过多热量而增大时,脂肪细胞开始分泌召集巨噬细胞的因子,聚集的巨噬细胞和脂肪细胞两者都会产生炎症因子,从而在脂肪组织中引起炎症( *10 )。
这里发生的炎症会导致胰岛素抵抗(在这种情况下,即使产生胰岛素,接收胰岛素信号的细胞也会变得不那么敏感)。
当出现胰岛素抵抗时,胰岛素分泌会增加以补偿其影响,结果导致胰脏的β细胞疲劳或死亡,导致真正的胰岛素不足,2型糖尿病发病。
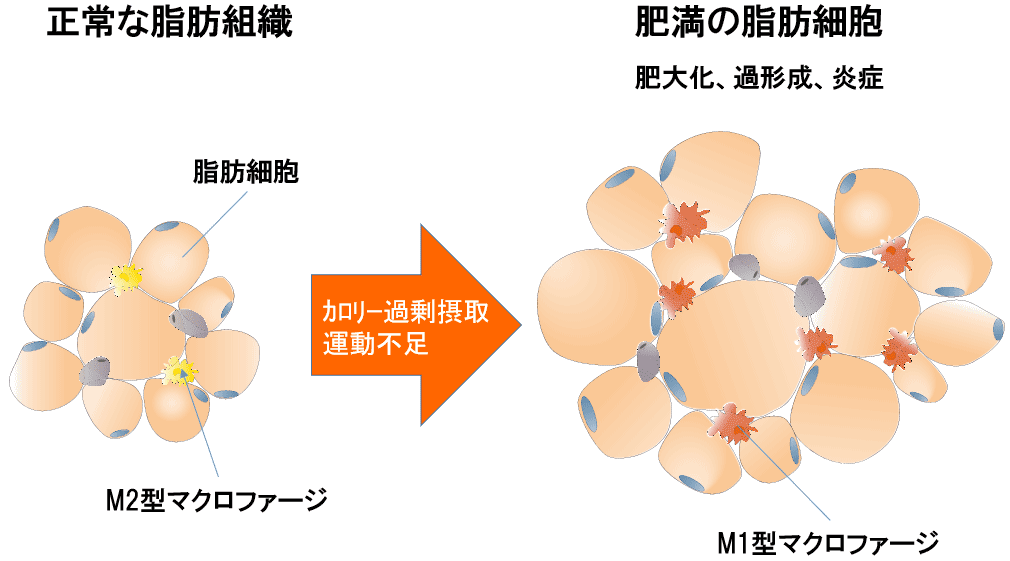
图丨脂肪组织的变化
但是,与是否肥胖无关,如上所述,过多的热量摄入都会破坏肠道细菌的平衡。
肠道细菌产生的短链脂肪酸还具有增加肠壁粘液和抗炎物质的作用,当肠道细菌失衡导致短链脂肪酸减少时,肠道屏障功能减弱,这将导致出现肠漏 (*11, *12)。
当发生肠漏时,肠道细菌和源自肠道细菌的LPS泛菌糖脂质会迁移到体内并引起炎症。由于卡路里摄入过多而导致的肠漏炎症也被认为是肥胖被称为炎症性疾病的原因。
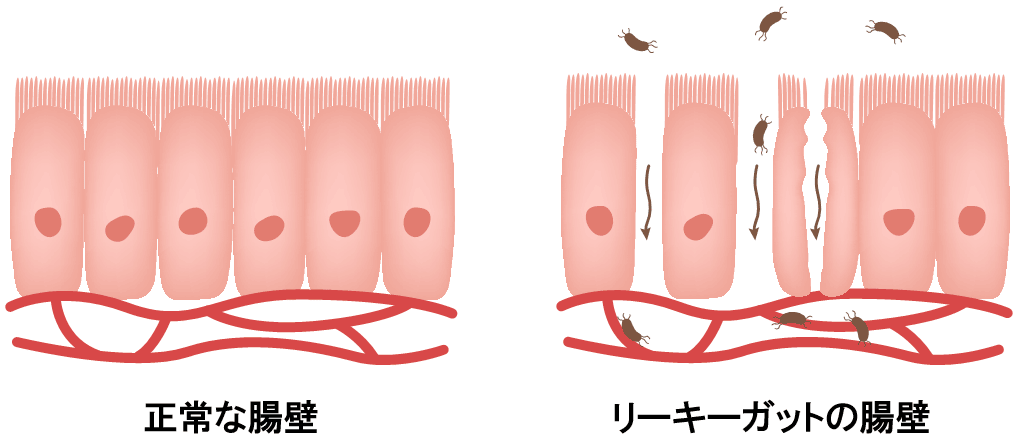
图丨肠道菌群紊乱引起肠漏
本文参考文献 :
(*1)投稿準備中
(*2)Metabolic endotoxemia initiates obesity and insulin resistance.
Diabetes, 56:1761-1772(2007)
(*3)Oral administration of Pantoea agglomerans-derived lipopolysaccharide prevents metabolic dysfunction and Alzheimer's disease-related memory loss in senescence-accelerated prone 8 (SAMP8) mice fed a high-fat diet.
PLOS ONE, https://doi.org/10.137/journal.pone.0198493 (2018)
(*4)Oral administration of Pantoea agglomerans-derived lipopolysaccharide prevents development of atherosclerosis in high-fat diet-fed apoE-deficient mice via ameliorating hyperlipidemia, pro-inflammatory mediators and oxidative resposes.
PLOS ONE, https://doi.org/10.137/journal.pone.0195008 (2018)
(*5)https://www.who.int/news-room/fact-sheets/detail/obesity-and-overweight
(*6)Obesity – is it a genetic disorder?
Journal of Internal Medicine, 254: 401–425 (2003)
(*7)Cultured gut microbiota from twins discordant for obesity modulate adiposity and metabolic phenotypes in mice.
Science, 341:6150-(2013)
(*8)The Gut Microbiome Profile in Obesity: A Systematic Review.
International Journal of Endocrinology, https://doi.org/10.1155/2018/4095789 (2018)
(*9)糖尿病と腸内細菌
モダンメディア、62:159-165 (2016)
(*10)肥満の脂肪組織における脂肪細胞とマクロファージのパラクリン調節系
「肥満研究」12:70-72 (2006)
(*11)Short chain fatty acids stimulate epithelial mucin 2 expression through differential effects on prostaglandin E1and E2 production by intestinal myofibroblasts.
Gut, 52: 1442–1447 (2003)
(*12)Microbiota-derived short-chain fatty acids promote Th1 cell IL-10 production to maintain intestinal homeostasis.
Nature Communications, 9: 3555 (2018)
复合免疫 健康活力





























