
研究实证|四氢姜黄素vs姜黄素:谁才是缓解氧化应激肾损伤的“最优解”?
姜黄素,特别是四氢姜黄素可改善氧化应激诱导的小鼠肾损伤
在追求健康生活的路上,我们总在寻找那些能抵御疾病、延缓衰老的“秘密武器”。氧化应激,这个看似陌生的词,其实悄悄关联着癌症、神经退行性疾病、糖尿病等棘手问题,也给肾脏带来不小负担——熬夜、代谢失衡、外界毒素,都在一点点加重它的压力。
那有没有一种天然成分,能帮身体更好地轻松应对这些挑战?
姜黄素,大家或许不陌生——它是咖喱泛着金黄的来源,也是抗氧化界公认的“明星成分”,早已在养生领域出圈。但你可能不知道,当姜黄素褪去颜色、在体内完成代谢转化后,会变身成一个“低调而强大”的代谢产物——四氢姜黄素。它无色、更易吸收,在抗氧化和保护器官损伤方面,甚至比姜黄素更出色。就连《营养学杂志》的经典研究都专门验证过这一点。
这项研究专门对比了两者缓解氧化应激肾损伤的差异,结果十分明确:四氢姜黄素不仅吸收更快、利用率更高,还能直击肾损伤核心——清除体内多余自由基、激活身体自带的抗氧化酶,给肾脏多一重天然、精准的守护,这也是它区别于姜黄素的核心优势所在。
今天,我们就来结合《营养学杂志》的研究,聊聊这场"颜色革命"背后的科学奥秘——四氢姜黄素究竟如何护肾?又会给我们的日常健康防护带来哪些启发?
姜黄素,特别是四氢姜黄素可改善氧化应激诱导的小鼠肾损伤
摘要
本研究探讨了姜黄素(U1,姜黄中主要的黄色色素之一)及其衍生物四氢姜黄素(THU1)对次氮基三乙酸铁(Fe-NTA)诱导的氧化性肾损伤的保护作用,实验对象为雄性ddY小鼠。单次Fe-NTA处理(5 mg Fe/kg体重,腹腔注射)可短暂引发氧化应激,表现为肾脏中脂质过氧化产物及8-羟基-2'-脱氧鸟苷的蓄积。小鼠饲喂含0.5 g/100 g U1或THU1的饲料4周。结果显示,THU1显著抑制了肾脏中2-硫代巴比妥酸反应物质、4-羟基-2-壬烯醛修饰蛋白及8-羟基-2'-脱氧鸟苷的形成;而U1仅抑制4-羟基-2-壬烯醛修饰蛋白的形成。为阐明U1与THU1的保护机制,采用高效液相色谱法考察其药代动力学特性,并利用电子自旋共振自旋捕集技术(以5,5-二甲基-1-吡咯啉-N-氧化物为捕集剂)分析二者的自由基清除能力,同时研究了抗氧化酶的诱导情况。THU1组肝脏及血清中THU1及其结合物(硫酸盐与葡萄糖醛酸苷形式)含量均高于U1组;即使在U1组中,U1及其结合物的含量也较低。这些结果表明,THU1比U1更易从胃肠道吸收。此外,THU1诱导抗氧化酶(如谷胱甘肽过氧化物酶、谷胱甘肽S-转移酶和NADPH:醌还原酶)的效果与U1相当或更优于U1,且在体外实验中对Fe-NTA诱导的自由基清除能力优于U1。这些结果表明U1在体内可转化为THU1,且THU1是一种更具前景的化学预防剂。《营养学杂志》131: 2090–2095, 2001。
多项研究证据表明,氧化应激可能在多种病理状态中发挥重要作用,包括癌症、神经退行性疾病、动脉粥样硬化、糖尿病、类风湿性关节炎,以及药物相关毒性、缺血后再灌注损伤和衰老等(1)。铁螯合物——(Fe-NTA)²可诱发急性肾近端小管坏死,这是自由基介导的氧化性组织损伤所致,最终会导致啮齿动物肾细胞癌的发病率升高(2-4)。研究显示,通过脂质过氧化产物、醛修饰蛋白及多种修饰DNA碱基(如8-羟基-2‘-脱氧鸟苷[8-OHdG])评估的自由基相关修饰分子含量,在单次Fe-NTA处理后3小时内即达到峰值,随后逐渐下降(5,6)。
姜黄素是姜黄(Curcuma longa Linn的根茎粉末)中主要的黄色色素,广泛用作咖喱、芥末、薯片等多种食品的香料和着色剂,同时也应用于化妆品和药品领域。学界已对姜黄素广泛的生物学及药理学活性进行了深入研究(7,8)。姜黄素是诱变和化学诱导致癌作用的有效抑制剂(9-11)。它具有多种治疗特性,包括抗炎和抗癌活性(12)。目前,姜黄素因其抗氧化潜力以及对啮齿类动物相对较低的毒性而备受关注。姜黄素类化合物在一些体外脂质过氧化系统中也表现出抗氧化活性(13,14),并能抑制12-O-十四烷酰佛波醇-13-乙酸酯诱导的小鼠表皮过氧化氢生成和氧化DNA形成(15)。此外,姜黄素还可抑制中性粒细胞反应(16)和巨噬细胞中超氧化物的生成(17)。
四氢姜黄素(THU1;图1)是姜黄素(U1)的主要无色代谢产物之一,以葡萄糖醛酸结合物的形式存在,在多个体外系统中表现出比姜黄素更强的抗氧化活性(13,14)。因此,学界推测THU1可能是肠道中生理活性和药理活性均优于U1的主要代谢产物之一。然而,关于U1与THU1在体内的代谢过程及抗氧化功能研究数据仍较为匮乏。此外,关于哪种分子作为化学预防剂更具疗效仍存在争议。最近有报道称,THU1在小鼠皮肤中的化学预防效果较姜黄素更弱(18,19)。然而,在饮食中添加0.5%的THU1能显著抑制1,2-二甲基肼诱导的小鼠结肠癌发生,而U1的抑制作用则不显著(20)。
图1、U1与THU1的化学结构。
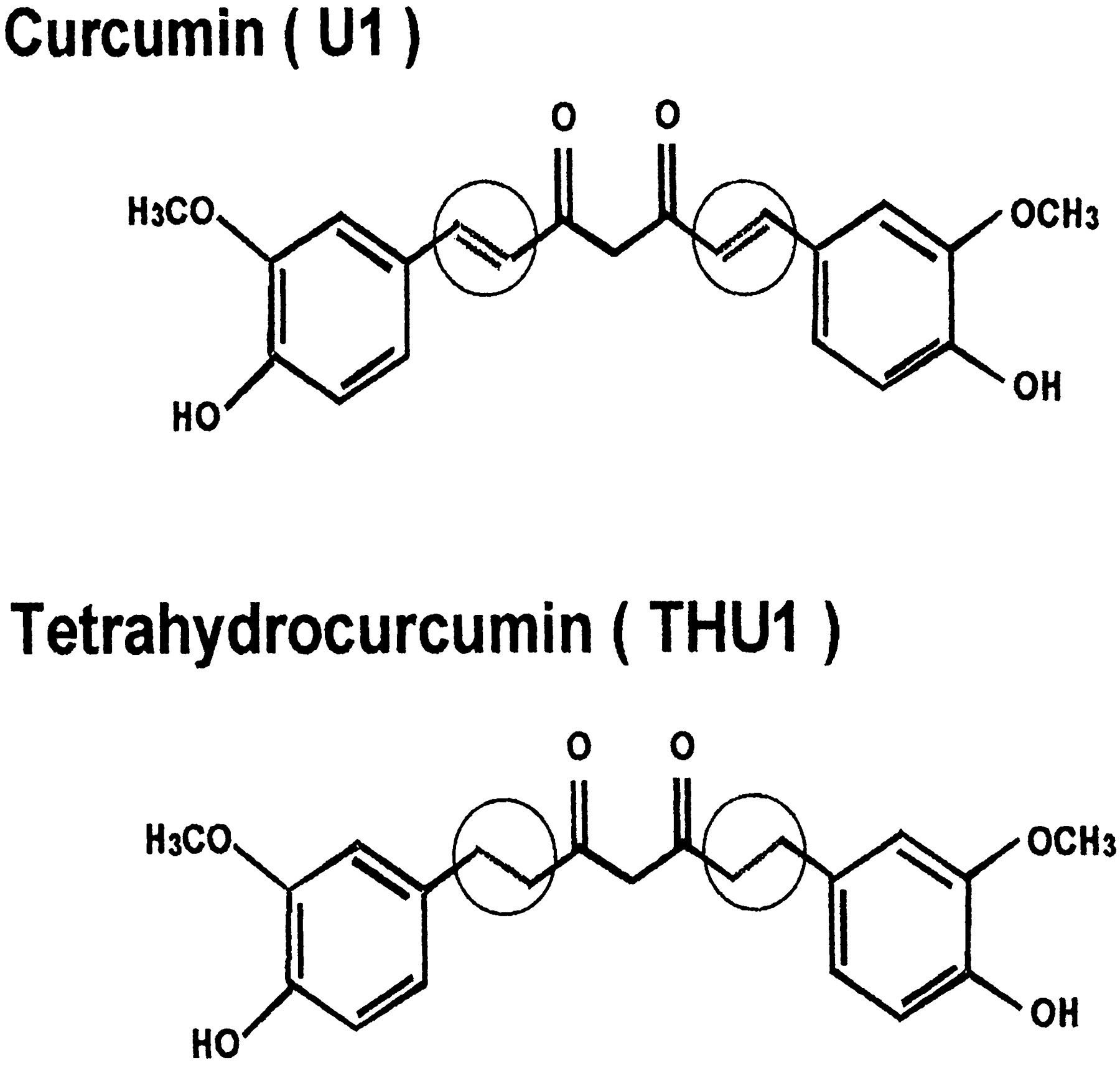
在本研究中,我们给小鼠喂食含有0.5% U1或THU1的饲料,评估它们对Fe-NTA诱导的氧化性肾损伤的影响,重点关注U1和THU1作为抗氧化剂的能力,并研究了这些化合物的代谢情况。
结果
体重及肝脏、肾脏重量
三组小鼠的体重、肝脏和肾脏重量均无显著差异(数据未显示),这表明U1与THU1饮食方案并未对食物摄入量产生不良影响。
U1和THU1的浓度
在肝脏和血清中,大部分U1和THU1以结合型葡萄糖醛酸苷或硫酸盐结合物的形式存在;仅检测到少量游离形式(表2和表3)。在U1饮食组的小鼠血清中检测出少量U1及其结合物(硫酸盐和葡萄糖醛酸结合物),但在肝脏(表2)或肾脏(数据未显示)中未检测到。THU1及其结合物的浓度均高于U1组肝脏和血清中的U1浓度。因此,当喂食U1时,它会转化为其代谢产物THU1。THU1组肝脏和血清中的THU1及其结合物浓度均高于U1组(表3)。由于HPLC分析灵敏度有限,肾脏中未检测到U1和THU1。
表2、饲喂U1小鼠肝脏与血清中姜黄素类化合物的分布
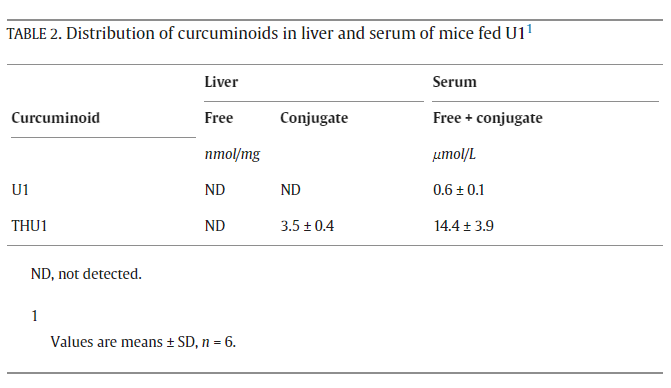
表3、THU1喂养小鼠体内姜黄素类化合物的分布
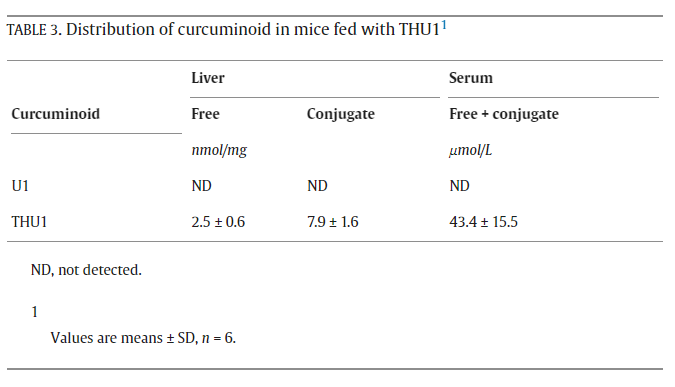
U1和THU1对Fe-NTA处理小鼠肾脏氧化应激的影响
THU1饮食显著抑制了Fe-NTA诱导的脂质过氧化和DNA氧化修饰水平升高(图2)。U1饮食显著降低了肾脏中HNE修饰蛋白浓度,但相对于Fe-NTA处理的对照组,并未显著降低TBARS或8-OHdG浓度。因此,THU1总体上比U1具有更强的抑制作用。
图2、膳食U1和THU1对Fe-NTA诱导的小鼠肾脏氧化应激抑制作用的影响。
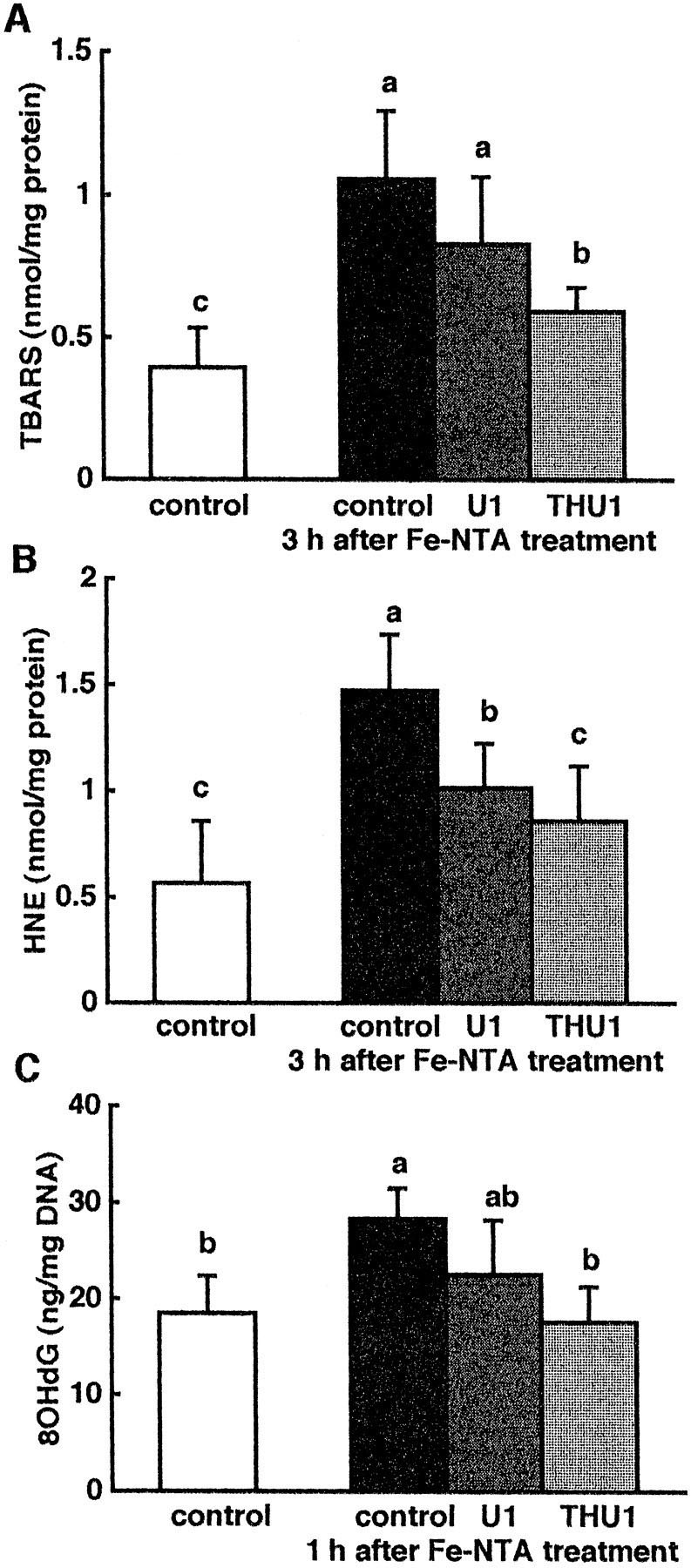
对照组肾脏匀浆中的TBARS和ESR测定
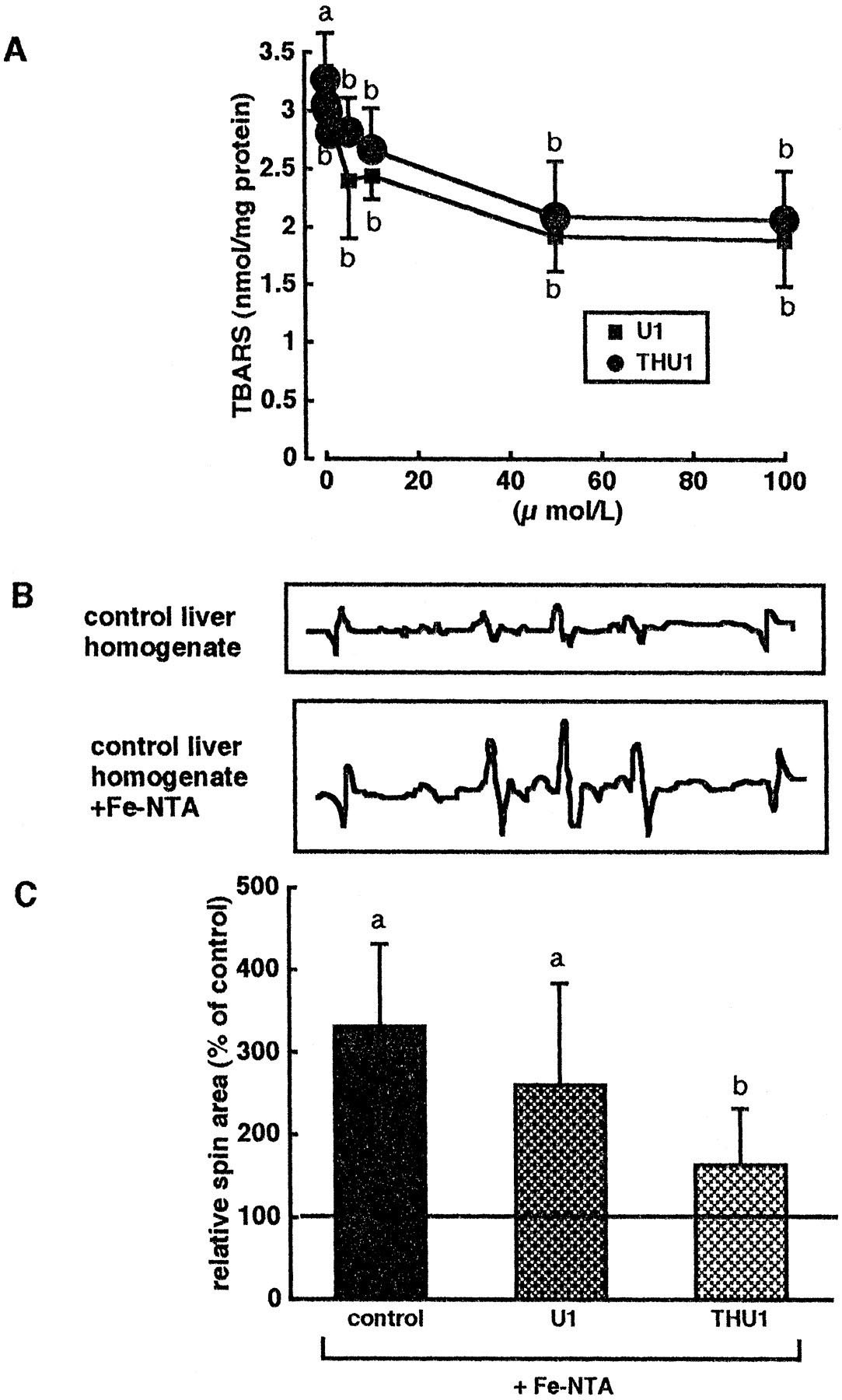
图3A显示对照组肾脏匀浆经U1或THU1按指定浓度处理后,直接给予Fe-NTA处理的TBARS 水平变化。对照组肾脏匀浆中的TBARS含量呈剂量依赖性下降,THU1的作用效果与U1相比无显著差异。图3B和3C显示了在U1和THU1存在下,Fe-NTA处理产生的DMPO自由基自旋加合物的ESR谱图。THU1抑制了由Fe-NTA处理介导的DMPO捕获自由基的形成(图3C)。而U1则未显示显著抑制作用。
图3、U1和THU1对体外实验中添加Fe-NTA后对照组肾脏匀浆中 DMPO自旋加合物脂质过氧化及ESR谱图的影响。
经Fe-NTA处理的小鼠肾脏中的酶活性
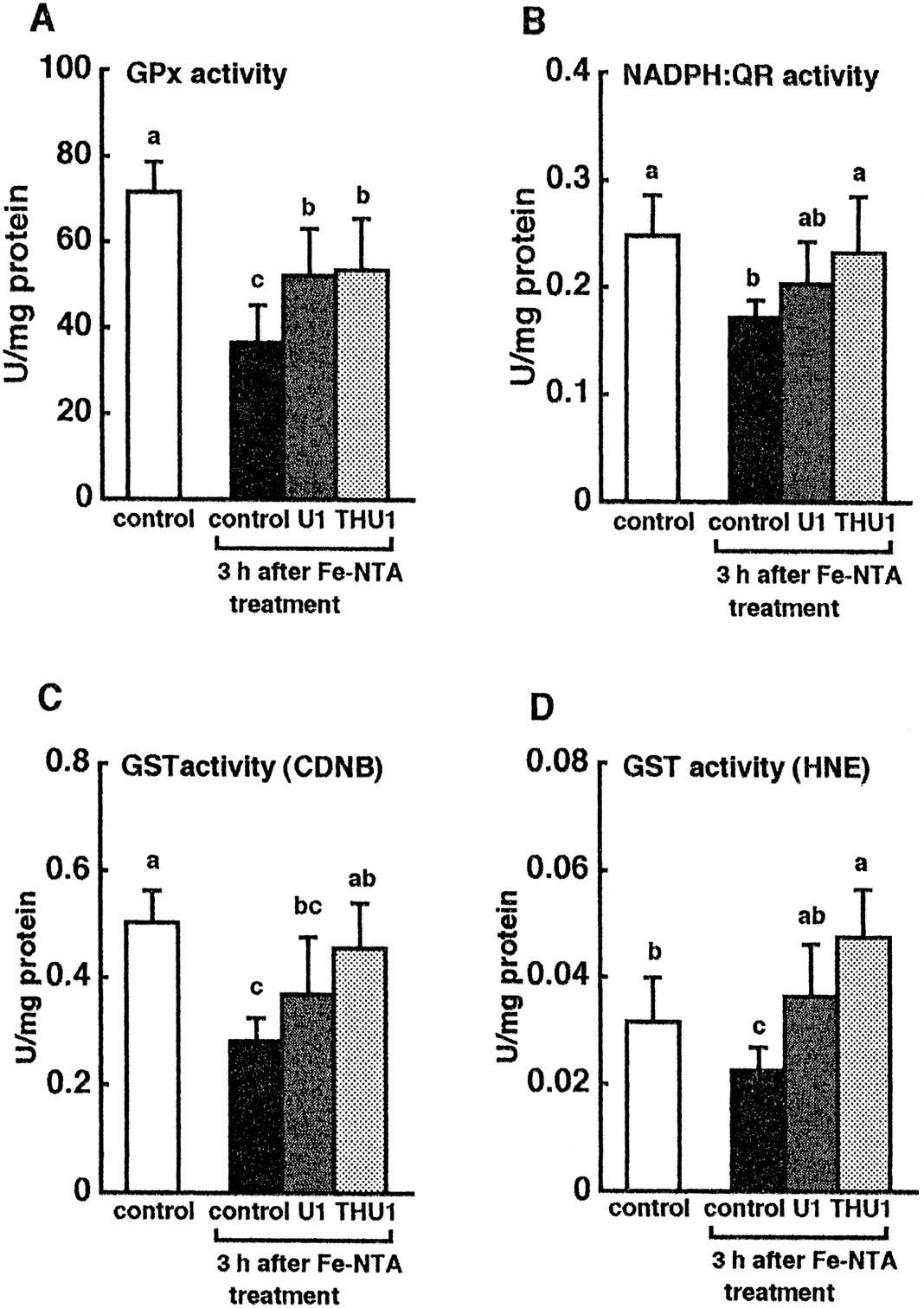
超氧化物歧化酶和过氧化氢酶的活性在Fe-NTA处理后而降低,且U1组与THU1组间无差异(数据未显示)。然而,U1和THU1组的GPx活性抑制程度均低于对照组(图4A)。I相解毒酶细胞色素P450的活性未受影响(数据未显示),而在THU1组中,II相解毒酶NADPH:QR和GST的活性受到抑制(图4B-D),U1组未见显著变化。在THU1组中,II相酶的诱导程度总体上高于U1组。THU1饮食不仅抑制了Fe-NTA处理导致的总GST活性下降,而且对HNE的GST活性诱导作用也显著强于未处理的对照肾脏样本(图4D)。
图4、饮食中U1和THU1对Fe-NTA处理小鼠肾脏中GPx(A)、NADPH:QR(B)及GST(C和D)活性的影响。
讨论
近年来,人们对膳食抗氧化剂的保护功能日益关注,这类物质是癌症化学预防和延长寿命的候选成分。已有研究发现,维生素E、维生素C、β-胡萝卜素、尿酸、泛醇及类黄酮等多种抗氧化剂,在非酶促防御氧化应激中发挥着重要作用。然而,有观点指出,这些抗氧化剂中的单一成分尚不足以预防癌变。因此,预期食物中仅少数成分能够协同发挥预防癌变的作用。在我们近期研究中,在我们近期研究中,口服给药后U1化合物在肠道内转化为具有强抗氧化活性的四氢型代谢产物(13,14)。该转化现象在培养细胞中亦被检测观察到(31)。我们由此推测THU1具有抗癌效应。
我们的研究结果表明,THU1比U1具有更好的吸收特性(表2和表3)。当给予相同剂量的THU1饮食,THU1组中THU1及其结合物(以硫酸盐和葡萄糖醛酸苷形式存在)的含量高于U1组。相比之下,两组中U1及其结合物的含量均较低。体外实验显示,THU1与U1具有相同的抗氧化能力(图3A),但THU1的抗氧化效果比U1更显著。事实上,在THU1混合肾脏匀浆中,Fe-NTA介导的DMPO自由基自旋加合物的ESR谱图信号比U1混合匀浆中减弱得更为明显,后者与对照组相比无显著差异(图 3B 和 3C)。
有观点认为,优先诱导II相生物转化酶(如GST和NADPH:QR),而非I相生物转化酶(细胞色素P450系统),可能是多种抗氧化剂在癌症预防中发挥作用的机制之一(32-34)。研究表明,即使采用高剂量,口服U1也能轻微提升小鼠肝脏中对CDNB的GST活性(35)。然而,小鼠肝脏对HNE的GST活性相对较高(36)。GST由多种催化特性不同的同工酶组成,每种同工酶的表达均受到细胞内氧化或抗氧化环境的差异调控(37)。因此,本研究旨在探讨口服U1和THU1对Fe-NTA注射后小鼠肾脏中GSH相关抗氧化防御系统的影响,包括GPx活性以及对CDNB和HNE的GST活性。
我们发现,U1的抗氧化作用通常通过恢复Fe-NTA降低的GPx活性和HNE代谢型GST同工酶活性而增强(图4)。在这些抗氧化酶诱导方面,THU1的作用效果强于U1。本研究还证实,口服THU1在II相酶诱导期间具有显著作用(图4)。具体而言,对HNE的GST活性诱导程度显著高于未处理的对照组。该诱导效应可能源于THU1单独暴露引起。目前正在进行更详细的研究,以阐明这些抗氧化剂如何诱导酶活性的分子机制。
I相酶通过氧化还原反应和水解作用使外源物质失活。细胞色素P450是主要的I相酶之一,可被药物、工业化学品、食品添加剂、烟草、酒精及各种食品成分等因素诱导。然而,多种化学物质也可被细胞色素P450激活。这类化合物被分为两类:双功能诱导剂(可同时提升I相和II相酶活性)和单功能诱导剂(可选择性提升II相酶活性)。I相酶(如细胞色素P450同工酶)的诱导是对于外源性物质的代谢清除所必需的(38),但由于其具有激活前致癌物而被视为潜在风险因素(39)。因此,U1和THU1被鉴定为单功能诱导剂这一发现具有重要的生物学意义。
综上所述,本研究为膳食U1和THU1抑制氧化应激诱导的肾损伤提供了明确的证据。U1和THU1可能通过两种不同的机制发挥作用:直接螯合或清除效应,以及诱导抗氧化酶(作为单功能诱导剂)。THU1的体内抗氧化作用优于U1。THU1可能比U1更易于从胃肠道吸收。此外,THU1 作为食品添加剂还具有一些优势,因为它无色,且可通过U1的标准氢化工艺轻松制备。未来仍需对姜黄素类化合物对氧化应激方面的影响,尤其是其分子机制进一步研究,我们认为THU1具有作为人类化学预防剂的应用潜力。
免责声明
以上部分内容来源于外网我们重在信息分享,版权归属原作者或原刊发平台所有,如有侵权、信息有误或其他异议,请联系处理,我们将在24小时内删除或整改。
复合免疫 健康活力





























