
四氢姜黄素:姜黄素家族的"后起之秀",凭什么抗癌更有效?
四氢姜黄素的癌症化学预防和治疗潜力
癌症,已然是21世纪最棘手的健康难题,每年夺走全球数百万人的生命。即便肿瘤研究不断取得突破,寻找更安全、高效的预防与干预方案,依然是科研与临床的核心方向。科学家们日夜求索,试图找到那把能打开治愈之门的钥匙。而答案,或许就藏在一味古老的香料之中——姜黄。
千百年来,姜黄作为“药食同源”的宝藏,被用于消炎、护肝、养生等方面沿用至今。真正让它在医学界掀起波澜的,是其核心成分姜黄素。然而一个尴尬的现实是:姜黄素虽好,人体却难以吸收。当它的临床应用因“吸收难、代谢快”而屡屡碰壁时,它的代谢产物——四氢姜黄素,却悄然崭露头角。
更好的水溶性、更强的化学稳定性、更高的生物利用度……这位“姜黄素家族”的后起之秀,正凭借其独特的抗癌潜力,成为肿瘤防治领域的新焦点。大量体外与体内研究证实,四氢姜黄素可通过调控氧化应激、炎症、细胞增殖、转移、程序性 细胞死亡及免疫等多条通路,发挥比姜黄素更具优势的抗癌作用。
那么,这份源自天然的物质,它究竟如何从分子层面狙击恶性肿瘤?距离真正的临床转化还有多远?临床应用的道路上又面临着哪些挑战?本文将带您深入解读四氢姜黄素的抗癌机制,看这味来自古老东方的天然产物,如何在现代科学的显微镜下,绽放出对抗癌症的新希望。
四氢姜黄素的癌症化学预防和治疗潜力
摘要
近几十年来,癌症一直是全球范围内主要的致死原因之一。尽管在对肿瘤发生的分子机制、诊断方法及临床治疗的基础研究方面已取得进展,但有效药物的发现与开发仍是癌症研究中活跃且至关重要的领域。四氢姜黄素是姜黄素的主要姜黄素类代谢产物,天然存在于姜黄中。随着研究的深入,四氢姜黄素因其在水溶性、化学稳定性、生物利用度和抗氧化活性方面均优于姜黄素而日益受到关注。大量体外与体内研究表明,四氢姜黄素通过调节氧化应激、外源性物质解毒、炎症、增殖、转移、程序性细胞死亡及免疫等多种机制发挥抗癌作用。尽管四氢姜黄素与姜黄素在药理作用上具有相似性,但四氢姜黄素的结构决定了其独特且特异性的分子机制,从而使其成为癌症预防与治疗的潜在候选药物。然而,由于目前仅开展了有限的药代动力学和口服生物利用度研究,四氢姜黄素的临床应用价值尚待进一步评估。本综述系统总结了四氢姜黄素抗癌特性研究进展,本综述系统总结了四氢姜黄素抗癌特性的相关研究进展,并阐述了其作用机制。
关键词:癌症化学预防;四氢姜黄素
1. 引言
姜黄是来源于姜科(Zingiberaceae)植物姜黄(Curcuma longa L.)的一种干燥的橙黄色根茎,可用作香料和食品添加剂。在中国和印度,姜黄作为传统药物已有数千年历史,用于治疗多种疾病,如炎症性疾病、肝胃疾病、感染及咳嗽等[1]。此外,在过去50年中,姜黄的生物学特性已得到广泛的科学的证实。姜黄素作为姜黄的一种主要活性成分,由Vogel和Pelletier于1815年首次鉴定发现[2],并于1949年首次报道其具有抗菌活性[3]。自20世纪90年代以来,关于姜黄素的生物学研究显著增加[4]。大量体外、体内研究及临床研究试验均已证实姜黄素在疾病预防与治疗中的益处。与此同时,学界对姜黄化学成分的研究兴趣也急剧增加[5]。目前已从姜黄中分离鉴定出超过230种植物化学物质,包括萜类化合物、姜黄素类、黄酮类、甾体类、生物碱及其他酚类化合物。这些化合物与姜黄素共同构成了姜黄广泛的生物活性谱系,为开发多种营养保健品和药物提供了重要来源 [6]。
姜黄素类化合物,包括姜黄素、去甲氧基姜黄素和双去甲氧基姜黄素,占姜黄活性成分的2-9%,具体含量取决于姜黄的品种以及根茎的栽培和加工条件[5]。它们属于具有芳基-C7-芳基骨架的二芳基庚烷类化合物,被认为是姜黄生物活性的主要活性成分[7]。其中,姜黄素含量最为丰富,研究也最为广泛,PubMed数据库中收录的相关文献已超过9000篇。多项研究强调了姜黄素具有广泛的生理和生物学特性,可能有助于预防和控制心血管疾病、肝脏疾病、高血压、肥胖症、糖尿病、神经系统疾病、炎症、皮肤病、纤维化和关节炎等疾病。其作用机制包括调节多种信号分子、转录因子和酶,以及调控表观遗传活性[8,9]。姜黄素在癌症化学预防和治疗方面的潜力也备受关注,多项细胞研究与动物实验已充分证实其抗癌作用[10,11]。姜黄素的抗癌机制被认为归因于其抗氧化、抗增殖、抗炎、抗侵袭、抗转移和抗血管生成等特性,以及其诱导细胞周期阻滞和程序性细胞死亡(凋亡和自噬)的能力 [8,10]。此外,多项临床研究评估了姜黄素单独使用或与传统化疗和放疗联合使用,对胰腺癌、结肠癌、乳腺癌和前列腺癌的疗效[11]。
尽管姜黄素强大的抗癌效果已被广泛报道,但由于其化学不稳定性、吸收差、快速代谢和快速消除导致的全身生物利用度低,其临床应用受到限制[12]。为解决姜黄素吸收受限的问题,目前已采用多种有前景的方法,包括纳米技术(如聚合物纳米颗粒、脂质体、纳米凝胶)、肽和蛋白质制剂以及环糊精复合物等[13]。胡椒碱可通过增加吸收并抑制葡萄糖醛酸化来提高姜黄素的生物利用度[14]。此外,对姜黄素进行结构修饰可改善其化学稳定性以及化学和药代动力学特性[15]。
过去十年间,为提高姜黄素的动力学稳定性、代谢产物及降解特性,科研人员已成功鉴定并分离出姜黄素代谢产物。这些发现有助于理解姜黄素的生物转化过程,并协助识别由其衍生的独特化合物。姜黄素生物利用度低与其多种生物学功效相矛盾[16]。口服后,姜黄素在体内通过还原和葡萄糖醛酸化发生生物转化,从而产生多种代谢产物,其中部分代谢物的化学稳定性优于母体分子。因此有研究指出,姜黄素的降解产物和代谢产物对其多种生物活性具有关键作用[17]。代谢产物的不同化学结构可能具有与姜黄素不同的生理特性和分子靶点;因此,有必要开展进一步的科学研究以确定其额外的潜在健康益处。
四氢姜黄素因其相较于姜黄素具有更好的生物利用度,以及不同的生物活性和分子机制而备受关注。四氢姜黄素以其抗氧化、抗糖尿病和细胞保护活性而闻名,相关研究已有文献综述[18,19]。多项研究还表明,四氢姜黄素在预防和治疗多种癌症方面比姜黄素更有效(详见下文第3节所述)。尽管四氢姜黄素的抗氧化潜力已被研究,但其对姜黄素已知药理学的贡献尚未得到足够重视。本综述总结了四氢姜黄素的抗癌特性,并探讨了其潜在的作用机制。
2.四氢姜黄素——姜黄素的候选代谢产物
已有许多研究来阐明姜黄素的药代动力学参数及其代谢过程。研究发现,口服给药后的最大血浆浓度(Cmax)和药时曲线下面积(AUC)显著低于静脉注射的结果,表明摄入后吸收率低且存在首过肝脏代谢[20]。研究表明,口服摄入后姜黄素主要在肝脏、肠道及肠道微生物群中经历快速I相和II相代谢,但其代谢产物也在其他器官中被检测到[17,21]。还原反应和结合反应是姜黄素的主要代谢途径。在I相代谢中,醇脱氢酶催化姜黄素双键的还原,形成二氢姜黄素、四氢姜黄素、六氢姜黄素和八氢姜黄素。II相代谢主要发生在肝脏和肠道中,葡萄糖醛酸转移酶和磺基转移酶的作用,将葡萄糖醛酸和硫酸基团结合到姜黄素的酚羟基位置[17]。葡萄糖醛酸化被认为是主要的结合途径。姜黄素及其还原代谢产物也会经历II相代谢,转化为葡萄糖醛酸结合物和硫酸结合物[22]。四氢姜黄素-葡萄糖醛酸和六氢姜黄素-葡萄糖醛酸是主要的胆汁代谢产物,而二氢阿魏酸和阿魏酸是次要代谢物[23]。姜黄素还会经历肠道微生物代谢(如大肠杆菌),通过烟酰胺腺嘌呤二核苷酸磷酸氢(NADPH)依赖性还原酶的催化,分两步还原:首先将姜黄素转化为二氢姜黄素,随后转化为四氢姜黄素[24](图1)。此外,研究还表明,其他代谢产物也可通过脱羟基化、环化及甲基化反应生成[25]。
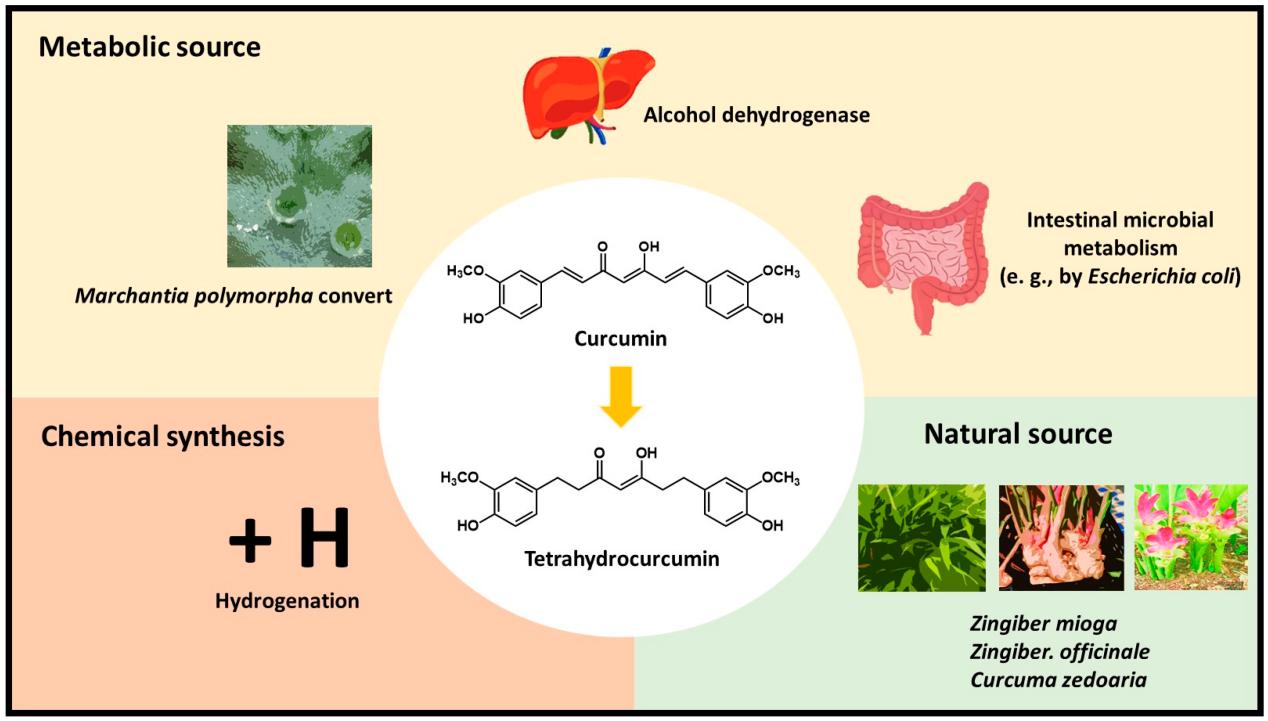
图1. 四氢姜黄素的来源。
2.1. 四氢姜黄素的特性
Holder等人于1978年通过使用氚标记姜黄素的大鼠体内代谢研究,首次将四氢姜黄素鉴定为一种代谢物[23]。四氢姜黄素的化学结构与姜黄素非常相似,但其分子中心七碳链中缺少双键。姜黄素中两个共轭双键是其姜黄特征颜色的的成因,而四氢姜黄素由于缺少α, β-不饱和羰基结构而呈灰白色。研究表明,四氢姜黄素主要以结合形式存在于血清和多种组织(如肠道、肝脏、肾脏、肺、肌肉、胰腺、脾脏和大脑)中被分离出来[26-28]。然而,在摄入姜黄素的小鼠肝脏和血浆中,也鉴定出了未结合和结合形式的四氢姜黄素[28]。在通过不同给药途径以及长期饮食干预后,用姜黄素给药小鼠的血浆和脑组织中也检测到了未结合的四氢姜黄素[29]。
虽然四氢姜黄素被认为是姜黄素的一种代谢产物,但它也天然存在于蘘荷(Zingiber mioga)、姜(Z. officinale)和莪术(Curcuma zedoaria)的根茎中[30,31]。此外,四氢姜黄素还可通过姜黄素的氢化反应(还原双键)进行化学合成获得[32]。研究还发现,地钱(Marchantia polymorpha)的培养细胞也能将姜黄素转化为四氢姜黄素,转化率可达90%/天[33](图1)。研究表明,四氢姜黄素比姜黄素具有更好的溶解性和化学稳定性。Pan等人报道,在不同pH值的0.1 M磷酸盐缓冲液中,四氢姜黄素均表现稳定。此外,在生理pH值的磷酸盐缓冲液中,四氢姜黄素比姜黄素更稳定[22]。进一步研究发现,在pH 8.0的水溶液中,四氢姜黄素比姜黄素更稳定,2小时内未检测到分解[34]。四氢姜黄素的稳定性更高且降解更慢:其在细胞培养基和血浆中的终末半衰期分别为813分钟和232分钟,而姜黄素分别为186分钟和111分钟[35]。
体内研究已证实四氢姜黄素具有更优的口服吸收特性。连续4周每日口服四氢姜黄素后,与单纯饲喂姜黄素的小鼠相比,在小鼠肝脏和血清中检测到的游离四氢姜黄素及其结合物(硫酸盐和葡萄糖醛酸苷)的水平均高于饲喂姜黄素的小鼠[28]。通过口服灌胃、肌肉注射和腹腔注射给予四氢姜黄素的小鼠,无论采用哪种给药途径,其血浆中游离四氢姜黄素的水平均高于给予姜黄素的小鼠。在Tg2576 APPsw小鼠中,这些小鼠连续4个月每日膳食摄入0.5%的四氢姜黄素和姜黄素,也观察到类似结果[29]。这些研究表明,四氢姜黄素比姜黄素具有更好的胃肠道(GI)吸收特性;但其在血浆中的水解稳定性可能更高。尽管如此,在大鼠中四氢姜黄素的口服生物利用度仍被认为较低。该研究还报道,由于尿液中四氢姜黄素浓度较低,四氢姜黄素主要通过非肾脏途径排泄[36]。
2.2. 四氢姜黄素对人类疾病的有益作用
四氢姜黄素比姜黄素具有更多理想的生物学和药理学特性。它已被认为是一种优越的抗氧化剂,这也是其对多种疾病具有化学预防功效的原因,包括高血压、动脉粥样硬化、糖尿病、神经毒性、心血管疾病、肝毒性和肝纤维化[18]。姜黄素同样具有抗氧化作用;但由于其分子中含有苯基羟基、苯基甲氧基和α,β-不饱和羰基结构,以及能够修饰酶活性导致活性氧(ROS)生成的能力,在高剂量下可能引发促氧化效应[37-40]。与姜黄素不同,四氢姜黄素因其中心七碳链中缺乏共轭双键而不会产生ROS[39]。四氢姜黄素的抗氧化机制被认为与其通过苯羟基清除自由基的能力有关;但更重要的是,其活性涉及在氧化过程中β-二酮结构部分两个羰基之间的活性亚甲基碳上的C-C键断裂。这种断裂会产生邻甲氧基苯酚产物,这些产物同样具有抗氧化活性[41]。四氢姜黄素的另一抗氧化机制表现为可增强超氧化物歧化酶、过氧化氢酶、谷胱甘肽过氧化物酶及谷胱甘肽-S-转移酶等抗氧化酶的活性;多项体内研究证实,四氢姜黄素显示出比姜黄素更强的效力[18,28,42,43]。
学界普遍认为,四氢姜黄素的细胞毒性低于姜黄素,并对活性氧(ROS)诱导的细胞损伤和死亡具有细胞保护作用[44–46]。事实上,多项体内研究已证实四氢姜黄素的低毒性特征[46,47]。在一项急性毒性研究中,口服100–10,000 mg/kg剂量的四氢姜黄素持续14天未引起异常行为改变、惊厥或死亡[48]。在免疫缺陷小鼠中,口服3000 mg/kg剂量的四氢姜黄素持续14天,也未显示毒性[46]。在一项为期90天的大鼠亚慢性毒性研究中,剂量高达400 mg/kg的四氢姜黄素未显示死亡率,也未产生生殖系统异常或副作用[49]。四氢姜黄素已被证明可延长果蝇的寿命[50]。此外,在13月龄小鼠中,长期摄入300 mg/kg的四氢姜黄素可延长平均寿命[47]。这些研究表明,四氢姜黄素在药物和营养保健品应用中可能是安全的。
四氢姜黄素相较于姜黄素更具优势的另一关键因素在于其分子靶点,这些靶点与其母体分子不同[19]。尽管二酮部分和酚羟基是姜黄素的主要化学活性官能团,但α,β-不饱和二酮部分被认为是与细胞分子、蛋白质和酶相互作用的最重要的亲核加成反应(即迈克尔加成)。然而,由于四氢姜黄素缺少不饱和二酮结构,无法在迈克尔反应中作为受体,因此,似乎不能直接与蛋白质和酶相互作用[19]。尽管如此,多项体外实验和分子对接对接研究显示,证实四氢姜黄素具有抑制酶活性的能力[36,51,52]。据学界推测,由于四氢姜黄素连接分子芳香环的烃链中缺少双键,四氢姜黄素比姜黄素在分子结构上更具灵活性,因此在与酶的相互作用中表现出更优的结合能[52]。总之,上述研究可能支持这样一个观点:四氢姜黄素的生物学潜力源于其独特的分子机制及对靶点的作用方式。
3 . 四氢姜黄素的抗癌效应及其作用机制
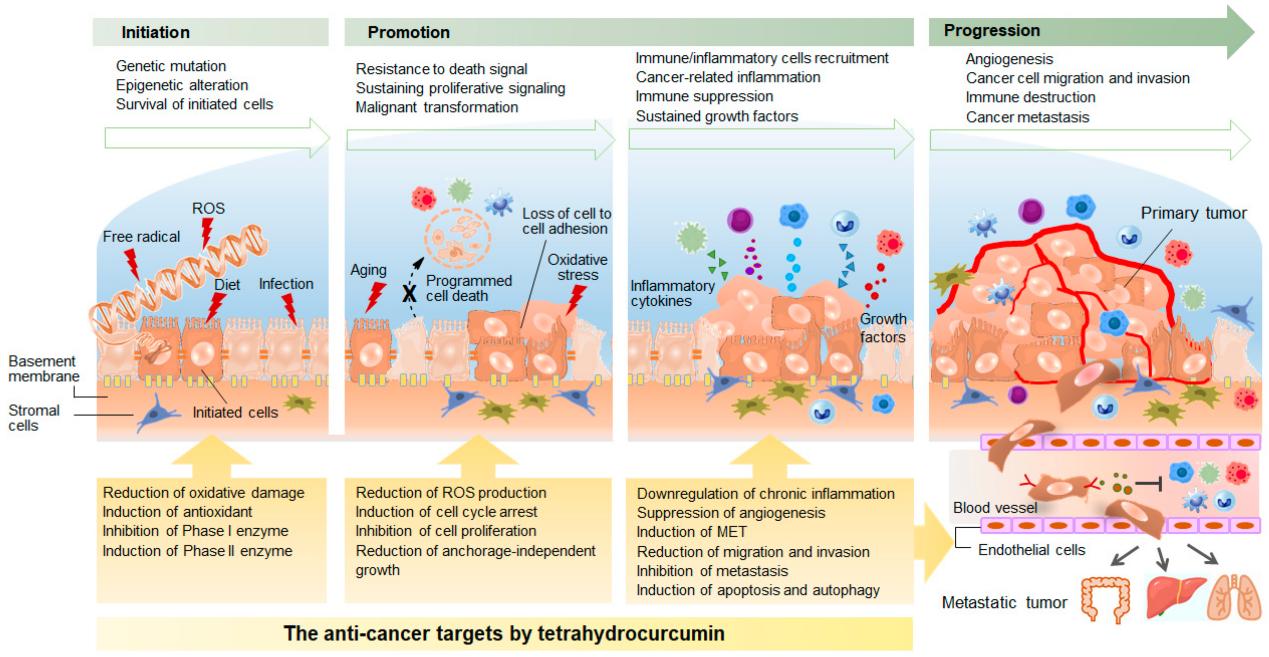
图2. 多步骤肿瘤发生的机制及四氢姜黄素发挥抗癌作用的机制。
癌症是全球发病率和死亡率位居第二的主要原因。肿瘤发生是一个复杂的病理过程,涉及基因表达的遗传和表观遗传学改变(图2)。基因表达失调会导致细胞功能的多种异常。2000年,Hanahan与Weinberg提出了癌症的六大特征:生长信号自给自足、对抗生长信号不敏感性、无限复制潜能、逃避凋亡能力、持续血管生成、组织侵袭和转移[53]。随后在2011年又新增了两个特征:能量代谢重编程和免疫破坏逃逸[54]。这些特征构成了我们理解多阶段肿瘤发生的主要基础。尽管这些概念已被广泛接受,但肿瘤发生和癌症进展的分子机制仍未完全阐明,且癌症依然与高发病率和高死亡率相关。最新研究表明,癌症发展是一个动态过程[55]。癌细胞相互交流,并与基质细胞相互作用,为其增殖和生长创造微环境,同时持续响应多种环境因素而进化。这一演变过程最终可能导致肿瘤内异质性,其特征是肿瘤组织中存在具有不同表型和分子特征的肿瘤细胞群。越来越多的证据表明,肿瘤异质性与治疗耐药性、预后不良和不良临床结局密切相关[55]。尽管癌症在一定程度上仍然神秘莫测,但关于肿瘤发生的认识正在不断积累,为诊断和制定针对各种人类恶性肿瘤的新型治疗策略提供了新信息[56]。姜黄素是姜黄发挥抗癌作用的主要活性成分,但其低生物利用度较低严重限制了其药理学应用。四氢姜黄素与姜黄素具有结构相似性,但表现出更好的溶解性、化学稳定性和生物利用度。由此产生的不同化学特性、生物学性质以及独特的分子靶点,表明四氢姜黄素在癌症预防和治疗中具有潜在应用价值。下文我们总结了四氢姜黄素针对多种恶性肿瘤的作用机制(表1)。
表1. 四氢姜黄素的抗癌机制及分子靶点
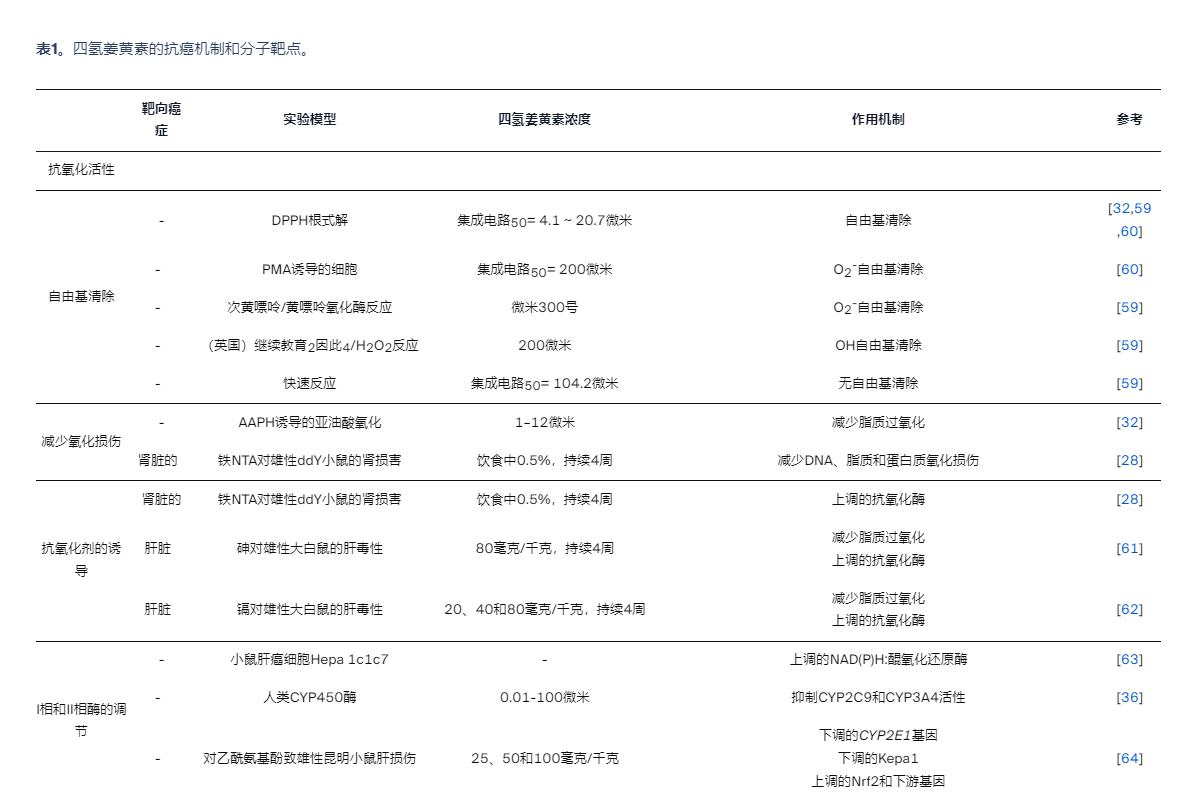



3.1 抗氧化活性
氧化应激(定义为促氧化剂与抗氧化剂之间的失衡)与癌症的发病机制密切相关。已知过量的自由基、活性氧(ROS)和活性氮(RNS)通过影响细胞转化、基因组不稳定性、细胞存活、增殖、分化、代谢、血管生成和侵袭性等机制,参与癌症的发生、促进及进展。癌细胞中的ROS浓度高于正常细胞,这对细胞功能产生显著影响[57]。ROS在癌症发生的启动中发挥重要作用,通过DNA损伤引发基因突变,进而导致原癌基因的激活或肿瘤抑制基因的失活。ROS还会攻击蛋白质、脂质等其他大分子,影响蛋白酶的功能并引起脂质过氧化。细胞膜脂质双层结构的改变最终导致细胞功能障碍[58]。
四氢姜黄素是一种经证实的强效抗氧化剂,研究表明其能够清除自由基、减少活性氧的产生,并上调抗氧化酶的表达,从而减轻肝脏、肾脏、大脑和血管等组织中的氧化应激与病理状态[18]。多项体内研究证实,四氢姜黄素对抗多种多项体内研究表明,四氢姜黄素对抗各种毒物或致癌物介导的氧化损伤及细胞功能障碍的潜在活性优于姜黄素[18,19]。在此,我们重点探讨四氢姜黄素在肿瘤发生过程中的抗氧化作用。
四氢姜黄素已被证实具有清除自由基的能力。在一项DPPH自由基清除实验中,四氢姜黄素表现出比姜黄素更好的清除效果[32,59],而另一项研究则显示两者的清除活性相似[60]。文献报道的四氢姜黄素对DPPH自由基清除的IC50值范围为4.1至20.7 µM;如自由基浓度、孵育时间、溶剂类型以及所用测量方法。超氧阴离子(O2-•)自由基清除实验也观察到类似结果。在佛波醇12-肉豆蔻酸13-乙酸酯(PMA)刺激的细胞悬液中,四氢姜黄素显示出比姜黄素更强的超氧阴离子自由基清除活性(IC50:200 µM姜黄素:IC50 >1357 µM)[60]。另一项研究表明,在次黄嘌呤和黄嘌呤氧化酶的酶促反应中,四氢姜黄素的超氧阴离子自由基清除潜力低于姜黄素[59]。此外,在Fenton反应中,四氢姜黄素清除羟自由基(OH•)的能力强于姜黄素;但对于S-亚硝基-N-乙酰青霉胺(SNAP)产生的一氧化氮(NO)自由基,其清除IC50与姜黄素相当(四氢姜黄素和姜黄素分别为104.2 µM和100.4 µM)[59]。研究认为,四氢姜黄素和姜黄素相当的自由基清除活性与共轭双键的缺失无关。不过,这可能主要与这两种化合物的结构特征有关,包括酚羟基、甲氧基和酮-烯醇部分。研究表明,四氢姜黄素因其结构中的两个共轭双键被氢化而具有供氢能力,这一特性被认为在其强效且高于姜黄素的自由基清除能力中发挥着重要作用[41,85]。此外,四氢姜黄素在Fenton反应中的羟基自由基清除活性,可能不仅有助于其直接清除作用,还可能与铁螯合作用有关[85]。然而,仍需进一步研究分子结构与自由基清除能力之间的关联机制。
四氢姜黄素在显著降低2,2'-偶氮双(2-脒基丙烷)二盐酸盐(AAPH)诱导的亚油酸氧化反应中的脂质过氧化作用方面也更为有效[32]。在脂质过氧化过程中,四氢姜黄素的抗氧化作用被认为源于其β-二酮结构活性亚甲基碳以及邻甲氧基苯酚衍生物处的C-C键断裂[41]。体内研究证实,四氢姜黄素可减轻大分子氧化损伤。次氮基三乙酸铁(Fe-NTA)是一种已知致癌物,可通过氧化损伤和肾毒性诱导肾细胞癌。喂食含0.5%四氢姜黄素饲料4周的小鼠显示,Fe-NTA诱导的肾脏中DNA和蛋白质加合物形成以及脂质过氧化作用均显著降低。与姜黄素治疗组相比,四氢姜黄素治疗组肾脏中8-羟基-2'-脱氧鸟苷(8-OHdG)和4-羟基壬烯醛(HNE)修饰蛋白的浓度显著降低[28]。在同一研究中,喂食四氢姜黄素的小鼠肾脏中谷胱甘肽过氧化物酶(GPx)、谷胱甘肽S-转移酶(GST)和NADPH醌还原酶的活性均高于姜黄素组,这表明四氢姜黄素对氧化损伤的保护作用可能还涉及另一潜在诱导抗氧化酶的产生的机制。四氢姜黄素诱导的肾脏GST活性强于对照组,这表明四氢姜黄素的活性具有特异性[28]。肝脏对代谢和清除毒素、重金属及外源性物质至关重要,但同时也易受毒物引发的病理损伤。研究表明,连续4周摄入80 mg/kg剂量的四氢姜黄素膳食,可通过降低肝脏脂质过氧化、上调谷胱甘肽(GSH)、谷胱甘肽过氧化物酶(GPx)、超氧化物歧化酶(SOD)和过氧化氢酶,显著减轻砷和镉诱导的肝毒性[61,62]。然而,这些研究得出结论,除了上调抗氧化酶外,四氢姜黄素的清除活性(前文已讨论)可能是其发挥肝脏保护作用的另一抗氧化机制。
3.2. I相与II相酶的调节作用
已知I相酶将化学物质或致癌物通过代谢生物转化为亲电中间体,会直接损伤DNA、促进基因突变并修饰其他大分子,这是致癌作用启动阶段的首要步骤[86]。相比之下,II相酶通过向原始分子或I相酶产生的中间体添加亲水基团来催化结合反应,从而促进其通过胆汁或尿液排出体外。一般而言,II相酶的结合反应是细胞防御有毒化学物质、药物和致癌物的解毒步骤。调节I相和II相代谢以减少致癌物的生物转化或增加其消除,是癌症化学预防的一种策略[87]。研究表明,姜黄素因其不饱和的α, β-二酮基团,可通过迈克尔加成反应激活或抑制酶。虽然四氢姜黄素缺乏直接的迈克尔加成反应活性,但它仍能上调小鼠肝癌细胞中NAD(P)H醌氧化还原酶的表达水平[63]。事实上,体内研究显示四氢姜黄素上调I相与II相酶活性可对重金属和药物诱导的肝毒性产生保护作用[62,64]。
四氢姜黄素似乎通过直接和间接机制上调I相和II相酶。Dinkova-Kostova等人报道,由于酮-烯醇互变异构,四氢姜黄素的β-二酮可能能够作为迈克尔反应的受体,从而诱导II相酶。这一点通过一个修饰分子——二苯甲酰丙烷(缺乏β-二酮且无诱导II相酶活性)进一步得到了证实[62]。Novaes等人也提出了类似的机制来解释四氢姜黄素对人I相药物代谢细胞色素P450(CYP450)酶(包括CYP2C9和CYP3A4)的抑制作用。根据色谱条件分析,四氢姜黄素的两种酮式和烯醇式互变异构体比例大致相等[36]。他们还假设,四氢姜黄素与姜黄素一样,可能通过芳香甲氧基的去甲基化发生O-脱烷基化反应,从而与CYP450酶结合以促进抑制作用[36]。近期研究表明,在小鼠对乙酰氨基酚诱导的肝损伤中,四氢姜黄素预处理可降低肝脏CYP2E1基因和蛋白表达,且其降低效果强于姜黄素[64]。分子对接研究进一步发现,四氢姜黄素与CYP2E1活性位点中的Arg344、Gly411和Asn143残基形成氢键,而姜黄素则与Leu215、Asn219和Ser366残基相互作用[64]。此外,四氢姜黄素通过转录机制上调解毒酶。它降低了胞质中Keap1蛋白的水平,并增加了核内Nrf2蛋白的水平,从而导致解毒分子——谷氨酸-半胱氨酸连接酶催化亚基(GCLC)、谷氨酸-半胱氨酸连接酶调节亚基(GCLM)和血红素加氧酶-1(HO-1)的转录上调。四氢姜黄素处理后,GCLM和HO-1的上调作用比姜黄素更强。其作用机制推测为:四氢姜黄素通过与Keap1蛋白的Val465和Ser508残基形成氢键插入Keap1的口袋中,从而占据Nrf2结合位点的一部分;干扰了Keap1与Nrf2的结合,最终激活Nrf2及其下游靶点[64]。同样,姜黄素与Keap1蛋白形成氢键的残基与四氢姜黄素完全不同。数据显示,四氢姜黄素对乙酰氨基酚所致肝损伤的肝保护作用强于姜黄素,这归因于其强大的抑制CYP2E1潜力和上调Nrf2的能力,该机制不仅减少了对乙酰氨基酚的代谢转化,还增强了抗氧化损伤的能力[64]。四氢姜黄素还可恢复镉暴露大鼠的肝脏GST活性;然而,其作用机制尚未被研究[62]。
3.3. 抗炎活性
慢性炎症是包括癌症在内的多种疾病的基本特征。与具有快速且自限性特征的先天性炎症不同,慢性炎症表现为失调、未解决且持续存在的病理过程。研究表明其参与肿瘤发生的所有阶段[88]。由基因改变、感染或损伤引起的慢性炎症会触发免疫/炎症细胞浸润,这些细胞释放多种氧化剂和促炎分子,诱导基因组不稳定性,进而导致DNA损伤和启动细胞突变。免疫/炎症细胞与肿瘤细胞产生的多种细胞因子、趋化因子及生长因子可促进启动细胞的恶性转化与增殖、细胞死亡抵抗、血管生成、侵袭及转移。在肿瘤进展过程中,癌细胞、基质细胞与炎症细胞之间通过自分泌和旁分泌模式协调促炎反应,为肿瘤生长维持炎症微环境[88,89]。靶向炎症反应被认为是癌症预防与治疗的相关策略,可通过下调炎症介质、调控炎症信号传导、抑制炎症浸润以及干扰癌细胞与免疫/炎症细胞间的相互作用来实现[89]。
多项研究表明,四氢姜黄素的抗炎效果低于姜黄素。Huang等人报道称,四氢姜黄素对雌性小鼠中肿瘤促进剂12-O-十四烷酰佛波醇-13-乙酸酯(TPA)诱导的耳水肿表现出最高50%的抑制作用,而姜黄素治疗则几乎达到了完全抑制[69]。在TPA刺激的分化HL-60细胞以及经双重TPA处理的小鼠皮肤中,也观察到了类似的O2-•和过氧化氢产生的抑制效应。四氢姜黄素对炎症细胞募集及活性抑制的抑制作用弱于姜黄素,这一点通过活化中性粒细胞中高度表达的表皮髓过氧化物酶(MPO)活性得到证实[65]。在7,12-二甲基苯并蒽/TPA诱导的小鼠皮肤肿瘤发生模型中,四氢姜黄素表现出抗肿瘤促进作用,尽管其活性低于姜黄素,但仍显示出肿瘤数量和发生率的降低[69]。多项研究表明,与姜黄素相比,四氢姜黄素对炎症信号和介质的调节活性相对较弱。在脂多糖(LPS)刺激的鼠巨噬细胞和体内小鼠模型中,四氢姜黄素在抑制IκB磷酸化、核因子-κB(NF-κB)活化以及肿瘤坏死因子-α(TNF-α)产生方面的效果较差[66]。Surh等人还证实,四氢姜黄素对转录因子NF-κB和信号转导及转录激活因子3(STAT3)的DNA结合活性以及下游炎症酶的抑制作用较弱,因此对葡聚糖硫酸钠(DSS)诱导的小鼠结肠炎的抑制作用也弱于姜黄素[68]。然而,Zhao等人研究证明,四氢姜黄素可抑制LPS诱导的RAW264.7小鼠巨噬细胞中的一氧化氮(NO)的产生以及TNF-α和IL-6的分泌,并且在较高浓度下表现出与姜黄素相当的抑制效果。四氢姜黄素还能有效降低诱导型一氧化氮合酶(iNOS)和环氧合酶-2(COX-2)的蛋白水平,并下调NF-κB的核转位。但研究最终得出结论:姜黄素对LPS诱导的炎症反应具有比四氢姜黄素更强的抑制作用[67]。
研究人员通过对姜黄素的结构基序进行修饰,目前已开发出多种合成类似物,这些类似物表现出更高的化学稳定性、生物利用度和生物活性,相关研究已在多篇综述文章中进行探讨[15,90,91]。其中一些类似物显示出比原始姜黄素更好的水溶性、细胞摄取能力、体内生物利用度抗癌效果[92-94];然而,关于姜黄素类似物与四氢姜黄素之间的比较研究相对较少。Pae等人报道,二甲氧基姜黄素——这种合成类似物相较于姜黄素具有更高的代谢稳定性,在LPS刺激的RAW264.7小鼠巨噬细胞中,其抑制NO产生的的效力优于姜黄素和四氢姜黄素[95]。他们的后续研究还表明,在诱导RAW264.7小鼠巨噬细胞中Nrf-2依赖的HO-1表达方面,合成的二甲氧基姜黄素比四氢姜黄素更有效[96]。这些研究不仅证实姜黄素中的两个共轭双键是其抗炎活性所必需的,还揭示了甲氧基数量的增加也起到了重要作用。
四氢姜黄素在LPS刺激的巨噬细胞中的抗炎作用强度可能因四氢姜黄素和LPS的浓度以及处理持续时间的不同而异。最近一项体内研究报告称,四氢姜黄素的抗炎效果优于姜黄素。Zhang等人证明,低剂量(40 mg/kg)的四氢姜黄素在减轻小鼠二甲苯诱导的耳水肿、角叉菜胶诱导的足爪水肿和乙酸诱导的血管通透性方面,表现出与姜黄素(100 mg/kg)相当甚至更强的疗效。研究还发现,在角叉菜胶诱导的足爪水肿中,四氢姜黄素下调COX-2蛋白的作用强于姜黄素,并指出四氢姜黄素可能是比姜黄素更好的选择性抑制剂[48]。然而,体外COX-2抑制试验显示,姜黄素和四氢姜黄素均不是COX-2酶的有效抑制剂,但两者在1 µM浓度下均对脂氧合酶活性表现出强效抑制作用[36]。大多数研究认为,四氢姜黄素较弱的抗炎活性是由于其缺乏姜黄素中存在的α,β-不饱和羰基部分,因而无法作为Michael反应受体发挥作用[19,36]。一项分子对接研究表明,四氢姜黄素与磷脂酶A2(一种参与多种促炎介质形成的酶)的结合能优于姜黄素,通过在活性位点的Gly30残基形成氢键实现的(而姜黄素则在Asp49处形成氢键)。四氢姜黄素与磷脂酶A2蛋白质原子形成的范德华力比姜黄素强得多。该研究表明,四氢姜黄素中心七碳链中双键的缺失可能导致其与姜黄素的结合模式存在差异,进而对炎症酶产生不同的调节机制[52]。总体而言,四氢姜黄素在调节炎症信号通路和介质方面似乎作用较弱,这些因素可能并非其抗癌活性的主要作用机制。
3.4. 抗增殖活性
不受控制的细胞增殖是肿瘤发生和肿瘤扩展中的关键事件。启动细胞中基因突变的积累以及促有丝分裂信号通路的组成性激活,改变了参与细胞周期进程的众多基因、蛋白质和酶的表达与功能,从而导致增殖失调。调控DNA复制、细胞周期进程和促有丝分裂信号通路,是抗增殖策略中具有意义的癌细胞靶点[97]。大量研究表明姜黄素在多种类型癌细胞中具有抗增殖潜力,而四氢姜黄素则鲜少被提及。据报道,在肿瘤促进剂TPA处理的小鼠表皮模型中,四氢姜黄素被发现可(轻微)降低鸟氨酸脱羧酶(ODC)的活性,该酶参与多胺的生物合成[69]。多胺通过维持核酸和染色质结构、调节离子通道及蛋白质合成,对细胞生长和分化至关重要。ODC表达上调会促进多胺合成,进而促进肿瘤的发生和生长。抑制ODC和多胺合成是抑制癌细胞异常增殖的合理方法[98]。
四氢姜黄素降低了TPA诱导的JB6细胞中锚定非依赖性生长,表明其具有抑制转化细胞向肿瘤表型进展的能力;但该效应明显低于姜黄素[69]。在1,2-二甲肼二盐酸盐(DMH)启动的B6C3F1小鼠中,给予0.5%四氢姜黄素处理7周后,结肠中癌前异常隐窝病灶(ACF)的数量显著减少。通过BrdU标记监测发现,膳食四氢姜黄素在抑制结肠隐窝中ACF形成及增殖方面比姜黄素更有效[70]。此外,给予膳食四氢姜黄素23周,在减少偶氮甲烷(AOM)诱导的小鼠结肠大型ACF形成方面比姜黄素更有效。四氢姜黄素在下调iNOS和COX-2以及降低结肠中Wnt-1/β-catenin/p-GSK3β增殖信号方面优于姜黄素[71]。这两项研究表明,膳食摄入四氢姜黄素对结肠癌发生具有比姜黄素更好的体内生物学效应。近期,Zhang等人报道,四氢姜黄素可增强胶质瘤细胞的放射敏感性;当与放射治疗联合使用时,具有协同作用,可抑制细胞集落形成。然而,其放射敏感性弱于姜黄素与放射治疗的联合应用的效果。四氢姜黄素的抗增殖效应降低了细胞周期G1期进程调节因子cyclin D1,以及参与DNA合成的核蛋白增殖细胞核抗原(PCNA)。这两种相互作用均导致胶质瘤细胞发生G0/G1期细胞周期阻滞。联合治疗在异种移植小鼠模型中对胶质瘤生长也表现出更强的抑制作用[72]。值得注意的是,该研究证实四氢姜黄素降低了胶质瘤细胞内的谷胱甘肽(GSH)水平:已有研究表明,升高的GSH水平会增强癌细胞对抗氧化应激的抗氧化能力,而氧化应激在治疗耐药性中起关键作用[99]。四氢姜黄素单独使用或与放射治疗联合应用对降低GSH含量的作用可能与其在胶质瘤细胞中的抗增殖效应有关[72]。由于四氢姜黄素缺乏姜黄素中存在的不饱和β-二酮基团,无法与硫醇反应并耗竭细胞GSH,因此目前尚不清楚其如何介导GSH降低的,需进一步研究验证。事实上,早期研究已揭示四氢姜黄素可在不刺激ROS产生的情况下降低髓系白血病细胞中的GSH含量[39]。
3 .5. 抗转移活性
癌症转移是一个动态的多步骤过程,导致超过了90%的癌症相关死亡率。该过程涉及癌细胞从原发组织扩散至淋巴或血管循环系统,随后在远处器官形成继发性肿瘤。研究表明,多种细胞事件参与癌症转移,例如细胞间黏附丧失、上皮-间质转化(EMT)、运动性和迁移能力增强、周围组织侵袭以及血管生成。阻断这些关键事件为预防癌症转移、疾病进展及由此导致的死亡提供了治疗策略[100]。多项研究表明,四氢姜黄素可作为癌细胞转移的优良抑制剂。在一项体外研究中,四氢姜黄素在Transwell实验中抑制了高转移性HT1080人纤维肉瘤细胞的运动和侵袭。基质金属蛋白酶(MMPs)和尿激酶型纤溶酶原激活物(uPA)等蛋白酶水平的升高参与细胞迁移和侵袭过程中细胞外基质(ECM)的降解。该研究表明,四氢姜黄素不仅消除了MMP-2、MMP-9和uPA的活性,还降低了HT1080细胞中膜型1-MMP的蛋白表达。此外,四氢姜黄素降低了HT1080细胞对Matrigel和层粘连蛋白包被培养板的黏附能力,但对纤维连接蛋白和IV型胶原包被孔的黏附无抑制作用,进一步证实了四氢姜黄素对ECM与癌细胞相互作用的干扰效应[73]。Yoysungnoen等人报道,在体内实验中,四氢姜黄素显示出优于姜黄素的抗血管生成效果。在移植了HepG2异种移植肿瘤的BALB/c裸鼠中,每日口服3000 mg/kg四氢姜黄素可显著降低肿瘤组织内的毛细血管密度,治疗21天后显示出比姜黄素更好的抑制效果。然而,四氢姜黄素降低肿瘤组织新生毛细血管密度的机制尚未得到进一步研究[46]。在宫颈肿瘤组织中也观察到了类似的四氢姜黄素抗血管生成效果[74]。在植入CaSki肿瘤的BALB/c裸鼠,每日口服100、300和500 mg/kg四氢姜黄素,持续30天,结果显示肿瘤组织内的新生毛细血管网络和CD31水平显著降低。肿瘤组织内癌细胞的快速增殖造成了缺氧环境,从而触发血管生成程序,上调缺氧诱导因子(HIF)-1α及其下游的血管内皮生长因子(VEGF),导致肿瘤血管生成和肿瘤进展。口服四氢姜黄素显著降低CaSki肿瘤组织中HIF-1α、VEGF和VEGF受体-2的水平;这支持了四氢姜黄素对肿瘤血管生成的抑制作用[74]。研究还发现,四氢姜黄素下调CaSki肿瘤组织中的COX-2、EGFR、p-ERK1/2和p-AKT表达;这种下调可能是其抑制血管生成和减小肿瘤体积的整体机制的一部分[75]。
在最近的一项研究中,Zhang等人报道了四氢姜黄素的体内抗转移疗效。在通过向裸鼠尾静脉注射骨肉瘤细胞建立的肺转移模型中,腹腔注射100 mg/kg四氢姜黄素(每周5天),持续8周,可显著减少转移结节的数量。实验动物未出现体重下降,也未发生急性或迟发性毒性[76]。一项利用骨肉瘤细胞进行的体外研究探索了四氢姜黄素抗转移特性的分子机制。四氢姜黄素处理上调了上皮标志物E-钙黏蛋白,而与间充质-上皮转化(MET)过程相关的间充质标志物——N-钙黏蛋白、波形蛋白、Snail、ZEB和Twist则被下调。此外,四氢姜黄素通过干扰Akt/mTOR和p38 MAPK 信号通路,抑制了HIF- 1α及其下游靶点(如VEGF、MMP2和MMP9),这些靶点参与侵袭和血管生成[76]。更重要的是,在缺氧条件下,四氢姜黄素能直接抑制骨肉瘤细胞的增殖和HIF-1α的积累,上调VEGF,并诱导MET过程。四氢姜黄素还能减轻缺氧诱导的人脐静脉内皮细胞中毛细血管样管样结构形成。该研究表明,对HIF-1α的调控作用可能使四氢姜黄素成为预防癌症转移的潜在候选药物[76]。
3 .6.程序性细胞死亡的诱导
细胞凋亡是一种程序性细胞死亡,是参与胚胎发育、细胞分化以及维持组织内细胞稳态的关键生理过程。该过程受到一系列细胞外和细胞内信号级联反应、基因转录、分子组装以及效应半胱天冬酶(caspase)激活的严格调控,这些caspase切割多种蛋白质,从而形成细胞凋亡的形态学和生化特征。若细胞凋亡过程中的任一环节出现缺陷,都会导致启动细胞的恶性转化、异常增殖以及对化疗药物产生耐药性[101]。诱导细胞凋亡是当前癌症治疗中一种有前景且广泛应用的策略。此外,迫切需要一种通过增强细胞凋亡或其他机制来克服癌症对化疗产生耐药性的有效方法[101]。
由于四氢姜黄素的毒性低于姜黄素,因此其应用很少被考虑,这并不令人意外[44-46]。尽管如此,仍有一些研究报道了四氢姜黄素对诱导癌细胞凋亡的作用。Kang等人研究显示,四氢姜黄素对人乳腺癌细胞表现出细胞毒性作用,IC50为33.08 µM,而姜黄素的IC50为19.68 µM[77]。四氢姜黄素可诱导MCF-7细胞线粒体依赖性凋亡,其证据包括线粒体跨膜电位(∆Ψm)丧失、Bax表达上调、Bcl-2表达降低、细胞色素c释放以及procaspases的切割。细胞周期蛋白依赖性激酶抑制剂p21的上调也参与了四氢姜黄素触发的凋亡过程[77]。Han等人进行的研究也观察到了类似结果,即四氢姜黄素诱导的线粒体依赖性凋亡可能归因于MCF-7细胞内活性氧(ROS)水平的升高[78]。在H22腹水瘤模型中,每日给小鼠腹腔注射5、10和20 mg/kg四氢姜黄素,持续7天,其存活率显著高于100 mg/kg姜黄素治疗组。与更高剂量的姜黄素相比,使用20 mg/kg四氢姜黄素观察到肿瘤重量和腹水体积更显著的减轻效果。此外,四氢姜黄素在增加H22诱导的腹水瘤细胞凋亡方面比姜黄素更有效。在分子水平上,四氢姜黄素和姜黄素均触发线粒体依赖性级联反应、上调p53并降低MDM2(p53的负调控因子)来诱导凋亡[79]。尽管它们具有相同的分子机制,但四氢姜黄素在体内抗肿瘤和诱导凋亡方面表现出优于姜黄素的效果。两项研究表明四氢姜黄素对恶性胶质瘤的化疗和放疗具有增敏作用。用20 µM四氢姜黄素预处理可显著增强放射治疗诱导的胶质瘤C6细胞凋亡[72]。在胶质瘤细胞中,使用四氢姜黄素和阿霉素共载的转铁蛋白修饰纳米粒预处理,比单独使用阿霉素纳米粒处理产生了显著更大的细胞毒性效应。通过四氢姜黄素和载阿霉素的转铁蛋白修饰纳米粒预处理,使胶质瘤C6细胞对放射治疗增敏,表现为集落形成减少[102]。这些研究表明,四氢姜黄素的联合应用是增强胶质瘤放疗敏感性的一种有前景的策略。然而,四氢姜黄素对放疗增敏作用的具体分子机制尚未得到研究。
自噬是另一种程序性细胞死亡方式。尽管其在癌症中的作用较为复杂,但仍可能为癌症治疗提供一种有效的治疗策略[103]。自噬似乎是四氢姜黄素一种特有的细胞毒性活性,与姜黄素对癌细胞的作用完全不同。Wu等人研究表明,四氢姜黄素可诱导酸性囊泡细胞器(AVOs)的形成,而姜黄素则诱导人HL-60早幼粒细胞白血病细胞发生凋亡。自噬体标志物LC3的上调反映了四氢姜黄素诱导的自噬性细胞死亡。研究还发现,四氢姜黄素通过抑制PI3K/Akt和mTOR/p70S6K信号通路,在HL-60细胞中触发自噬[80]。在阿糖胞苷耐药的HL-60细胞中,四氢姜黄素通过上调p62和LC3诱导自噬,而姜黄素则通过激活caspases引发细胞凋亡[81]。这些发现提示四氢姜黄素在克服癌症耐药性方面具有新型治疗应用价值。四氢姜黄素抑制P-糖蛋白以及ABCC1和ABCG2(均为多药耐药蛋白)的外排功能,从而提高耐药癌细胞对化疗药物的敏感性。四氢姜黄素逆转多药耐药表型的机制可能与其与转运蛋白药物结合位点的相互作用有关,这一点通过P-糖蛋白和ABCG2ATP酶活性的增强得到证实[104]。四氢姜黄素诱导自噬的作用在非小细胞肺癌细胞中同样得到证实。用四氢姜黄素处理A549肺癌细胞,通过提高LC3 I/II比值和Beclin-1水平,同时下调PI3K/Akt/mTOR信号通路,导致自噬性细胞死亡[82]。
3.7 免疫调节活性
癌细胞通过多种机制逃避免疫监视和免疫清除。巨噬细胞和髓系免疫细胞吞噬清除功能的受损是癌症侵袭与转移的重要机制。已知癌细胞通过表达CD47受体操控巨噬细胞以逃避免疫监视;阻断CD47/信号调节蛋白α(SIRPα)轴可增强癌细胞吞噬作用及免疫应答[105]。两项体外研究表明,四氢姜黄素无论是否存在脂多糖(LPS)刺激条件下均能刺激RAW264.7巨噬细胞的吞噬活性[83,84]。此外,四氢姜黄素还能增强LPS刺激下培养上清液(小鼠脾细胞)中NK细胞的活性。四氢姜黄素的刺激作用比姜黄素更强[84]。然而,四氢姜黄素刺激吞噬作用的具体机制尚需进一步研究。
4.通过结构修饰和递送效率提升四氢姜黄素生物活性
由于缺乏α, β-不饱和β-二酮结构,四氢姜黄素在亲核加成反应中的反应性低于姜黄素[19,36]。对四氢姜黄素进行结构修饰可改善其原有的抗癌活性,并产生额外的、独特的生物学功能。近期一项研究表明,合成的四氢姜黄素-铱(Ir)III配合物在可见光照射下,对HeLa细胞表现出显著且快速的细胞毒性效应。四氢姜黄素-Ir III引发的光毒性效应高于姜黄素-Ir III,为光动力治疗提供了新的应用方向[106]。Mahal等人分别通过四氢姜黄素与各种肼类和伯胺直接缩合,合成了其吡唑类和席夫碱类衍生物。这些合成的吡唑类和席夫碱类四氢姜黄素衍生物在A549、HeLa和MCF-7癌细胞中大多表现出比四氢姜黄素更强的细胞毒性效应[107,108]。
尽管四氢姜黄素被认为在体内具有优于姜黄素的生物学效应,但其应用仍受到低水溶性的限制。不同的纳米技术已被证实可以改善四氢姜黄素的水溶性。两项研究报道了一种通过混合不同的油、表面活性剂和助表面活性剂形成四氢姜黄素纳米乳剂的自乳化药物递送系统,与未修饰的四氢姜黄素相比,该系统在模拟胃液中的溶解度显著提高[109,110]。Kakkar等人制备了四氢姜黄素的脂质纳米粒,在酒精和磷酸盐缓冲液混合介质中,显示出比游离四氢姜黄素更高且更快的药物释放。四氢姜黄素药物释放的增加归因于其水溶性的增强[111]。其他研究表明,将四氢姜黄素与葡萄糖基团结合,或通过微乳化或液体自乳化技术与羧甲基纤维素配制,可提高其生物利用度。采用上述方法,四氢姜黄素的递送、吸收和可控释放均得到显著改善,从而增强了其生物学功效[110–113]。上述研究表明,四氢姜黄素纳米粒及其结合物未来有望成为有前景的化学预防和治疗剂;然而,此类制剂的药代动力学特性尚待确定。
5. 结论与未来展望
四氢姜黄素因其相对优越的化学稳定性和生物利用度,以及与姜黄素高度相似的结构,被认为是开发癌症预防和治疗药物的有价值的先导化合物。本综述所讨论的四氢姜黄素的抗癌特性,被认为源于其强大的抗氧化能力。这些特性通过调节多种信号分子和基因表达,与参与炎症、增殖、转移、程序性细胞死亡及免疫功能的酶和蛋白质相互作用而产生的(图3)。尽管四氢姜黄素缺乏反应性的α, β-不饱和β-二酮结构,但它以不同的酮-烯醇形式及其他类似物存在,这可能与其不同于姜黄素的功能和机制多样性有关。前瞻性研究以确定四氢姜黄素的确切分子靶点,将为开发新型高效预防和治疗多种人类恶性肿瘤的策略提供重要指导。
图3. 四氢姜黄素在癌症预防与治疗中的潜在作用机制及分子靶点。
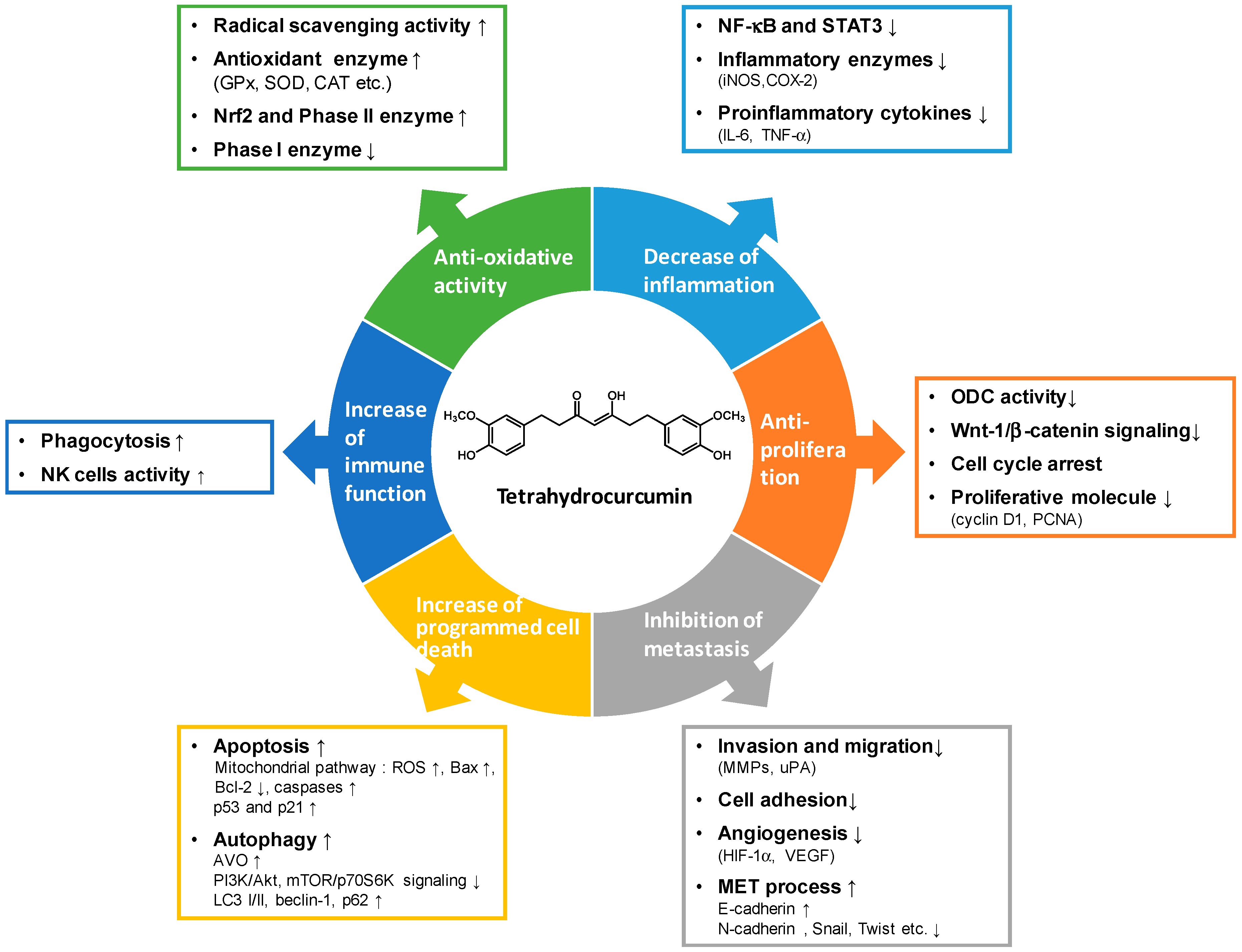
尽管四氢姜黄素具有有益的抗癌作用,但其临床转化仍需克服诸多挑战。例如,在多项研究中,四氢姜黄素表现出比姜黄素更强的有益效果;然而,这些研究大多基于细胞系和动物实验。需要对四氢姜黄素颇具前景的抗癌潜力进行临床研究,并深入探究其确切的作用机制。此外,四氢姜黄素生物利用度差是其临床应用的主要限制因素。尽管已经开发了多种递送系统来提高四氢姜黄素的水溶性、摄取和药物释放,但仍需在临床试验中加以验证。同时,确定四氢姜黄素对人体临床安全性和有效性方面的生理相关剂量也至关重要。
免责声明
以上部分内容来源于外网我们重在信息分享,版权归属原作者或原刊发平台所有,如有侵权、信息有误或其他异议,请联系处理,我们将在24小时内删除或整改。
复合免疫 健康活力





























